Fonte do estudo: https://ivmmeta.com/
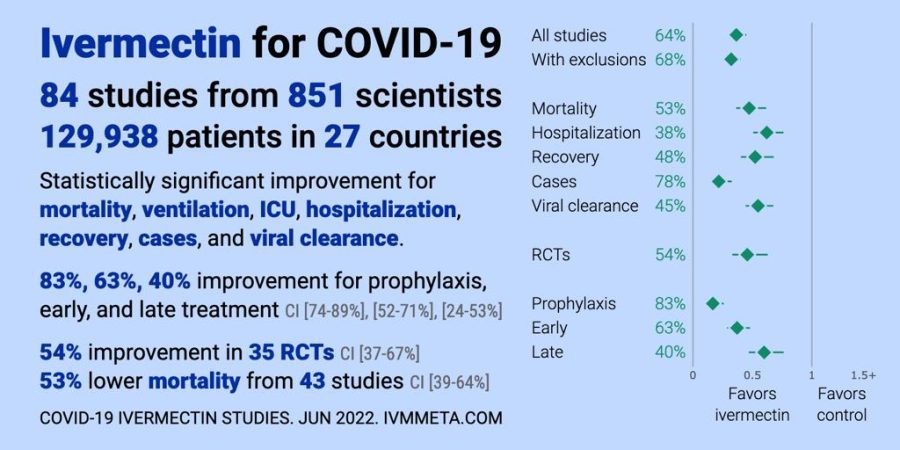
Ivermectina para COVID-19: meta-análise em tempo real de 85 estudos
GMK ,
BBC ,
Strongyloides00.511.5+All studies63%85131,529Improvement, Studies, PatientsRelative RiskPrimary outcome56%85131,582Mortality52%44118,686Ventilation31%1532,212ICU admission54%822,347Hospitalization37%2442,867Recovery46%296,178Cases78%1513,297Viral clearance45%263,096RCTs54%368,828Peer-reviewed63%63119,529Prophylaxis83%1619,365Early63%3356,011Late40%3656,153Ivermectin for COVID-19ivmmeta.com Jun 2022FavorsivermectinFavorscontrolafter exclusions
•Melhorias estatisticamente significativas são observadas para
casos e
eliminação viral . Todos permanecem significativos após as
exclusões . 55 estudos de 50 equipes independentes em 22 países diferentes mostram melhorias estatisticamente significativas isoladamente (39 desfechos primários, 36 desfechos mais graves).
•A meta-análise usando o desfecho mais grave mostra 63%
[52-71%] e 83%
[74-89%] de melhora para
tratamento e profilaxia precoces , com resultados semelhantes após
análise de sensibilidade baseada em exclusão , para
desfechos primários , para

estudos revisados por pares , e para
ECRs .
•Os resultados são muito robustos — na análise de sensibilidade de exclusão de pior caso, 54 de 85 estudos devem ser excluídos para evitar encontrar eficácia estatisticamente significativa.
•Embora
muitos tratamentos tenham algum nível de eficácia, eles não substituem as vacinas e outras medidas para evitar a infecção. Apenas 24% dos estudos com ivermectina mostram zero eventos no braço de tratamento.
Vários tratamentos são normalmente usados em combinação, o que pode ser significativamente mais eficaz.
•Nenhum tratamento, vacina ou intervenção está 100% disponível e eficaz para todas as variantes. Todos os meios práticos, eficazes e seguros devem ser usados. Negar a eficácia dos tratamentos aumenta a mortalidade, morbidade, danos colaterais e risco endêmico.
•Mais de 20 países adotaram a ivermectina para o COVID-19. A base de evidências é
muito maior e tem um conflito de interesses muito menor do que normalmente usado para aprovar medicamentos.
•Todos os dados para reproduzir este artigo e fontes estão no
apêndice . Veja
[ Bryant , Hariyanto , Kory , Lawrie , Nardelli ] para
outras meta-análises com resultados semelhantes confirmando a eficácia.
| Base de evidências usada para outras aprovações COVID-19 | |||
| Medicamento | Estudos | Pacientes | Melhoria |
| Molnupiravir (Reino Unido) | 1 | 775 | 50% |
| Budesonida (Reino Unido) | 1 | 1.779 | 17% |
| Remdesivir (EUA EUA) | 1 | 1.063 | 31% |
| Casirivimab/i.. (EUA EUA) | 1 | 799 | 66% |
| Evidência de ivermectina | 85 | 131.529 | 63% [55-70%] |
DESTAQUESA ivermectina reduz o risco de COVID-19 com confiança muito alta para
casos ,
eliminação viral e em
análises agrupadas .Mostramos análises tradicionais específicas de resultados e evidências combinadas de todos os estudos, incorporando o atraso no tratamento, um fator de confusão primário nos estudos COVID-19.
Atualizações e correções em tempo real , análise transparente com todos os resultados no mesmo formato, protocolo consistente para
42 tratamentos .UMA00.250.50.7511.251.51.752+Chowdhury (RCT)81%0.19 [0.01-3.96]14mghosp.0/602/56OT1 CT2Improvement, RR [CI]Dose (4d)TreatmentControlEspitia-Hernandez70%0.30 [0.16-0.55]12mgrecov. time28 (n)7 (n)CT2Carvallo85%0.15 [0.02-1.28]36mgdeath1/323/14CT2Mahmud (DB RCT)86%0.14 [0.01-2.75]12mgdeath0/1833/183CT2Szente Fonseca-14%1.14 [0.75-1.66]24mghosp.340 (n)377 (n)Cadegiani78%0.22 [0.01-4.48]42mgdeath0/1102/137CT2Ahmed (DB RCT)85%0.15 [0.01-2.70]48mgsymptoms0/173/19Chaccour (DB RCT)96%0.04 [0.00-1.01]28mgsymptoms12 (n)12 (n)Ghauri92%0.08 [0.01-0.88]48mgno recov.0/377/53Babalola (DB RCT)64%0.36 [0.10-1.27]24mgviral+40 (n)20 (n)OT1Ravikirti (DB RCT)89%0.11 [0.01-2.05]24mgdeath0/554/57Bukhari (RCT)82%0.18 [0.07-0.46]12mgviral+4/4125/45Mohan (DB RCT)62%0.38 [0.08-1.75]28mgno recov.2/406/45Biber (DB RCT)70%0.30 [0.03-2.76]36mghosp.1/473/42Elalfy87%0.13 [0.06-0.27]36mgviral+7/6244/51CT2López-Me.. (DB RCT)67%0.33 [0.01-8.11]84mgdeath0/2001/198Roy6%0.94 [0.52-1.93]n/arecov. time14 (n)15 (n)CT2Chahla (CLUS. RCT)87%0.13 [0.03-0.54]24mgno disch.2/11020/144Mourya89%0.11 [0.05-0.25]48mgviral+5/5047/50Loue (QR)70%0.30 [0.04-2.20]14mgdeath1/105/15Merino (QR)74%0.26 [0.11-0.57]24mghosp.population-based cohortcensored, see notes CS5Faisal (RCT)68%0.32 [0.14-0.72]48mgno recov.6/5019/50Aref (RCT)63%0.37 [0.22-0.61]n/arecov. time57 (n)57 (n)Krolewiecki (RCT)-152%2.52 [0.11-58.1]168mgventilation1/270/14Vallejos (DB RCT)-33%1.33 [0.30-5.72]24mgdeath4/2503/251Reis (DB RCT)12%0.88 [0.49-1.55]84mgdeath21/67924/679Buonfrate (DB RCT)-211%3.11 [0.13-73.3]336mghosp.1/280/31Mayer55%0.45 [0.32-0.63]151mgdeath3,266 (n)17,966 (n)Borody92%0.08 [0.01-0.79]96mgdeath0/6006/600CT2 SC4Abbas (DB RCT)-4%1.04 [0.07-16.4]84mgdeath1/991/103de Jesús Ascenci..59%0.41 [0.36-0.47]12mgdeath/hosp.7,898 (n)20,150 (n)CT2Manomai.. (DB RCT)43%0.57 [0.20-1.46]48mgno recov.3/366/36Rocha (DB RCT)-187%2.87 [0.12-67.5]36mgmisc.1/300/26Tau2 = 0.18, I2 = 56.2%, p < 0.0001Early treatment63%0.37 [0.29-0.48]61/14,508234/41,50363% improvementShouman (RCT)91%0.09 [0.03-0.23]36mgsymp. case15/20359/101Improvement, RR [CI]Dose (1m)TreatmentControlCarvallo96%0.04 [0.00-0.63]14mgcases0/13111/98see notes CT2Behera54%0.46 [0.29-0.71]42mgcases41/117145/255Carvallo100%0.00 [0.00-0.02]48mgcases0/788237/407see notes CT2Hellwig (ECO.)78%0.22 [0.06-0.76]14mgcasesecologicalBernigaud99%0.01 [0.00-0.10]84mgdeath0/69150/3,062Alam91%0.09 [0.04-0.25]12mgcases4/5844/60IVERCOR PREP73%0.27 [0.15-0.48]48mgcases13/38961/486MD3Chahla (RCT)95%0.05 [0.00-0.80]48mgm/s case0/11710/117CT2Behera83%0.17 [0.12-0.23]42mgcases45/2,199133/1,147Tanioka (ECO.)88%0.12 [0.03-0.46]14mgdeathecologicalSeet (CLUS. RCT)50%0.50 [0.33-0.76]12mgsymp. case32/61764/619OT1Morgenstern (PSM)80%0.20 [0.01-4.15]56mghosp.0/2712/271Mondal88%0.12 [0.01-0.55]n/asymp. case128 (n)1,342 (n)Samajdar80%0.20 [0.11-0.38]n/acases12/16429/81Kerr (PSM)70%0.30 [0.19-0.46]56mgdeath25/3,03479/3,034Tau2 = 0.45, I2 = 81.8%, p < 0.0001Prophylaxis83%0.17 [0.11-0.26]187/8,2851,024/11,08083% improvementAll studies72%0.28 [0.22-0.35]248/22,7931,258/52,58372% improvementIvermectin COVID-19 early treatment and prophylaxis studiesivmmeta.com Jun 2022Tau2 = 0.30, I2 = 73.4%, p < 0.0001Effect extraction pre-specified, see appendix1 OT: ivermectin vs. other treatment3 MD: minimal detail available currently5 CS: preprint censored, see details2 CT: study uses combined treatment4 SC: study uses synthetic control armFavors ivermectinFavors controlB
 C
C
 D
D

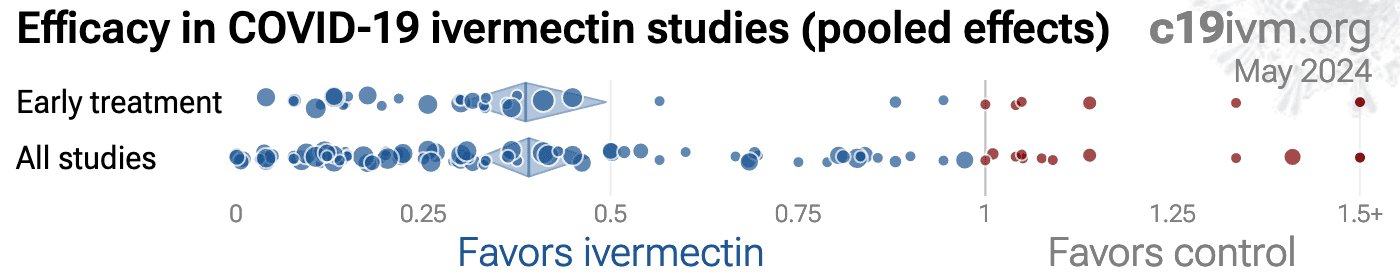
Figura 1. A. Meta-análise de efeitos aleatórios excluindo tratamento tardio. Este gráfico mostra os efeitos agrupados, a análise para os resultados individuais está abaixo e mais detalhes sobre os efeitos agrupados podem ser encontrados na seção de heterogeneidade. A extração do efeito é pré-especificada, usando o resultado mais grave relatado. As dosagens simplificadas são mostradas para comparação, estas são a dose total nos primeiros quatro dias para tratamento e a dose mensal para profilaxia, para uma pessoa de 70kg. Para detalhes da extração do efeito e informações completas sobre a dosagem, consulte o
apêndice .
B. Gráfico de dispersão mostrando a distribuição dos efeitos relatados nos estudos iniciais de tratamento e em todos os estudos.
C e DHistórico cronológico de todos os efeitos relatados, com a probabilidade de que a frequência observada ou maior de resultados positivos tenha sido gerada por um tratamento ineficaz.
Analisamos todos os estudos significativos sobre o uso de ivermectina para COVID-19. Métodos de busca, critérios de inclusão, critérios de extração de efeitos (resultados mais graves têm prioridade), todos os dados de estudos individuais, respostas PRISMA e métodos estatísticos estão detalhados no
Apêndice 1 . Apresentamos os resultados da meta-análise de efeitos aleatórios para todos os estudos, estudos dentro de cada estágio de tratamento, resultados específicos, estudos revisados por pares, ensaios controlados randomizados (RCTs) e após exclusões.Também realizamos uma análise simples da distribuição dos efeitos do estudo. Se o tratamento não fosse eficaz, os efeitos observados seriam distribuídos aleatoriamente (ou com maior probabilidade de serem negativos se o tratamento for prejudicial). Podemos calcular a probabilidade de que a porcentagem observada de resultados positivos (ou superior) possa ocorrer devido ao acaso com um tratamento ineficaz (a probabilidade de >=
k caras em
n lançamentos de moedas, ou o teste de sinal unilateral / teste binomial). A análise do viés de publicação é importante e ajustes podem ser necessários se houver um viés de publicação de resultados positivos.
A Figura 2 mostra as etapas do possível tratamento para COVID-19.
A profilaxia refere-se a tomar medicamentos regularmente antes de adoecer, a fim de prevenir ou minimizar a infecção.
O Tratamento Precoce refere-se ao tratamento imediatamente ou logo após o aparecimento dos sintomas, enquanto
o Tratamento Tardio refere-se ao tratamento mais tardio.

Figura 2. Etapas do tratamento.Pesquisa pré-clínica18 Estudos
in Silico comprovam a eficácia da ivermectina
[ Alvarado , Aminpour , Bello , Choudhury , Eweas , Francés-Monerris , Francés-Monerris (B) , González-Paz , González-Paz (B) , Kern , Muthusamy , Parvez , Qureshi , Rana , Saha , Schöning , Swargiary , Udofia ] .12 Estudos
in vitro apoiam a eficácia da ivermectina
[ Caly , Delandre , Jeffreys , Jitobaom , Jitobaom (B) , Li , Liu , Mody , Mountain Valley MD , Segatori , Surnar , Yesilbag ] .7 Estudos em animais
in vivo comprovam a eficácia da ivermectina
[ Albariqi , Arévalo , Chaccour , de Melo , Errecalde , Madrid , Zheng ] .5 estudos investigam novas formulações de ivermectina que podem ser mais eficazes para COVID-19
[ Albariqi , Albariqi (B) , Chaccour , Errecalde , Mansour ] .A pesquisa pré-clínica é uma parte importante do desenvolvimento de tratamentos, porém os resultados podem ser muito diferentes nos ensaios clínicos. Os resultados pré-clínicos não são usados neste artigo.Resultados
A Figura 3 mostra uma visão geral dos resultados. As Figuras
4 ,
5 e
6 mostram os resultados por estágio de tratamento. Figura
7 ,
8 ,
9 ,
10 ,
11 ,
12 ,
13 e
14 mostram gráficos de floresta para uma meta-análise de efeitos aleatórios de todos os estudos com efeitos agrupados e para estudos que relatam resultados de mortalidade, admissão na UTI, ventilação mecânica, hospitalização, recuperação , casos de COVID-19 e apenas resultados de depuração viral.
A Figura 15 mostra os resultados apenas para ensaios revisados por pares e os
dados complementarescontém resultados revisados por pares e resultados individuais após exclusões.
A Tabela 1 e a
Tabela 2 resumem os resultados.00.511.5+ALL STUDIESPRIMARY OUTCOMEMORTALITYVENTILATIONICU ADMISSIONHOSPITALIZATIONRECOVERYCASESVIRAL CLEARANCERANDOMIZED CONTROLLED TRIALSPEER-REVIEWEDAfter ExclusionsALL STUDIESPRIMARY OUTCOMEMORTALITYVENTILATIONICU ADMISSIONHOSPITALIZATIONRECOVERYCASESVIRAL CLEARANCERANDOMIZED CONTROLLED TRIALSPEER-REVIEWEDAllProphylaxisEarlyLateIvermectin for COVID-19IVMMETA.COM JUN 2022
Figura 3. Visão geral dos resultados.
| Tempo de tratamento | Número de estudos relatando efeitos positivos | Número total de estudos | Porcentagem de estudos relatando efeitos positivos | Probabilidade de uma porcentagem igual ou maior de resultados positivos de um tratamento ineficaz | Resultados de meta-análise de efeitos aleatórios |
| Tratamento precoce | 27 | 33 | 81,8% | 1 em 6 mil | 63% de melhora RR 0,37 [0,29-0,48] p < 0,0001 |
| Tratamento tardio | 29 | 36 | 80,6% | 1 em 6 mil | 40% de melhora RR 0,60 [0,47-0,77] p < 0,0001 |
| Profilaxia | 16 | 16 | 100% | 1 em 66 mil | 83% de melhora RR 0,17 [0,11-0,26] p < 0,0001 |
| Todos os estudos | 72 | 85 | 84,7% | 1 em 43 bilhões | 63% de melhora RR 0,37 [0,30-0,45] p < 0,0001 |
Tabela 1. Resultados por fase de tratamento.
| Estudos | Profilaxia | Tratamento precoce | Tratamento tardio | Pacientes | Autores | |
| Todos os estudos | 85 | 83% [74-89%] | 63% [52-71%] | 40% [23-53%] | 131.529 | 852 |
| Revisado por pares | 63 | 83% [73-90%] | 62% [50-72%] | 41% [18-57%] | 119.529 | 679 |
| Após exclusões | 58 | 82% [68-89%] | 69% [61-76%] | 53% [33-68%] | 116.680 | 632 |
| Ensaios controlados randomizados | 36 | 84% [25-96%] | 59% [41-71%] | 23% [0-40%] | 8.828 | 457 |
| ECRs após exclusões | 30 | 84% [25-96%] | 66% [54-75%] | 29% [4-47%] | 6.706 | 370 |
Tabela 2. Resultados por estágio de tratamento para todos os estudos e com diferentes exclusões.
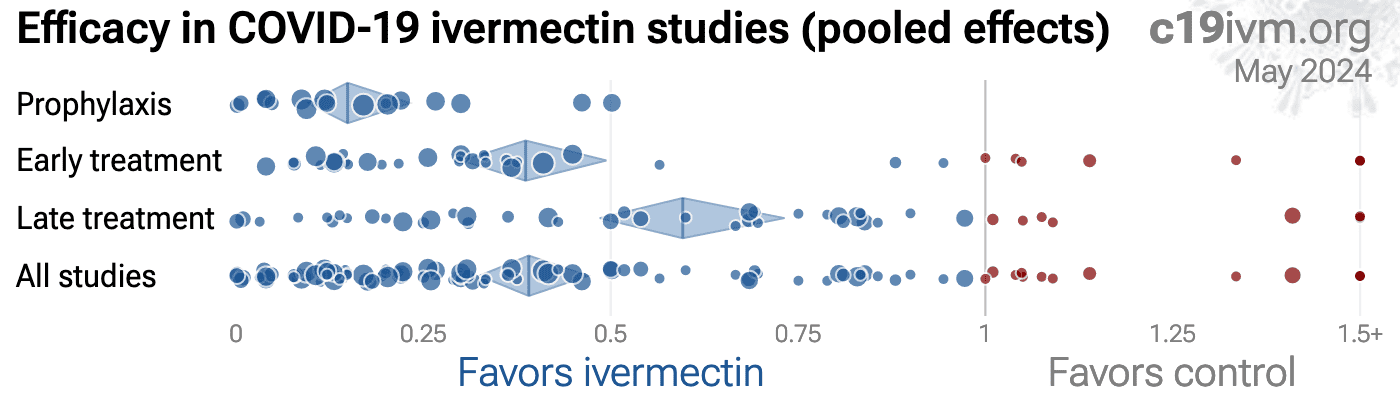
Figura 4. Resultados por fase de tratamento.


Figura 5. Histórico cronológico dos resultados do tratamento precoce e tardio, com a probabilidade de que a frequência observada ou maior de resultados positivos tenha sido gerada por um tratamento ineficaz.

Figura 6. Histórico cronológico dos resultados da profilaxia.00.250.50.7511.251.51.752+Chowdhury (RCT)81%0.19 [0.01-3.96]14mghosp.0/602/56OT1 CT2Improvement, RR [CI]Dose (4d)TreatmentControlEspitia-Hernandez70%0.30 [0.16-0.55]12mgrecov. time28 (n)7 (n)CT2Carvallo85%0.15 [0.02-1.28]36mgdeath1/323/14CT2Mahmud (DB RCT)86%0.14 [0.01-2.75]12mgdeath0/1833/183CT2Szente Fonseca-14%1.14 [0.75-1.66]24mghosp.340 (n)377 (n)Cadegiani78%0.22 [0.01-4.48]42mgdeath0/1102/137CT2Ahmed (DB RCT)85%0.15 [0.01-2.70]48mgsymptoms0/173/19Chaccour (DB RCT)96%0.04 [0.00-1.01]28mgsymptoms12 (n)12 (n)Ghauri92%0.08 [0.01-0.88]48mgno recov.0/377/53Babalola (DB RCT)64%0.36 [0.10-1.27]24mgviral+40 (n)20 (n)OT1Ravikirti (DB RCT)89%0.11 [0.01-2.05]24mgdeath0/554/57Bukhari (RCT)82%0.18 [0.07-0.46]12mgviral+4/4125/45Mohan (DB RCT)62%0.38 [0.08-1.75]28mgno recov.2/406/45Biber (DB RCT)70%0.30 [0.03-2.76]36mghosp.1/473/42Elalfy87%0.13 [0.06-0.27]36mgviral+7/6244/51CT2López-Me.. (DB RCT)67%0.33 [0.01-8.11]84mgdeath0/2001/198Roy6%0.94 [0.52-1.93]n/arecov. time14 (n)15 (n)CT2Chahla (CLUS. RCT)87%0.13 [0.03-0.54]24mgno disch.2/11020/144Mourya89%0.11 [0.05-0.25]48mgviral+5/5047/50Loue (QR)70%0.30 [0.04-2.20]14mgdeath1/105/15Merino (QR)74%0.26 [0.11-0.57]24mghosp.population-based cohortcensored, see notes CS5Faisal (RCT)68%0.32 [0.14-0.72]48mgno recov.6/5019/50Aref (RCT)63%0.37 [0.22-0.61]n/arecov. time57 (n)57 (n)Krolewiecki (RCT)-152%2.52 [0.11-58.1]168mgventilation1/270/14Vallejos (DB RCT)-33%1.33 [0.30-5.72]24mgdeath4/2503/251Reis (DB RCT)12%0.88 [0.49-1.55]84mgdeath21/67924/679Buonfrate (DB RCT)-211%3.11 [0.13-73.3]336mghosp.1/280/31Mayer55%0.45 [0.32-0.63]151mgdeath3,266 (n)17,966 (n)Borody92%0.08 [0.01-0.79]96mgdeath0/6006/600CT2 SC4Abbas (DB RCT)-4%1.04 [0.07-16.4]84mgdeath1/991/103de Jesús Ascenci..59%0.41 [0.36-0.47]12mgdeath/hosp.7,898 (n)20,150 (n)CT2Manomai.. (DB RCT)43%0.57 [0.20-1.46]48mgno recov.3/366/36Rocha (DB RCT)-187%2.87 [0.12-67.5]36mgmisc.1/300/26Tau2 = 0.18, I2 = 56.2%, p < 0.0001Early treatment63%0.37 [0.29-0.48]61/14,508234/41,50363% improvementGorial71%0.29 [0.01-5.76]14mgdeath0/162/71Improvement, RR [CI]Dose (4d)TreatmentControlKishoria (RCT)-8%1.08 [0.57-2.02]12mgno disch.11/197/13Podder (RCT)16%0.84 [0.55-1.12]14mgrecov. time32 (n)30 (n)Khan87%0.13 [0.02-1.00]12mgdeath1/1159/133Chachar (RCT)10%0.90 [0.44-1.83]36mgno recov.9/2510/25Soto-Becerra17%0.83 [0.71-0.97]14mgdeath92/2031,438/2,630Rajter (PSM)46%0.54 [0.27-0.99]14mgdeath13/9824/98Hashim (SB RCT)92%0.08 [0.00-1.44]28mgdeath0/596/70CT2Camprubí40%0.60 [0.18-2.01]14mgventilation3/135/13Spoorthi21%0.79 [0.64-0.98]n/arecov. time50 (n)50 (n)CT2Budhiraja99%0.01 [0.00-0.15]n/adeath0/34103/942Okumuş (DB RCT)33%0.67 [0.27-1.64]56mgdeath6/309/30Shahbazn.. (DB RCT)-197%2.97 [0.13-70.5]14mgdeath1/350/34Lima-Morales78%0.22 [0.12-0.41]12mgdeath15/48152/287CT2Beltran .. (DB RCT)14%0.86 [0.29-2.56]12mgdeath5/366/37Pott-Junior (RCT)85%0.15 [0.01-1.93]14mgventilation1/271/4censored, see notesHuvemek (DB RCT)32%0.68 [0.38-1.23]84mgno improv.13/5019/50Ahsan50%0.50 [0.28-0.90]21mgdeath17/11017/55CT2Abd-Elsalam (RCT)25%0.75 [0.17-3.06]36mgdeath3/824/82Hazan86%0.14 [0.01-2.15]24mgdeath0/24syntheticCT2 SC4Elavarasi20%0.80 [0.61-1.06]n/adeath48/283311/1,475Rezk80%0.20 [0.01-4.13]72mgdeath0/1602/160Lim (RCT)69%0.31 [0.09-1.11]112mgdeath3/24110/249Ozer75%0.25 [0.06-1.13]28mgdeath2/608/60Ferreira-5%1.05 [0.32-3.43]n/adeath3/2111/81Jamir (ICU)-53%1.53 [0.88-2.67]n/adeath32/7669/190ICU patientsBaguma97%0.03 [0.00-11.7]n/adeath7 (n)474 (n)Mustafa64%0.36 [0.12-1.14]variesdeath3/7342/371Shimizu100%0.00 [0.00-0.01]14mgdeath0/398/49Zubair-9%1.09 [0.33-3.64]12mgdeath5/905/98Thairu (PSM)88%0.12 [0.01-2.14]56mgdeath0/214/26Efimenko (PSM)69%0.31 [0.20-0.48]n/adeath1,072 (n)40,536 (n)self-censored, see notes OT1Soto-41%1.41 [1.16-1.76]n/adeath280/484374/934Ravikirti3%0.97 [0.74-1.24]variesdeath53/171254/794George (RCT)30%0.70 [0.25-1.93]24mgdeath5/358/39Naggie (DB RCT)-195%2.95 [0.12-72.2]84mgdeath1/8170/774Tau2 = 0.24, I2 = 80.6%, p < 0.0001Late treatment40%0.60 [0.47-0.77]625/5,1892,818/50,96440% improvementShouman (RCT)91%0.09 [0.03-0.23]36mgsymp. case15/20359/101Improvement, RR [CI]Dose (1m)TreatmentControlCarvallo96%0.04 [0.00-0.63]14mgcases0/13111/98see notes CT2Behera54%0.46 [0.29-0.71]42mgcases41/117145/255Carvallo100%0.00 [0.00-0.02]48mgcases0/788237/407see notes CT2Hellwig (ECO.)78%0.22 [0.06-0.76]14mgcasesecologicalBernigaud99%0.01 [0.00-0.10]84mgdeath0/69150/3,062Alam91%0.09 [0.04-0.25]12mgcases4/5844/60IVERCOR PREP73%0.27 [0.15-0.48]48mgcases13/38961/486MD3Chahla (RCT)95%0.05 [0.00-0.80]48mgm/s case0/11710/117CT2Behera83%0.17 [0.12-0.23]42mgcases45/2,199133/1,147Tanioka (ECO.)88%0.12 [0.03-0.46]14mgdeathecologicalSeet (CLUS. RCT)50%0.50 [0.33-0.76]12mgsymp. case32/61764/619OT1Morgenstern (PSM)80%0.20 [0.01-4.15]56mghosp.0/2712/271Mondal88%0.12 [0.01-0.55]n/asymp. case128 (n)1,342 (n)Samajdar80%0.20 [0.11-0.38]n/acases12/16429/81Kerr (PSM)70%0.30 [0.19-0.46]56mgdeath25/3,03479/3,034Tau2 = 0.45, I2 = 81.8%, p < 0.0001Prophylaxis83%0.17 [0.11-0.26]187/8,2851,024/11,08083% improvementAll studies63%0.37 [0.30-0.45]873/27,9824,076/103,54763% improvementAll 85 ivermectin COVID-19 studiesivmmeta.com Jun 2022Tau2 = 0.51, I2 = 87.5%, p < 0.0001Effect extraction pre-specified, see appendix1 OT: ivermectin vs. other treatment3 MD: minimal detail available currently5 CS: preprint censored, see details2 CT: study uses combined treatment4 SC: study uses synthetic control armFavors ivermectinFavors control
Figura 7. Meta-análise de efeitos aleatórios para todos os estudos. Este gráfico mostra os efeitos agrupados, a análise para os resultados individuais está abaixo e mais detalhes sobre os efeitos agrupados podem ser encontrados na seção de heterogeneidade. A extração do efeito é pré-especificada, usando o resultado mais grave relatado. As dosagens simplificadas são mostradas para comparação, estas são a dose total nos primeiros quatro dias para tratamento e a dose mensal para profilaxia, para uma pessoa de 70kg. Para detalhes da extração do efeito e informações completas sobre a dosagem, consulte o
apêndice .00.250.50.7511.251.51.752+Carvallo85%0.15 [0.02-1.28]36mg1/323/14CT2Improvement, RR [CI]Dose (4d)TreatmentControlMahmud (DB RCT)86%0.14 [0.01-2.75]12mg0/1833/183CT2Cadegiani78%0.22 [0.01-4.48]42mg0/1102/137CT2Ravikirti (DB RCT)89%0.11 [0.01-2.05]24mg0/554/57López-Me.. (DB RCT)67%0.33 [0.01-8.11]84mg0/2001/198Loue (QR)70%0.30 [0.04-2.20]14mg1/105/15Vallejos (DB RCT)-33%1.33 [0.30-5.72]24mg4/2503/251Reis (DB RCT)12%0.88 [0.49-1.55]84mg21/67924/679Mayer55%0.45 [0.32-0.63]151mg3,266 (n)17,966 (n)Borody92%0.08 [0.01-0.79]96mg0/6006/600CT2 SC3Abbas (DB RCT)-4%1.04 [0.07-16.4]84mg1/991/103de Jesús Ascenci..15%0.85 [0.68-1.06]12mg101/7,898303/20,150CT2Tau2 = 0.13, I2 = 47.2%, p = 0.0067Early treatment43%0.57 [0.38-0.86]129/13,382355/40,35343% improvementGorial71%0.29 [0.01-5.76]14mg0/162/71Improvement, RR [CI]Dose (4d)TreatmentControlKhan87%0.13 [0.02-1.00]12mg1/1159/133Soto-Becerra17%0.83 [0.71-0.97]14mg92/2031,438/2,630Rajter (PSM)46%0.54 [0.27-0.99]14mg13/9824/98Hashim (SB RCT)92%0.08 [0.00-1.44]28mg0/596/70CT2Budhiraja99%0.01 [0.00-0.15]n/a0/34103/942Okumuş (DB RCT)33%0.67 [0.27-1.64]56mg6/309/30Shahbazn.. (DB RCT)-197%2.97 [0.13-70.5]14mg1/350/34Lima-Morales78%0.22 [0.12-0.41]12mg15/48152/287CT2Beltran .. (DB RCT)14%0.86 [0.29-2.56]12mg5/366/37Ahsan50%0.50 [0.28-0.90]21mg17/11017/55CT2Abd-Elsalam (RCT)25%0.75 [0.17-3.06]36mg3/824/82Hazan86%0.14 [0.01-2.15]24mg0/24syntheticCT2 SC3Elavarasi20%0.80 [0.61-1.06]n/a48/283311/1,475Rezk80%0.20 [0.01-4.13]72mg0/1602/160Lim (RCT)69%0.31 [0.09-1.11]112mg3/24110/249Ozer75%0.25 [0.06-1.13]28mg2/608/60Ferreira-5%1.05 [0.32-3.43]n/a3/2111/81Jamir (ICU)-53%1.53 [0.88-2.67]n/a32/7669/190ICU patientsBaguma97%0.03 [0.00-11.7]n/a7 (n)474 (n)Mustafa64%0.36 [0.12-1.14]varies3/7342/371Shimizu100%0.00 [0.00-0.01]14mg0/398/49Zubair-9%1.09 [0.33-3.64]12mg5/905/98Thairu (PSM)88%0.12 [0.01-2.14]56mg0/214/26Efimenko (PSM)69%0.31 [0.20-0.48]n/a1,072 (n)40,536 (n)self-censored, see notes OT1Soto-41%1.41 [1.16-1.76]n/a280/484374/934Ravikirti3%0.97 [0.74-1.24]varies53/171254/794George (RCT)30%0.70 [0.25-1.93]24mg5/358/39Naggie (DB RCT)-195%2.95 [0.12-72.2]84mg1/8170/774Tau2 = 0.33, I2 = 83.8%, p < 0.0001Late treatment47%0.53 [0.39-0.73]588/4,9732,776/50,77947% improvementBernigaud99%0.01 [0.00-0.10]84mg0/69150/3,062Improvement, RR [CI]Dose (1m)TreatmentControlTanioka (ECO.)88%0.12 [0.03-0.46]14mgecologicalKerr (PSM)70%0.30 [0.19-0.46]56mg25/3,03479/3,034Tau2 = 1.39, I2 = 76.5%, p = 0.005Prophylaxis90%0.10 [0.02-0.50]25/3,103229/6,09690% improvementAll studies52%0.48 [0.37-0.62]742/21,4583,360/97,22852% improvementAll 44 ivermectin COVID-19 mortality resultsivmmeta.com Jun 2022Tau2 = 0.34, I2 = 83.0%, p < 0.00011 OT: ivermectin vs. other treatment3 SC: study uses synthetic control arm2 CT: study uses combined treatmentFavors ivermectinFavors control
Figura 8. Meta-análise de efeitos aleatórios para mortalidade.00.250.50.7511.251.51.752+Cadegiani94%0.06 [0.00-0.99]42mg0/1109/137CT1Improvement, RR [CI]Dose (4d)TreatmentControlRavikirti (DB RCT)79%0.21 [0.03-1.72]24mg1/555/57Krolewiecki (RCT)-152%2.52 [0.11-58.1]168mg1/270/14Vallejos (DB RCT)-33%1.33 [0.30-5.72]24mg4/2503/251Reis (DB RCT)23%0.77 [0.43-1.36]84mg19/67925/679de Jesús Ascenci..9%0.91 [0.70-1.18]12mg77/7,898216/20,150CT1Tau2 = 0.05, I2 = 20.8%, p = 0.32Early treatment18%0.82 [0.55-1.21]102/9,019258/21,28818% improvementRajter (PSM)64%0.36 [0.12-1.10]14mg4/9811/98Improvement, RR [CI]Dose (4d)TreatmentControlCamprubí40%0.60 [0.18-2.01]14mg3/135/13Shahbazn.. (DB RCT)-94%1.94 [0.18-20.4]14mg2/351/34Lima-Morales52%0.48 [0.20-1.18]12mg8/43411/287CT1Pott-Junior (RCT)85%0.15 [0.01-1.93]14mg1/271/4censored, see notesAbd-Elsalam (RCT)0%1.00 [0.21-4.81]36mg3/823/82Lim (RCT)59%0.41 [0.13-1.30]112mg4/24110/249Ozer13%0.87 [0.11-5.58]28mg3/602/60Shimizu48%0.52 [0.29-0.93]14mg39 (n)49 (n)Tau2 = 0.00, I2 = 0.0%, p = 0.00048Late treatment48%0.52 [0.36-0.75]28/1,02944/87648% improvementAll studies31%0.69 [0.54-0.89]130/10,048302/22,16431% improvementAll 15 ivermectin COVID-19 mechanical ventilation resultsivmmeta.com Jun 2022Tau2 = 0.02, I2 = 9.5%, p = 0.00361 CT: study uses combined treatmentFavors ivermectinFavors control
Figura 9. Metanálise de efeitos aleatórios para ventilação mecânica.00.250.50.7511.251.51.752+Ravikirti (DB RCT)14%0.86 [0.28-2.67]24mg5/556/57Improvement, RR [CI]Dose (4d)TreatmentControlMayer66%0.34 [0.22-0.51]151mg3,266 (n)17,966 (n)Tau2 = 0.24, I2 = 56.4%, p = 0.081Early treatment53%0.47 [0.20-1.10]5/3,3216/18,02353% improvementKhan89%0.11 [0.01-0.80]12mg1/11511/133Improvement, RR [CI]Dose (4d)TreatmentControlCamprubí33%0.67 [0.13-3.35]14mg2/133/13Pott-Junior (RCT)85%0.15 [0.01-1.93]14mg1/271/4censored, see notesLim (RCT)22%0.78 [0.27-2.20]112mg6/2418/249Ozer49%0.51 [0.09-2.50]28mg6/603/60Shimizu43%0.57 [0.32-1.02]14mg39 (n)49 (n)Tau2 = 0.00, I2 = 0.0%, p = 0.0054Late treatment46%0.54 [0.35-0.83]16/49526/50846% improvementAll studies54%0.46 [0.33-0.64]21/3,81632/18,53154% improvementAll 8 ivermectin COVID-19 ICU resultsivmmeta.com Jun 2022Tau2 = 0.02, I2 = 8.4%, p < 0.0001Favors ivermectinFavors control
Figura 10. Meta-análise de efeitos aleatórios para admissão na UTI.00.250.50.7511.251.51.752+Chowdhury (RCT)81%0.19 [0.01-3.96]14mghosp.0/602/56OT1 CT2Improvement, RR [CI]Dose (4d)TreatmentControlSzente Fonseca-14%1.14 [0.75-1.66]24mghosp.340 (n)377 (n)Cadegiani98%0.02 [0.00-0.33]42mghosp.0/11027/137CT2Biber (DB RCT)70%0.30 [0.03-2.76]36mghosp.1/473/42Merino (QR)74%0.26 [0.11-0.57]24mghosp.population-based cohortcensored, see notes CS4Vallejos (DB RCT)33%0.67 [0.34-1.28]24mghosp.14/25021/251Reis (DB RCT)17%0.83 [0.63-1.10]84mghosp.79/67995/679Buonfrate (DB RCT)-211%3.11 [0.13-73.3]336mghosp.1/280/31Borody93%0.07 [0.04-0.13]96mghosp.5/60070/600CT2 SC3de Jesús Ascenci..48%0.52 [0.48-0.58]12mghosp.485/7,8982,360/20,150CT2Tau2 = 0.39, I2 = 87.4%, p = 0.00069Early treatment59%0.41 [0.25-0.69]585/10,0122,578/22,32359% improvementGorial42%0.58 [0.45-0.75]14mghosp. time16 (n)71 (n)Improvement, RR [CI]Dose (4d)TreatmentControlKhan40%0.60 [0.44-0.81]12mghosp. time115 (n)133 (n)Spoorthi16%0.84 [0.74-0.96]n/ahosp. time50 (n)50 (n)CT2Shahbazn.. (DB RCT)15%0.85 [0.74-0.97]14mghosp. time35 (n)34 (n)Lima-Morales67%0.33 [0.22-0.47]12mghosp.44/48189/287CT2Beltran .. (DB RCT)-20%1.20 [0.77-1.87]12mghosp. time36 (n)37 (n)Abd-Elsalam (RCT)20%0.80 [0.63-1.03]36mghosp. time82 (n)82 (n)Hazan93%0.07 [0.00-1.02]24mghosp.0/24syntheticCT2 SC3Lim (RCT)-5%1.05 [0.94-1.19]112mghosp. time241 (n)249 (n)Ozer-9%1.09 [0.99-1.22]28mghosp. time60 (n)60 (n)Zubair-8%1.08 [0.91-1.29]12mghosp. time90 (n)98 (n)Naggie (DB RCT)-5%1.05 [0.43-2.58]84mghosp.10/8179/774Tau2 = 0.06, I2 = 87.3%, p = 0.012Late treatment19%0.81 [0.68-0.95]54/2,04798/1,87519% improvementMorgenstern (PSM)80%0.20 [0.01-4.15]56mghosp.0/2712/271Improvement, RR [CI]Dose (1m)TreatmentControlKerr (PSM)67%0.33 [0.23-0.46]56mghosp.44/3,03499/3,034Tau2 = 0.00, I2 = 0.0%, p < 0.0001Prophylaxis67%0.33 [0.23-0.46]44/3,305101/3,30567% improvementAll studies37%0.63 [0.52-0.77]683/15,3642,777/27,50337% improvementAll 24 ivermectin COVID-19 hospitalization resultsivmmeta.com Jun 2022Tau2 = 0.16, I2 = 92.3%, p < 0.00011 OT: ivermectin vs. other treatment3 SC: study uses synthetic control arm2 CT: study uses combined treatment4 CS: preprint censored, see detailsFavors ivermectinFavors control
Figura 11. Meta-análise de efeitos aleatórios para hospitalização.00.250.50.7511.251.51.752+Chowdhury (RCT)46%0.54 [0.40-0.73]14mgno recov.27/6047/56OT1 CT2Improvement, RR [CI]Dose (4d)TreatmentControlEspitia-Hernandez70%0.30 [0.16-0.55]12mgrecov. time28 (n)7 (n)CT2Mahmud (DB RCT)94%0.06 [0.04-0.09]12mgno recov.72/183100/180CT2Ghauri92%0.08 [0.01-0.88]48mgno recov.0/377/53Babalola (DB RCT)41%0.59 [0.33-1.05]24mg∆Spo238 (n)18 (n)OT1Ravikirti (DB RCT)89%0.11 [0.01-2.05]24mgno disch.0/554/57Mohan (DB RCT)62%0.38 [0.08-1.75]28mgno recov.2/406/45López-Me.. (DB RCT)15%0.85 [0.56-1.25]84mgno recov.36/20042/198Roy6%0.94 [0.52-1.93]n/arecov. time14 (n)15 (n)CT2Chahla (CLUS. RCT)87%0.13 [0.03-0.54]24mgno disch.2/11020/144Faisal (RCT)68%0.32 [0.14-0.72]48mgno recov.6/5019/50Aref (RCT)63%0.37 [0.22-0.61]n/arecov. time57 (n)57 (n)Abbas (DB RCT)36%0.64 [0.43-0.96]84mgno recov.26/9942/103Manomai.. (DB RCT)43%0.57 [0.20-1.46]48mgno recov.3/366/36Tau2 = 0.72, I2 = 89.3%, p = 0.00013Early treatment63%0.37 [0.22-0.61]174/1,007293/1,01963% improvementGorial71%0.29 [0.01-5.76]14mgno recov.0/162/71Improvement, RR [CI]Dose (4d)TreatmentControlKishoria (RCT)-8%1.08 [0.57-2.02]12mgno disch.11/197/13Podder (RCT)16%0.84 [0.55-1.12]14mgrecov. time32 (n)30 (n)Khan87%0.13 [0.02-1.00]12mgno recov.1/1159/133Chachar (RCT)10%0.90 [0.44-1.83]36mgno recov.9/2510/25Hashim (SB RCT)41%0.59 [0.46-0.77]28mgrecov. time70 (n)70 (n)CT2Spoorthi21%0.79 [0.64-0.98]n/arecov. time50 (n)50 (n)CT2Shahbazn.. (DB RCT)32%0.68 [0.47-1.00]14mgrecov. time35 (n)34 (n)Lima-Morales59%0.41 [0.30-0.55]12mgno recov.75/481118/287CT2Beltran .. (DB RCT)-37%1.37 [0.33-5.70]12mgno disch.4/363/37Rezk33%0.67 [0.35-1.27]72mgno recov.14/14520/138Lim (RCT)-2%1.02 [0.85-1.23]112mgno recov.116/241116/247Thairu (PSM)55%0.45 [0.28-0.73]56mgno disch.61 (n)26 (n)George (RCT)19%0.81 [0.52-1.27]24mgrecov. time35 (n)39 (n)Naggie (DB RCT)7%0.93 [0.85-1.04]84mgno recov.817 (n)774 (n)Tau2 = 0.08, I2 = 76.4%, p = 0.00094Late treatment28%0.72 [0.60-0.88]230/2,178285/1,97428% improvementAll studies46%0.54 [0.43-0.69]404/3,185578/2,99346% improvementAll 29 ivermectin COVID-19 recovery resultsivmmeta.com Jun 2022Tau2 = 0.28, I2 = 88.9%, p < 0.00011 OT: ivermectin vs. other treatment2 CT: study uses combined treatmentFavors ivermectinFavors control
Figura 12. Meta-análise de efeitos aleatórios apenas para resultados de recuperação.00.250.50.7511.251.51.752+Shouman (RCT)91%0.09 [0.03-0.23]36mgsymp. case15/20359/101Improvement, RR [CI]Dose (1m)TreatmentControlCarvallo96%0.04 [0.00-0.63]14mgcases0/13111/98see notes CT2Behera54%0.46 [0.29-0.71]42mgcases41/117145/255Carvallo100%0.00 [0.00-0.02]48mgcases0/788237/407see notes CT2Hellwig (ECO.)78%0.22 [0.06-0.76]14mgcasesecologicalBernigaud55%0.45 [0.22-0.91]84mgcases7/69692/3,062Alam91%0.09 [0.04-0.25]12mgcases4/5844/60IVERCOR PREP73%0.27 [0.15-0.48]48mgcases13/38961/486MD3Chahla (RCT)84%0.16 [0.04-0.46]48mgcases4/11725/117CT2Behera83%0.17 [0.12-0.23]42mgcases45/2,199133/1,147Seet (CLUS. RCT)50%0.50 [0.33-0.76]12mgsymp. case32/61764/619OT1Morgenstern (PSM)74%0.26 [0.10-0.71]56mgcases5/27118/271Mondal88%0.12 [0.01-0.55]n/asymp. case128 (n)1,342 (n)Samajdar80%0.20 [0.11-0.38]n/acases12/16429/81Kerr (PSM)44%0.56 [0.53-0.58]56mgcasespopulation-based cohortTau2 = 0.44, I2 = 91.2%, p < 0.0001Prophylaxis78%0.22 [0.14-0.33]178/5,2511,518/8,04678% improvementAll studies78%0.22 [0.14-0.33]178/5,2511,518/8,04678% improvementAll 15 ivermectin COVID-19 case resultsivmmeta.com Jun 2022Tau2 = 0.44, I2 = 91.2%, p < 0.00011 OT: ivermectin vs. other treatment3 MD: minimal detail available currently2 CT: study uses combined treatmentFavors ivermectinFavors control
Figura 13. Meta-análise de efeitos aleatórios para resultados de casos de COVID-19.00.250.50.7511.251.51.752+Chowdhury (RCT)81%0.19 [0.01-3.96]14mgviral+0/602/56OT1 CT2Improvement, RR [CI]Dose (4d)TreatmentControlEspitia-Hernandez97%0.03 [0.01-0.10]12mgviral+0/287/7CT2Mahmud (DB RCT)39%0.61 [0.44-0.83]12mgviral+14/18336/180CT2Ahmed (DB RCT)76%0.24 [0.07-0.91]48mgviral+11/2220/23Chaccour (DB RCT)95%0.05 [0.01-0.50]28mgviral load12 (n)12 (n)Babalola (DB RCT)64%0.36 [0.10-1.27]24mgviral+40 (n)20 (n)OT1Ravikirti (DB RCT)-12%1.12 [0.89-1.40]24mgviral+42/5539/57Bukhari (RCT)82%0.18 [0.07-0.46]12mgviral+4/4125/45Mohan (DB RCT)24%0.76 [0.53-1.09]28mgviral+21/4031/45Biber (DB RCT)45%0.55 [0.27-0.97]36mgviral+13/4721/42Elalfy87%0.13 [0.06-0.27]36mgviral+7/6244/51CT2Mourya89%0.11 [0.05-0.25]48mgviral+5/5047/50Aref (RCT)79%0.21 [0.07-0.71]n/aviral+3/5714/57Krolewiecki (RCT)66%0.34 [0.10-1.16]168mgdecay rate20 (n)14 (n)Vallejos (DB RCT)-5%1.05 [0.88-1.21]24mgviral+137/250131/251Reis (DB RCT)0%1.00 [0.68-1.47]84mgviral+106/142123/165Buonfrate (DB RCT)20%0.80 [0.36-1.76]336mgviral load28 (n)29 (n)Manomai.. (DB RCT)5%0.95 [0.62-1.45]48mgviral+19/3620/36Rocha (DB RCT)2%0.98 [0.89-1.08]36mgviral load30 (n)26 (n)Tau2 = 0.16, I2 = 86.6%, p < 0.0001Early treatment47%0.53 [0.41-0.67]382/1,203560/1,16647% improvementKishoria (RCT)-8%1.08 [0.57-2.02]12mgviral+11/197/13Improvement, RR [CI]Dose (4d)TreatmentControlKhan73%0.27 [0.12-0.58]12mgviral time115 (n)133 (n)Camprubí-25%1.25 [0.43-3.63]14mgviral+5/134/13Okumuş (DB RCT)80%0.20 [0.05-0.81]56mgviral+2/165/8Pott-Junior (RCT)1%0.99 [0.04-26.3]14mgviral+27 (n)3 (n)censored, see notesRezk27%0.73 [0.57-0.93]72mgviral time160 (n)160 (n)Thairu (PSM)95%0.05 [0.00-0.85]56mgviral+0/2110/26Tau2 = 0.24, I2 = 61.4%, p = 0.052Late treatment40%0.60 [0.36-1.01]18/37126/35640% improvementAll studies45%0.55 [0.44-0.68]400/1,574586/1,52245% improvementAll 26 ivermectin COVID-19 viral clearance resultsivmmeta.com Jun 2022Tau2 = 0.15, I2 = 84.0%, p < 0.00011 OT: ivermectin vs. other treatment2 CT: study uses combined treatmentFavors ivermectinFavors control
Figura 14. Meta-análise de efeitos aleatórios para depuração viral.00.250.50.7511.251.51.752+Chowdhury (RCT)81%0.19 [0.01-3.96]14mghosp.0/602/56OT1 CT2Improvement, RR [CI]Dose (4d)TreatmentControlEspitia-Hernandez70%0.30 [0.16-0.55]12mgrecov. time28 (n)7 (n)CT2Carvallo85%0.15 [0.02-1.28]36mgdeath1/323/14CT2Mahmud (DB RCT)86%0.14 [0.01-2.75]12mgdeath0/1833/183CT2Szente Fonseca-14%1.14 [0.75-1.66]24mghosp.340 (n)377 (n)Cadegiani78%0.22 [0.01-4.48]42mgdeath0/1102/137CT2Ahmed (DB RCT)85%0.15 [0.01-2.70]48mgsymptoms0/173/19Chaccour (DB RCT)96%0.04 [0.00-1.01]28mgsymptoms12 (n)12 (n)Ghauri92%0.08 [0.01-0.88]48mgno recov.0/377/53Babalola (DB RCT)64%0.36 [0.10-1.27]24mgviral+40 (n)20 (n)OT1Ravikirti (DB RCT)89%0.11 [0.01-2.05]24mgdeath0/554/57Mohan (DB RCT)62%0.38 [0.08-1.75]28mgno recov.2/406/45Elalfy87%0.13 [0.06-0.27]36mgviral+7/6244/51CT2López-Me.. (DB RCT)67%0.33 [0.01-8.11]84mgdeath0/2001/198Mourya89%0.11 [0.05-0.25]48mgviral+5/5047/50Loue (QR)70%0.30 [0.04-2.20]14mgdeath1/105/15Faisal (RCT)68%0.32 [0.14-0.72]48mgno recov.6/5019/50Aref (RCT)63%0.37 [0.22-0.61]n/arecov. time57 (n)57 (n)Krolewiecki (RCT)-152%2.52 [0.11-58.1]168mgventilation1/270/14Vallejos (DB RCT)-33%1.33 [0.30-5.72]24mgdeath4/2503/251Reis (DB RCT)12%0.88 [0.49-1.55]84mgdeath21/67924/679Buonfrate (DB RCT)-211%3.11 [0.13-73.3]336mghosp.1/280/31Mayer55%0.45 [0.32-0.63]151mgdeath3,266 (n)17,966 (n)Abbas (DB RCT)-4%1.04 [0.07-16.4]84mgdeath1/991/103de Jesús Ascenci..59%0.41 [0.36-0.47]12mgdeath/hosp.7,898 (n)20,150 (n)CT2Tau2 = 0.17, I2 = 57.2%, p < 0.0001Early treatment62%0.38 [0.28-0.50]50/13,630174/40,59562% improvementKishoria (RCT)-8%1.08 [0.57-2.02]12mgno disch.11/197/13Improvement, RR [CI]Dose (4d)TreatmentControlPodder (RCT)16%0.84 [0.55-1.12]14mgrecov. time32 (n)30 (n)Chachar (RCT)10%0.90 [0.44-1.83]36mgno recov.9/2510/25Rajter (PSM)46%0.54 [0.27-0.99]14mgdeath13/9824/98Hashim (SB RCT)92%0.08 [0.00-1.44]28mgdeath0/596/70CT2Camprubí40%0.60 [0.18-2.01]14mgventilation3/135/13Spoorthi21%0.79 [0.64-0.98]n/arecov. time50 (n)50 (n)CT2Okumuş (DB RCT)33%0.67 [0.27-1.64]56mgdeath6/309/30Shahbazn.. (DB RCT)-197%2.97 [0.13-70.5]14mgdeath1/350/34Lima-Morales78%0.22 [0.12-0.41]12mgdeath15/48152/287CT2Beltran .. (DB RCT)14%0.86 [0.29-2.56]12mgdeath5/366/37Pott-Junior (RCT)85%0.15 [0.01-1.93]14mgventilation1/271/4censored, see notesAhsan50%0.50 [0.28-0.90]21mgdeath17/11017/55CT2Abd-Elsalam (RCT)25%0.75 [0.17-3.06]36mgdeath3/824/82Rezk80%0.20 [0.01-4.13]72mgdeath0/1602/160Lim (RCT)69%0.31 [0.09-1.11]112mgdeath3/24110/249Ozer75%0.25 [0.06-1.13]28mgdeath2/608/60Ferreira-5%1.05 [0.32-3.43]n/adeath3/2111/81Jamir (ICU)-53%1.53 [0.88-2.67]n/adeath32/7669/190ICU patientsMustafa64%0.36 [0.12-1.14]variesdeath3/7342/371Shimizu100%0.00 [0.00-0.01]14mgdeath0/398/49Zubair-9%1.09 [0.33-3.64]12mgdeath5/905/98Efimenko (PSM)69%0.31 [0.20-0.48]n/adeath1,072 (n)40,536 (n)self-censored, see notes OT1Soto-41%1.41 [1.16-1.76]n/adeath280/484374/934George (RCT)30%0.70 [0.25-1.93]24mgdeath5/358/39Tau2 = 0.39, I2 = 84.1%, p = 0.0017Late treatment41%0.59 [0.43-0.82]417/3,448678/43,59541% improvementShouman (RCT)91%0.09 [0.03-0.23]36mgsymp. case15/20359/101Improvement, RR [CI]Dose (1m)TreatmentControlBehera54%0.46 [0.29-0.71]42mgcases41/117145/255Carvallo100%0.00 [0.00-0.02]48mgcases0/788237/407see notes CT2Hellwig (ECO.)78%0.22 [0.06-0.76]14mgcasesecologicalBernigaud99%0.01 [0.00-0.10]84mgdeath0/69150/3,062Alam91%0.09 [0.04-0.25]12mgcases4/5844/60Chahla (RCT)95%0.05 [0.00-0.80]48mgm/s case0/11710/117CT2Behera83%0.17 [0.12-0.23]42mgcases45/2,199133/1,147Seet (CLUS. RCT)50%0.50 [0.33-0.76]12mgsymp. case32/61764/619OT1Morgenstern (PSM)80%0.20 [0.01-4.15]56mghosp.0/2712/271Mondal88%0.12 [0.01-0.55]n/asymp. case128 (n)1,342 (n)Samajdar80%0.20 [0.11-0.38]n/acases12/16429/81Kerr (PSM)70%0.30 [0.19-0.46]56mgdeath25/3,03479/3,034Tau2 = 0.50, I2 = 84.8%, p < 0.0001Prophylaxis83%0.17 [0.10-0.27]174/7,765952/10,49683% improvementAll studies63%0.37 [0.28-0.47]641/24,8431,804/94,68663% improvementAll 63 ivermectin COVID-19 peer reviewed trialsivmmeta.com Jun 2022Tau2 = 0.62, I2 = 89.7%, p < 0.0001Effect extraction pre-specified(most serious outcome, see appendix)1 OT: ivermectin vs. other treatment2 CT: study uses combined treatmentFavors ivermectinFavors control
Figura 15. Meta-análise de efeitos aleatórios para estudos revisados por pares.
[ Zeraatkar ] analisam 356 ensaios COVID-19, não encontrando evidências significativas de que estudos revisados por pares sejam mais confiáveis. Eles também mostram tempos de revisão extremamente lentos durante uma pandemia. Os autores recomendam o uso de evidências de pré-impressão, com verificações apropriadas para possíveis dados falsificados, o que fornece maior certeza muito mais cedo. A extração do efeito é pré-especificada, usando o resultado mais grave relatado, consulte o
apêndice para obter detalhes.
Ensaios controlados randomizados (RCTs)Os resultados restritos a Ensaios Controlados Randomizados (RCTs) são mostrados na Figura
16 ,
17 ,
18 ,
19 e
20 e na
Tabela 3 . Os
dados suplementares contêm os resultados do RCT após as exclusões.ECRs ajudam a tornar os grupos de estudo mais semelhantes, no entanto, eles estão sujeitos a muitos vieses, incluindo viés de idade, viés de atraso no tratamento, viés de gravidade da doença, viés de regulação, viés de recrutamento, viés de desenho de estudo, viés de tempo de acompanhamento, viés de relatório seletivo, viés de fraude , viés de agenda oculta, viés de interesse adquirido, viés de publicação e viés de atraso de publicação
[ Jadad ] , todos observados com ECRs COVID-19.Os ECRs têm um viés contra encontrar um efeito para intervenções amplamente disponíveis – os pacientes que acreditam que precisam da intervenção têm maior probabilidade de recusar a participação e fazer a intervenção. Isso é ilustrado com o exemplo extremo de um RCT que não mostra diferenças significativas para o uso de um pára-quedas ao pular de um avião
[ Yeh ]. ECRs para ivermectina são mais propensos a inscrever participantes de baixo risco que não precisam de tratamento para se recuperar, tornando os resultados menos aplicáveis à prática clínica. Esse viés provavelmente será maior para tratamentos amplamente conhecidos, como a ivermectina. O viés também pode ser maior em locais onde a ivermectina é mais facilmente obtida. Observe que esse viés não se aplica ao teste farmacêutico típico de um novo medicamento que de outra forma não está disponível.As evidências mostram que os ensaios não-RCT também podem fornecer resultados confiáveis.
[ Concato ] descobriram que estudos observacionais bem desenhados não superestimam sistematicamente a magnitude dos efeitos do tratamento em comparação com os ECRs.
[ Anglemyer ] resumiu revisões comparando RCTs a estudos observacionais e encontrou pouca evidência para diferenças significativas nas estimativas de efeito.
[ Lee ]mostra que apenas 14% das diretrizes da Infectious Diseases Society of America foram baseadas em ECRs. A avaliação dos estudos depende de uma compreensão do estudo e de possíveis vieses. As limitações em um ECR podem superar os benefícios, por exemplo, dosagens excessivas, atrasos excessivos no tratamento ou viés de pesquisa na Internet podem ter um efeito maior nos resultados. Questões éticas também podem impedir a execução de ECRs para tratamentos eficazes conhecidos. Para mais informações sobre problemas com RCTs, veja
[ Deaton , Nichol ] .Em resumo, precisamos avaliar cada ensaio em seus próprios méritos. ECRs para um determinado medicamento e doença podem ser mais confiáveis, mas também podem ser menos confiáveis. Por exemplo, considere ensaios para um medicamento sem patente, ensaios de conflito de interesse muito alto podem ser mais prováveis de serem ensaios clínicos randomizados (e mais prováveis de serem ensaios grandes que dominam metanálises).
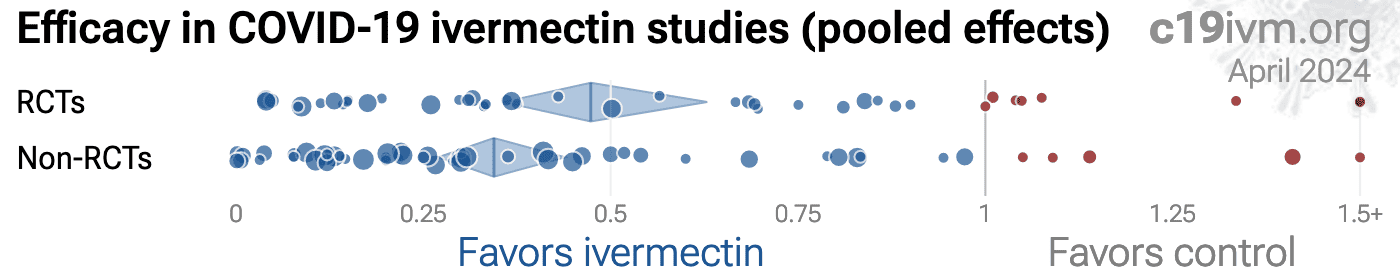

Figura 16. Ensaios controlados randomizados. A distribuição dos resultados dos ECRs é semelhante à distribuição de todos os outros estudos.00.250.50.7511.251.51.752+Chowdhury (RCT)81%0.19 [0.01-3.96]14mghosp.0/602/56OT1 CT2Improvement, RR [CI]Dose (4d)TreatmentControlMahmud (DB RCT)86%0.14 [0.01-2.75]12mgdeath0/1833/183CT2Ahmed (DB RCT)85%0.15 [0.01-2.70]48mgsymptoms0/173/19Chaccour (DB RCT)96%0.04 [0.00-1.01]28mgsymptoms12 (n)12 (n)Babalola (DB RCT)64%0.36 [0.10-1.27]24mgviral+40 (n)20 (n)OT1Ravikirti (DB RCT)89%0.11 [0.01-2.05]24mgdeath0/554/57Bukhari (RCT)82%0.18 [0.07-0.46]12mgviral+4/4125/45Mohan (DB RCT)62%0.38 [0.08-1.75]28mgno recov.2/406/45Biber (DB RCT)70%0.30 [0.03-2.76]36mghosp.1/473/42López-Me.. (DB RCT)67%0.33 [0.01-8.11]84mgdeath0/2001/198Chahla (CLUS. RCT)87%0.13 [0.03-0.54]24mgno disch.2/11020/144Faisal (RCT)68%0.32 [0.14-0.72]48mgno recov.6/5019/50Aref (RCT)63%0.37 [0.22-0.61]n/arecov. time57 (n)57 (n)Krolewiecki (RCT)-152%2.52 [0.11-58.1]168mgventilation1/270/14Vallejos (DB RCT)-33%1.33 [0.30-5.72]24mgdeath4/2503/251Reis (DB RCT)12%0.88 [0.49-1.55]84mgdeath21/67924/679Buonfrate (DB RCT)-211%3.11 [0.13-73.3]336mghosp.1/280/31Abbas (DB RCT)-4%1.04 [0.07-16.4]84mgdeath1/991/103Manomai.. (DB RCT)43%0.57 [0.20-1.46]48mgno recov.3/366/36Rocha (DB RCT)-187%2.87 [0.12-67.5]36mgmisc.1/300/26Tau2 = 0.12, I2 = 22.3%, p < 0.0001Early treatment59%0.41 [0.29-0.59]47/2,061120/2,06859% improvementKishoria (RCT)-8%1.08 [0.57-2.02]12mgno disch.11/197/13Improvement, RR [CI]Dose (4d)TreatmentControlPodder (RCT)16%0.84 [0.55-1.12]14mgrecov. time32 (n)30 (n)Chachar (RCT)10%0.90 [0.44-1.83]36mgno recov.9/2510/25Hashim (SB RCT)92%0.08 [0.00-1.44]28mgdeath0/596/70CT2Okumuş (DB RCT)33%0.67 [0.27-1.64]56mgdeath6/309/30Shahbazn.. (DB RCT)-197%2.97 [0.13-70.5]14mgdeath1/350/34Beltran .. (DB RCT)14%0.86 [0.29-2.56]12mgdeath5/366/37Pott-Junior (RCT)85%0.15 [0.01-1.93]14mgventilation1/271/4censored, see notesHuvemek (DB RCT)32%0.68 [0.38-1.23]84mgno improv.13/5019/50Abd-Elsalam (RCT)25%0.75 [0.17-3.06]36mgdeath3/824/82Lim (RCT)69%0.31 [0.09-1.11]112mgdeath3/24110/249George (RCT)30%0.70 [0.25-1.93]24mgdeath5/358/39Naggie (DB RCT)-195%2.95 [0.12-72.2]84mgdeath1/8170/774Tau2 = 0.00, I2 = 0.0%, p = 0.05Late treatment23%0.77 [0.60-1.00]58/1,48880/1,43723% improvementShouman (RCT)91%0.09 [0.03-0.23]36mgsymp. case15/20359/101Improvement, RR [CI]Dose (1m)TreatmentControlChahla (RCT)95%0.05 [0.00-0.80]48mgm/s case0/11710/117CT2Seet (CLUS. RCT)50%0.50 [0.33-0.76]12mgsymp. case32/61764/619OT1Tau2 = 1.43, I2 = 93.0%, p = 0.02Prophylaxis84%0.16 [0.04-0.75]47/937133/83784% improvementAll studies54%0.46 [0.34-0.64]152/4,486333/4,34254% improvementAll 36 ivermectin COVID-19 Randomized Controlled Trialsivmmeta.com Jun 2022Tau2 = 0.41, I2 = 61.9%, p < 0.0001Effect extraction pre-specified(most serious outcome, see appendix)1 OT: ivermectin vs. other treatment2 CT: study uses combined treatmentFavors ivermectinFavors control
Figura 17. Meta-análise de efeitos aleatórios apenas para Ensaios Controlados Randomizados. A extração do efeito é pré-especificada, usando o resultado mais grave relatado, consulte o
apêndice para obter detalhes.


Figura 18. ECRs excluindo tratamento tardio.00.250.50.7511.251.51.752+Mahmud (DB RCT)86%0.14 [0.01-2.75]12mg0/1833/183CT1Improvement, RR [CI]Dose (4d)TreatmentControlRavikirti (DB RCT)89%0.11 [0.01-2.05]24mg0/554/57López-Me.. (DB RCT)67%0.33 [0.01-8.11]84mg0/2001/198Vallejos (DB RCT)-33%1.33 [0.30-5.72]24mg4/2503/251Reis (DB RCT)12%0.88 [0.49-1.55]84mg21/67924/679Abbas (DB RCT)-4%1.04 [0.07-16.4]84mg1/991/103Tau2 = 0.00, I2 = 0.0%, p = 0.41Early treatment19%0.81 [0.49-1.34]26/1,46636/1,47119% improvementHashim (SB RCT)92%0.08 [0.00-1.44]28mg0/596/70CT1Improvement, RR [CI]Dose (4d)TreatmentControlOkumuş (DB RCT)33%0.67 [0.27-1.64]56mg6/309/30Shahbazn.. (DB RCT)-197%2.97 [0.13-70.5]14mg1/350/34Beltran .. (DB RCT)14%0.86 [0.29-2.56]12mg5/366/37Abd-Elsalam (RCT)25%0.75 [0.17-3.06]36mg3/824/82Lim (RCT)69%0.31 [0.09-1.11]112mg3/24110/249George (RCT)30%0.70 [0.25-1.93]24mg5/358/39Naggie (DB RCT)-195%2.95 [0.12-72.2]84mg1/8170/774Tau2 = 0.00, I2 = 0.0%, p = 0.073Late treatment35%0.65 [0.40-1.04]24/1,33543/1,31535% improvementAll studies28%0.72 [0.51-1.02]50/2,80179/2,78628% improvementAll 14 ivermectin COVID-19 RCT mortality resultsivmmeta.com Jun 2022Tau2 = 0.00, I2 = 0.0%, p = 0.0611 CT: study uses combined treatmentFavors ivermectinFavors control
Figura 19. Meta-análise de efeitos aleatórios para resultados de mortalidade por ECR.00.250.50.7511.251.51.752+Chowdhury (RCT)81%0.19 [0.01-3.96]14mgviral+0/602/56OT1 CT2Improvement, RR [CI]Dose (4d)TreatmentControlMahmud (DB RCT)39%0.61 [0.44-0.83]12mgviral+14/18336/180CT2Ahmed (DB RCT)76%0.24 [0.07-0.91]48mgviral+11/2220/23Chaccour (DB RCT)95%0.05 [0.01-0.50]28mgviral load12 (n)12 (n)Babalola (DB RCT)64%0.36 [0.10-1.27]24mgviral+40 (n)20 (n)OT1Ravikirti (DB RCT)-12%1.12 [0.89-1.40]24mgviral+42/5539/57Bukhari (RCT)82%0.18 [0.07-0.46]12mgviral+4/4125/45Mohan (DB RCT)24%0.76 [0.53-1.09]28mgviral+21/4031/45Biber (DB RCT)45%0.55 [0.27-0.97]36mgviral+13/4721/42Aref (RCT)79%0.21 [0.07-0.71]n/aviral+3/5714/57Krolewiecki (RCT)66%0.34 [0.10-1.16]168mgdecay rate20 (n)14 (n)Vallejos (DB RCT)-5%1.05 [0.88-1.21]24mgviral+137/250131/251Reis (DB RCT)0%1.00 [0.68-1.47]84mgviral+106/142123/165Buonfrate (DB RCT)20%0.80 [0.36-1.76]336mgviral load28 (n)29 (n)Manomai.. (DB RCT)5%0.95 [0.62-1.45]48mgviral+19/3620/36Rocha (DB RCT)2%0.98 [0.89-1.08]36mgviral load30 (n)26 (n)Tau2 = 0.05, I2 = 71.0%, p = 0.0032Early treatment23%0.77 [0.65-0.92]370/1,063462/1,05823% improvementKishoria (RCT)-8%1.08 [0.57-2.02]12mgviral+11/197/13Improvement, RR [CI]Dose (4d)TreatmentControlOkumuş (DB RCT)80%0.20 [0.05-0.81]56mgviral+2/165/8Pott-Junior (RCT)1%0.99 [0.04-26.3]14mgviral+27 (n)3 (n)censored, see notesTau2 = 0.38, I2 = 57.3%, p = 0.44Late treatment31%0.69 [0.28-1.74]13/6212/2431% improvementAll studies23%0.77 [0.65-0.91]383/1,125474/1,08223% improvementAll 19 ivermectin COVID-19 RCT viral clearance resultsivmmeta.com Jun 2022Tau2 = 0.05, I2 = 68.2%, p = 0.00241 OT: ivermectin vs. other treatment2 CT: study uses combined treatmentFavors ivermectinFavors control
Figura 20. Meta-análise de efeitos aleatórios para resultados de depuração viral RCT.
| Tempo de tratamento | Número de estudos relatando efeitos positivos | Número total de estudos | Porcentagem de estudos relatando efeitos positivos | Probabilidade de uma porcentagem igual ou maior de resultados positivos de um tratamento ineficaz | Resultados de meta-análise de efeitos aleatórios |
| Ensaios controlados randomizados | 28 | 36 | 77,8% | 1 em 2 mil | 54% de melhoria RR 0,46 [0,34-0,64] p < 0,0001 |
| Ensaios controlados randomizados (excluindo tratamento tardio) | 18 | 23 | 78,3% | 1 em 188 | 66% de melhora RR 0,34 [0,22-0,53] p < 0,0001 |
Tabela 3. Resumo dos resultados do ECR.ExclusõesPara evitar viés na seleção de estudos, analisamos todos os estudos não retratados. Aqui mostramos os resultados após a exclusão de estudos com questões críticas que provavelmente alteram os resultados, estudos não padronizados e estudos em que detalhes muito mínimos estão disponíveis atualmente. Nossa avaliação de viés é baseada na análise de cada estudo e na identificação de quando há uma chance significativa de que as limitações alterem substancialmente o resultado do estudo. Acreditamos que isso pode ser mais valioso do que abordagens baseadas em listas de verificação, como o Cochrane GRADE, que pode subestimar questões sérias não capturadas nas listas de verificação, enfatizar demais questões que provavelmente não alterarão os resultados em casos específicos (por exemplo, falta de cegamento para um resultado objetivo de mortalidade, ou certas especificidades de randomização com um tamanho de efeito muito grande), ou estar sujeito a
viés. No entanto, eles também podem ser de alta qualidade
[ Bryant ] .Uma equipe de pesquisadores analisou os dados em estudos com ivermectina e identificou vários estudos com preocupações. Estudos retratados não estão nesta análise. Todos os outros estudos que a equipe identificou são excluídos aqui. Para obter mais detalhes, consulte a
seção de resposta .A descrição detalhada dos problemas com
[ López-Medina ] pode ser encontrada na seção de
[ Soto-Becerra ]é uma análise de banco de dados que abrange qualquer pessoa com códigos ICD-10 COVID-19, que inclui pacientes PCR+ assintomáticos. Portanto, muitos pacientes no grupo de controle provavelmente são assintomáticos em relação ao SARS-CoV-2, mas no hospital por outro motivo. Para aqueles que tiveram COVID-19 sintomático, também é provável que haja confusão significativa por indicação. As curvas KM mostram que os grupos de tratamento estavam em condições mais graves, com mais do que o excesso de mortalidade total em 30 dias ocorrendo no dia 1. Todos os tratamentos são piores do que o grupo de controle em 30 dias, enquanto no último acompanhamento todos os tratamentos mostram menor mortalidade do que controle. O sistema de aprendizado de máquina usado também parece superparametrizado e provavelmente resultará em sobreajuste significativo e resultados imprecisos. Também não há um grupo controle real neste estudo – os pacientes que receberam os tratamentos após 48 horas foram colocados no grupo controle. Os autores também afirmam que os desfechos em 24 horas foram excluídos, porém as curvas KM mostram mortalidade significativa no dia 1 (somente para os grupos de tratamento). Várias violações de protocolo também foram relatadas neste estudo
[ Yim ] . Observe que este estudo fornece curvas de mortalidade em 30 dias e KM ponderada até o dia 43 para ivermectina, usamos os resultados do dia 43 de acordo com nosso protocolo.
[ IVERCOR PREP ] relata os resultados da profilaxia, no entanto, apenas detalhes muito mínimos estão atualmente disponíveis em uma reportagem.
[ Hellwig ] analisam países africanos e casos de COVID-19 em outubro de 2020 em função do uso profilático generalizado de ivermectina para infecções parasitárias.
[ Tanioka ] realizam uma análise semelhante para a mortalidade por COVID-19 em janeiro de 2021. Esses estudos foram excluídos porque não são ensaios clínicos.
[ Shahbaznejad ]teve apenas uma morte que ocorreu em um paciente que estava gravemente doente no momento da admissão e morreu nas primeiras 24 horas.
[ Galan ] realizam um ECR comparando a ivermectina e outros tratamentos com pacientes hospitalizados em estado grave em estágio muito avançado, não mostrando diferenças significativas entre os tratamentos. Os autores não conseguiram adicionar um braço de controle devido a questões éticas. A comparação de controle mais próxima que pudemos encontrar é
[ Baqui ], que mostra 43% de mortalidade hospitalar na região norte do Brasil onde o estudo foi realizado, a partir do qual podemos estimar a mortalidade com ivermectina neste estudo como 47% menor, RR 0,53. Além disso, o estudo é restrito a casos mais graves, portanto, a mortalidade esperada e, portanto, o benefício do tratamento podem ser maiores.
[ Kishoria ] restringem a inclusão a pacientes que não responderam ao tratamento padrão, não fornecem detalhes sobre o momento da alta e há diferenças não ajustadas muito grandes nos grupos, com mais do dobro de pacientes no grupo da ivermectina com idade > 40, e todos os pacientes com mais de 60 anos no grupo ivermectina.Resumindo, os estudos excluídos são os seguintes, e o gráfico de floresta resultante é mostrado na
Figura 21 . Os
dados complementares mostram resultados após restrições e exclusões.
[ Abbas ] , informações mínimas do paciente, três resultados diferentes para o resultado da recuperação, omissão seletiva do valor p de recuperação estatisticamente significativo e outras inconsistências.
[ Ahsan ] , resultados não ajustados sem detalhes do grupo.
[ Beltran Gonzalez ] , grandes inconsistências relatadas e os dados não estão mais disponíveis
[ Chamie ] , embora os autores afirmem que estão disponíveis e os compartilharam com um grupo antitratamento.
[ Borody ] , relatório preliminar com detalhes mínimos.
[ Buonfrate ] , diferenças significativas não ajustadas entre os grupos, com 3 vezes mais pacientes nos braços de ivermectina tendo a consulta inicial em um ambiente hospitalar, e o braço C tendo grandes diferenças no sexo basal, peso, tosse, pirexia e anosmia, dose excessiva para braço C.
[ Cadegiani ] , grupo controle obtido retrospectivamente de pacientes não tratados na mesma população.
[ Carvallo ] , preocupação com possíveis problemas de dados.
[ Carvallo (B) ] , preocupação com possíveis problemas de dados.
[ Carvallo (C) ] , detalhes mínimos dos grupos fornecidos.
[ de Jesús Ascencio-Montiel ] , resultados não ajustados com resultado alternativo resultados ajustados mostrando mudanças significativas com ajustes. Resultados excluídos: óbito, ventilação mecânica, internação, progressão.
[ Elavarasi ] , resultados não ajustados sem detalhes do grupo.
[ Ferreira ] , resultados não ajustados sem detalhes do grupo, provável confusão substancial não ajustada por indicação.
[ Hazan ] , o estudo usa um braço de controle sintético.
[ Hellwig ] , não um ensaio típico, análise de países africanos que usaram ou não a profilaxia de ivermectina para infecções parasitárias.
[ IVERCOR PREP ] , detalhes mínimos fornecidos.
[ Kishória ] , diferenças excessivas não ajustadas entre os grupos.
[ López-Medina ] , forte evidência de pacientes do grupo controle se automedicando, ivermectina amplamente utilizada na população da época, e a identidade do medicamento do estudo foi ocultada pelo uso do nome D11AX22.
[ Mustafa ] , resultados não ajustados sem detalhes do grupo.
[ Ravikirti ] , exclusão de pacientes em condições menos graves, preocupações com dados/análises.
[ Reis ] , múltiplas anomalias conforme análise detalhada.
[ Roy ] , sem resultados graves relatados e recuperação rápida nos grupos de tratamento e controle, há pouco espaço para um tratamento melhorar os resultados.
[ Samajdar ] , detalhes mínimos fornecidos, resultados não ajustados sem detalhes do grupo, os resultados podem ser significativamente afetados pelo viés da pesquisa.
[ Soto ] , confusão substancial não ajustada por indicação provável, confusão substancial por tempo possível devido a mudanças significativas no SOC e propensão ao tratamento próximo ao início da pandemia.
[ Soto-Becerra ] , provável confusão não ajustada substancial por indicação, inclui pacientes PCR + que podem ser assintomáticos para COVID-19, mas hospitalizados por outros motivos.
[ Szente Fonseca ] , o resultado provavelmente é afetado pela colinearidade entre os tratamentos no modelo.
[ Tanioka ] , não um ensaio típico, análise de países africanos que usaram ou não a profilaxia de ivermectina para infecções parasitárias.
[ Thairu ] , confusão significativa por tempo possível devido à separação de grupos em diferentes períodos de tempo.
[ Zubair ] , confusão substancial não ajustada por indicação provável, resultados não ajustados sem detalhes do grupo.00.250.50.7511.251.51.752+Chowdhury (RCT)81%0.19 [0.01-3.96]14mghosp.0/602/56OT1 CT2Improvement, RR [CI]Dose (4d)TreatmentControlEspitia-Hernandez70%0.30 [0.16-0.55]12mgrecov. time28 (n)7 (n)CT2Mahmud (DB RCT)86%0.14 [0.01-2.75]12mgdeath0/1833/183CT2Ahmed (DB RCT)85%0.15 [0.01-2.70]48mgsymptoms0/173/19Chaccour (DB RCT)96%0.04 [0.00-1.01]28mgsymptoms12 (n)12 (n)Ghauri92%0.08 [0.01-0.88]48mgno recov.0/377/53Babalola (DB RCT)64%0.36 [0.10-1.27]24mgviral+40 (n)20 (n)OT1Ravikirti (DB RCT)89%0.11 [0.01-2.05]24mgdeath0/554/57Bukhari (RCT)82%0.18 [0.07-0.46]12mgviral+4/4125/45Mohan (DB RCT)62%0.38 [0.08-1.75]28mgno recov.2/406/45Biber (DB RCT)70%0.30 [0.03-2.76]36mghosp.1/473/42Elalfy87%0.13 [0.06-0.27]36mgviral+7/6244/51CT2Chahla (CLUS. RCT)87%0.13 [0.03-0.54]24mgno disch.2/11020/144Mourya89%0.11 [0.05-0.25]48mgviral+5/5047/50Loue (QR)70%0.30 [0.04-2.20]14mgdeath1/105/15Merino (QR)74%0.26 [0.11-0.57]24mghosp.population-based cohortcensored, see notes CS3Faisal (RCT)68%0.32 [0.14-0.72]48mgno recov.6/5019/50Aref (RCT)63%0.37 [0.22-0.61]n/arecov. time57 (n)57 (n)Krolewiecki (RCT)-152%2.52 [0.11-58.1]168mgventilation1/270/14Vallejos (DB RCT)-33%1.33 [0.30-5.72]24mgdeath4/2503/251Mayer55%0.45 [0.32-0.63]151mgdeath3,266 (n)17,966 (n)de Jesús Ascenci..59%0.41 [0.36-0.47]12mgdeath/hosp.7,898 (n)20,150 (n)CT2Manomai.. (DB RCT)43%0.57 [0.20-1.46]48mgno recov.3/366/36Rocha (DB RCT)-187%2.87 [0.12-67.5]36mgmisc.1/300/26Tau2 = 0.08, I2 = 38.8%, p < 0.0001Early treatment69%0.31 [0.24-0.39]37/12,406197/39,34969% improvementGorial71%0.29 [0.01-5.76]14mgdeath0/162/71Improvement, RR [CI]Dose (4d)TreatmentControlPodder (RCT)16%0.84 [0.55-1.12]14mgrecov. time32 (n)30 (n)Khan87%0.13 [0.02-1.00]12mgdeath1/1159/133Chachar (RCT)10%0.90 [0.44-1.83]36mgno recov.9/2510/25Rajter (PSM)46%0.54 [0.27-0.99]14mgdeath13/9824/98Hashim (SB RCT)92%0.08 [0.00-1.44]28mgdeath0/596/70CT2Camprubí40%0.60 [0.18-2.01]14mgventilation3/135/13Spoorthi21%0.79 [0.64-0.98]n/arecov. time50 (n)50 (n)CT2Budhiraja99%0.01 [0.00-0.15]n/adeath0/34103/942Okumuş (DB RCT)33%0.67 [0.27-1.64]56mgdeath6/309/30Shahbazn.. (DB RCT)-197%2.97 [0.13-70.5]14mgdeath1/350/34Lima-Morales78%0.22 [0.12-0.41]12mgdeath15/48152/287CT2Pott-Junior (RCT)85%0.15 [0.01-1.93]14mgventilation1/271/4censored, see notesHuvemek (DB RCT)32%0.68 [0.38-1.23]84mgno improv.13/5019/50Abd-Elsalam (RCT)25%0.75 [0.17-3.06]36mgdeath3/824/82Rezk80%0.20 [0.01-4.13]72mgdeath0/1602/160Lim (RCT)69%0.31 [0.09-1.11]112mgdeath3/24110/249Ozer75%0.25 [0.06-1.13]28mgdeath2/608/60Jamir (ICU)-53%1.53 [0.88-2.67]n/adeath32/7669/190ICU patientsBaguma97%0.03 [0.00-11.7]n/adeath7 (n)474 (n)Shimizu100%0.00 [0.00-0.01]14mgdeath0/398/49Efimenko (PSM)69%0.31 [0.20-0.48]n/adeath1,072 (n)40,536 (n)self-censored, see notes OT1George (RCT)30%0.70 [0.25-1.93]24mgdeath5/358/39Naggie (DB RCT)-195%2.95 [0.12-72.2]84mgdeath1/8170/774Tau2 = 0.39, I2 = 71.5%, p < 0.0001Late treatment53%0.47 [0.32-0.67]108/3,654349/44,45053% improvementShouman (RCT)91%0.09 [0.03-0.23]36mgsymp. case15/20359/101Improvement, RR [CI]Dose (1m)TreatmentControlBehera54%0.46 [0.29-0.71]42mgcases41/117145/255Bernigaud99%0.01 [0.00-0.10]84mgdeath0/69150/3,062Alam91%0.09 [0.04-0.25]12mgcases4/5844/60Chahla (RCT)95%0.05 [0.00-0.80]48mgm/s case0/11710/117CT2Behera83%0.17 [0.12-0.23]42mgcases45/2,199133/1,147Seet (CLUS. RCT)50%0.50 [0.33-0.76]12mgsymp. case32/61764/619OT1Morgenstern (PSM)80%0.20 [0.01-4.15]56mghosp.0/2712/271Mondal88%0.12 [0.01-0.55]n/asymp. case128 (n)1,342 (n)Kerr (PSM)70%0.30 [0.19-0.46]56mgdeath25/3,03479/3,034Tau2 = 0.47, I2 = 86.0%, p < 0.0001Prophylaxis82%0.18 [0.11-0.32]162/6,813686/10,00882% improvementAll studies68%0.32 [0.26-0.40]307/22,8731,232/93,80768% improvement58 ivermectin COVID-19 studies after exclusionsivmmeta.com Jun 2022Tau2 = 0.32, I2 = 76.5%, p < 0.0001Effect extraction pre-specified, see appendix1 OT: ivermectin vs. other treatment3 CS: preprint censored, see details2 CT: study uses combined treatmentFavors ivermectinFavors control
Figura 21. Meta-análise de efeitos aleatórios excluindo estudos com problemas significativos. A extração do efeito é pré-especificada, usando o resultado mais grave relatado, consulte o
apêndice para obter detalhes.HeterogeneidadeA heterogeneidade nos estudos COVID-19 surge de muitos fatores, incluindo:
Atraso no tratamento. O tempo entre a infecção ou o início dos sintomas e o tratamento pode afetar criticamente o funcionamento de um tratamento. Por exemplo, um antiviral pode ser muito eficaz quando usado precocemente, mas pode não ser eficaz na doença em estágio avançado e pode até ser prejudicial. O oseltamivir, por exemplo, geralmente só é considerado eficaz para influenza quando usado dentro de 0-36 ou 0-48 horas
A Figura 22 mostra uma meta-regressão de efeitos mistos para eficácia em função do atraso no tratamento em estudos COVID-19 de
42 tratamentos , mostrando que a eficácia diminui rapidamente com o atraso no tratamento. O tratamento precoce é fundamental para o COVID-19.
Figura 22. Meta-regressão mostrando eficácia em função do atraso do tratamento em estudos de COVID-19 de
42 tratamentos . O tratamento precoce é fundamental.
Demografia do paciente. Detalhes da população de pacientes, incluindo idade e comorbidades, podem afetar criticamente o desempenho de um tratamento. Por exemplo, muitos estudos de COVID-19 com pacientes relativamente jovens com baixa comorbidade mostram que todos os pacientes se recuperam rapidamente com ou sem tratamento. Nesses casos, há pouco espaço para um tratamento eficaz para melhorar os resultados (como em
[ López-Medina ] ).
Efeito medido. A eficácia pode diferir significativamente dependendo do efeito medido, por exemplo, um tratamento pode ser muito eficaz na redução da mortalidade, mas menos eficaz na minimização de casos ou hospitalização. Ou um tratamento pode não ter efeito sobre a eliminação viral enquanto ainda é eficaz na redução da mortalidade.
Variantes. Existem muitas variantes diferentes do SARS-CoV-2 e a eficácia pode depender criticamente da distribuição das variantes encontradas pelos pacientes em um estudo. Por exemplo, a variante Gamma apresenta características significativamente diferentes
[ Faria , Karita , Nonaka , Zavascki ] . Diferentes mecanismos de ação podem ser mais ou menos eficazes dependendo das variantes, por exemplo, o processo de entrada viral para a variante omicron mudou para a fusão independente de TMPRSS2, sugerindo que os inibidores de TMPRSS2 podem ser menos eficazes
Regime. A eficácia pode depender fortemente da dosagem e do regime de tratamento. Verificou-se que doses mais altas são mais bem-sucedidas para ivermectina
[ Babalola ] . O método de administração também pode ser crítico.
[ Guzzo ] mostram que a concentração plasmática de ivermectina é muito maior quando administrada com alimentos (
Figura 23 : AUC média geométrica 2,6 vezes maior). Muitos estudos de ivermectina especificam jejum ou não especificam a administração. Espera-se que a administração em jejum reduza a eficácia do COVID-19 devido a concentrações mais baixas no plasma e nos tecidos. Observe que isso é diferente do uso de anti-helmínticos no trato gastrointestinal, onde o jejum é recomendado.
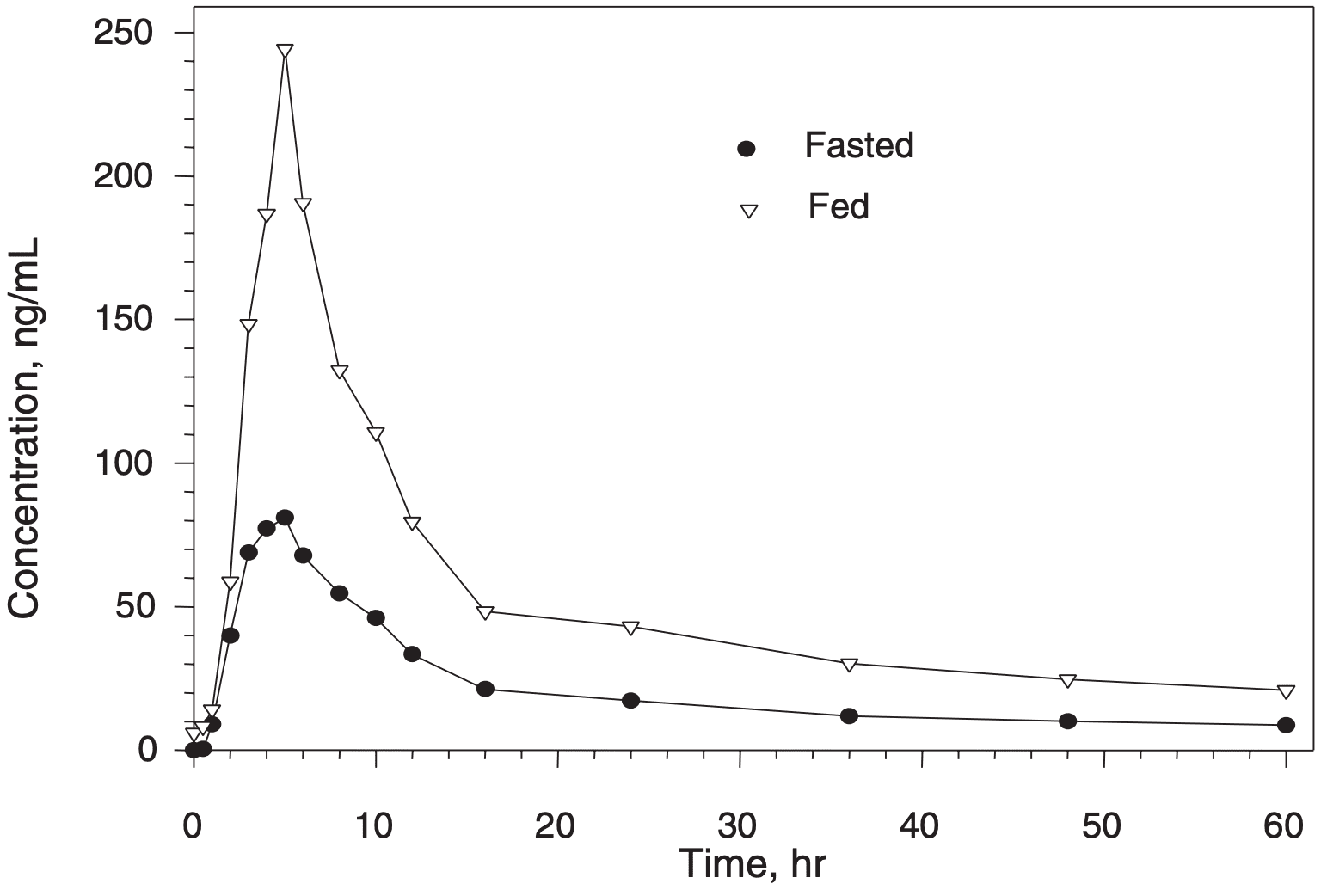
Figura 23. Perfis de concentração plasmática média (ng/ml) de ivermectina após doses orais únicas de 30 mg (administração alimentada e em jejum), de
[ Guzzo ] .
Tratamentos. O uso de outros tratamentos pode afetar significativamente os resultados, incluindo suplementos, outros medicamentos ou outros tipos de tratamento, como posicionamento de bruços.A distribuição dos estudos irá alterar o resultado de uma meta-análise. Considere um exemplo simplificado em que tudo é igual, exceto o atraso do tratamento, e a eficácia diminui para zero ou abaixo com o aumento do atraso. Se houver muitos estudos usando tratamento muito tardio, o resultado pode ser negativo, mesmo que o tratamento possa ser muito eficaz quando usado mais cedo.Em geral, ao combinar estudos heterogêneos, como fazem todas as metanálises, corremos o risco de obscurecer um efeito ao incluir estudos em que o tratamento é menos eficaz, ineficaz ou prejudicial.Ao incluir estudos em que um tratamento é menos eficaz, esperamos que o tamanho do efeito estimado seja menor do que para o caso ideal.
A priori , não esperamos que o agrupamento de todos os estudos crie um resultado positivo para um tratamento eficaz. A análise de todos os estudos é valiosa para fornecer uma visão geral de todas as pesquisas, importante para evitar a escolha seletiva e informativa quando um resultado positivo é encontrado, apesar de combinar situações menos ideais. No entanto, a estimativa resultante não se aplica a casos específicos, como tratamento precoce em populações de alto risco.Os estudos com ivermectina variam amplamente em todos os fatores acima, o que torna os resultados consistentemente positivos ainda mais notáveis. A falha em detectar uma associação após a combinação de estudos heterogêneos não significa que o tratamento não seja eficaz (pode funcionar apenas em alguns casos), mas o inverso não é verdadeiro – uma associação identificada é válida, embora a magnitude do efeito possa ser maior para casos mais ótimos e menor para casos menos ótimos. Como acima, a probabilidade de um tratamento ineficaz gerar resultados tão positivos quanto os 85 estudos até o momento é estimada em 1 em 43 bilhões. Esse resultado se beneficia do fato de a ivermectina apresentar algum grau de eficácia para COVID-19 em uma ampla variedade de casos. Também é provável que se beneficie do fato de que relativamente poucos ensaios com ivermectina até o momento foram projetados de forma a favorecer resultados ruins. No entanto, são esperados mais ensaios projetados dessa maneira, por exemplo, o ensaio TOGETHER está testando a ivermectina em locais conhecidos por ter um alto grau de automedicação e usando doses baixas em comparação com as recomendações clínicas atuais, atualizadas para as variantes atuais. Tal como acontece com um estudo complementar, este estudo também pode incluir pacientes de risco muito baixo, incluir tratamento relativamente tardio ao identificar como um estudo de tratamento inicial e usar um placebo ativo (vitamina C). Embora apresentemos resultados para todos os estudos neste artigo, as análises de resultados individuais e de tempo de tratamento são mais relevantes para casos de uso específicos. por exemplo, o estudo TOGETHER está testando a ivermectina em locais conhecidos por ter um alto grau de automedicação e usando doses baixas em comparação com as recomendações clínicas atuais, atualizadas para as variantes atuais. Tal como acontece com um estudo complementar, este estudo também pode incluir pacientes de risco muito baixo, incluir tratamento relativamente tardio ao identificar como um estudo de tratamento inicial e usar um placebo ativo (vitamina C). Embora apresentemos resultados para todos os estudos neste artigo, as análises de resultados individuais e de tempo de tratamento são mais relevantes para casos de uso específicos. por exemplo, o estudo TOGETHER está testando a ivermectina em locais conhecidos por ter um alto grau de automedicação e usando doses baixas em comparação com as recomendações clínicas atuais, atualizadas para as variantes atuais. Tal como acontece com um estudo complementar, este estudo também pode incluir pacientes de risco muito baixo, incluir tratamento relativamente tardio ao identificar como um estudo de tratamento inicial e usar um placebo ativo (vitamina C). Embora apresentemos resultados para todos os estudos neste artigo, as análises de resultados individuais e de tempo de tratamento são mais relevantes para casos de uso específicos. inclua o tratamento relativamente tardio enquanto se identifica como um estudo de tratamento precoce e use um placebo ativo (vitamina C). Embora apresentemos resultados para todos os estudos neste artigo, as análises de resultados individuais e de tempo de tratamento são mais relevantes para casos de uso específicos. inclua o tratamento relativamente tardio enquanto se identifica como um estudo de tratamento precoce e use um placebo ativo (vitamina C). Embora apresentemos resultados para todos os estudos neste artigo, as análises de resultados individuais e de tempo de tratamento são mais relevantes para casos de uso específicos.Discussão
Viés de publicação. A publicação é muitas vezes tendenciosa para resultados positivos, para os quais precisaríamos ajustar ao analisar a porcentagem de resultados positivos. Para a ivermectina, atualmente não há dados suficientes para avaliar o viés de publicação com alta confiança. Um método para avaliar o viés é comparar estudos prospectivos versus retrospectivos. Estudos prospectivos provavelmente serão publicados independentemente do resultado, enquanto estudos retrospectivos são mais propensos a apresentar viés. Por exemplo, os pesquisadores podem realizar análises preliminares com esforço mínimo e os resultados podem influenciar sua decisão de continuar. Os estudos retrospectivos também oferecem mais oportunidades para as especificidades da extração de dados e ajustes para influenciar os resultados.
Figura 24mostra um gráfico de dispersão de resultados para estudos prospectivos e retrospectivos. O tamanho do efeito mediano para estudos prospectivos é de 68% de melhora, comparado a 70% para estudos retrospectivos, não mostrando diferença significativa.
[ Bryant ] também realizam uma análise de gráfico de funil, que eles descobriram não sugerir evidências de viés de publicação. A ivermectina tem uma das bases de evidências mais observadas e examinadas de perto na história. Estudos negativos são enviados a nós por várias pessoas imediatamente após a publicação. Por outro lado, há evidências substanciais de que os periódicos estão rejeitando e atrasando a publicação de estudos positivos, por exemplo, aceitando um artigo para revisão, mantendo-o por algum tempo e depois rejeitando-o sem revisão
[ Jerusalem Post, Kory (B) ] . Um grupo realizou ensaios de profilaxia e tratamento precoce, com apenas o estudo menos positivo sendo formalmente publicado até o momento
[ IVERCOR PREP , Vallejos ] , sugerindo um viés de publicação negativo. O RCT duplo-cego do Dr. Eli Schwartz
[ Biber ] foi rejeitado sem revisão pela The Lancet e Clinical Infectious Diseases
[ Fox ] . Autores de
[ Efimenko ]não planejam submeter os resultados muito positivos a um periódico e autocensuraram a publicação da conferência, fornecendo mais evidências de um viés de publicação negativo. Ensaios com publicação pendente e possivelmente atrasada geralmente envolvem pesquisadores que podem ser restritos devido à política – a publicação de resultados positivos pode ser incompatível com a continuidade do emprego, enquanto resultados negativos podem receber tratamento prioritário em certos periódicos conhecidos, apoiar as posições de empregadores ou organizações de financiamento , e receber imprensa substancial.
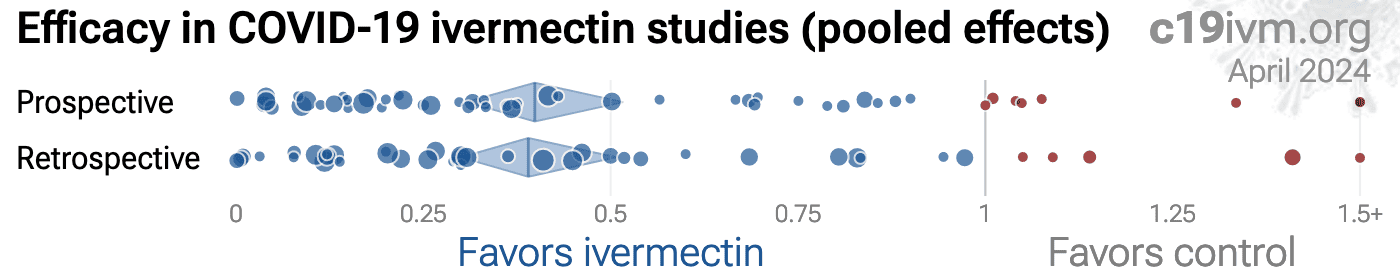
Figura 24. Estudos prospectivos vs. retrospectivos.A cobertura jornalística dos estudos com ivermectina é extremamente tendenciosa. Apenas dois estudos até o momento receberam cobertura significativa da imprensa na mídia ocidental
[ López-Medina , Reis ] , ambos com vários problemas críticos, conforme discutido abaixo.
Resultados da série de casos do médico.A Tabela 4 mostra os resultados relatados de médicos que usam tratamentos precoces para COVID-19, em comparação com os resultados de um médico não tratador (este médico supostamente prescreveu tratamento precoce para si mesmo, mas não para pacientes
[ medicospelavidacovid19.com.br ] ). Os tratamentos utilizados variam entre os médicos. Quase todos relatam o uso de ivermectina e/ou HCQ, e a maioria usa tratamentos adicionais em combinação. Uma análise mais detalhada requer informações sobre as populações de pacientes, no entanto, os resultados são consistentes com as extensas evidências de estudos controlados que mostram uma redução significativa no risco com tratamentos precoces e melhores resultados com o uso de vários tratamentos.
| TRATAMENTO TARDIO | ||||||
| Médico / Equipe | Localização | Pacientes | Hospitalização | Mortalidade | ||
| Dr. David Uip (*) | Brasil | 2.200 | 38,6% (850) | Ref. | 2,5% (54) | Ref. |
| TRATAMENTO PRECOCE – 31 médicos/equipes | ||||||
| Médico / Equipe | Localização | Pacientes | Hospitalização | Melhoria | Mortalidade | Melhoria |
| Dr. Roberto Alfonso Accinelli 0/360 óbitos por tratamento em 3 dias | Peru | 1.265 | 0,6% (7) | 77,5% | ||
| Pacientes do Dr. Mohammed Tarek Alam até 84 anos | Bangladesh | 100 | 0,0% (0) | 100,0% | ||
| Dr. Oluwagbenga Alonge | Nigéria | 310 | 0,0% (0) | 100,0% | ||
| Dr. Raja Bhattacharya até 88 anos, 81% de comorbidades | Índia | 148 | 1,4% (2) | 44,9% | ||
| Dr. Flávio Cadegiani | Brasil | 3.450 | 0,1% (4) | 99,7% | 0,0% (0) | 100,0% |
| Dr. Alessandro Capucci | Itália | 350 | 4,6% (16) | 88,2% | ||
| Dr. Shankara Chetty | África do Sul | 8.000 | 0,0% (0) | 100,0% | ||
| Dra. Deborah Chisholm | EUA | 100 | 0,0% (0) | 100,0% | ||
| Dr. Ryan Cole | EUA | 400 | 0,0% (0) | 100,0% | 0,0% (0) | 100,0% |
| Dr. Marco Cosentino vs. 3-3,8% de mortalidade no período; tratamento precoce melhor | Itália | 392 | 6,4% (25) | 83,5% | 0,3% (1) | 89,6% |
| Dr. Dhanajay | Índia | 500 | 0,0% (0) | 100,0% | ||
| Dr. Bryan Tyson e Dr. George Fareed | EUA | 4.375 | 0,2% (9) | 99,5% | 0,1% (3) | 97,2% |
| Dra. Heather Gessling | EUA | 1.500 | 0,1% (1) | 97,3% | ||
| Dra. Ellen Guimarães | Brasil | 500 | 1,6% (8) | 95,9% | 0,4% (2) | 83,7% |
| Dr. Syed Haider | EUA | 4.000 | 0,1% (5) | 99,7% | 0,0% (0) | 100,0% |
| Dr. Mark Hancock | EUA | 24 | 0,0% (0) | 100,0% | ||
| Dra. Mollie James | EUA | 3.500 | 1,1% (40) | 97,0% | 0,0% (1) | 98,8% |
| Dra. Roberta Lacerda | Brasil | 550 | 1,5% (8) | 96,2% | 0,4% (2) | 85,2% |
| Dr. Ben Mármore | EUA | 150.000 | 0,0% (4) | 99,9% | ||
| Dr. Edimilson Migowski | Brasil | 2.000 | 0,3% (7) | 99,1% | 0,1% (2) | 95,9% |
| Dr. Abdulrahman Mohana | Arábia Saudita | 2.733 | 0,0% (0) | 100,0% | ||
| Dr. Carlos Nigro | Brasil | 5.000 | 0,9% (45) | 97,7% | 0,5% (23) | 81,3% |
| Dr. Benoit Ochs | Luxemburgo | 8.000 | 0,0% (0) | 100,0% | ||
| Dr. Valerio Pascua uma morte para um paciente que se apresentou no 5º dia com necessidade de oxigênio suplementar | Honduras | 415 | 6,3% (26) | 83,8% | 0,2% (1) | 90,2% |
| Dr. Brian Proctor | EUA | 869 | 2,3% (20) | 94,0% | 0,2% (2) | 90,6% |
| Dr. Anastácio Queiroz | Brasil | 700 | 0,0% (0) | 100,0% | ||
| Dr. Didier Raoult | França | 8.315 | 2,6% (214) | 93,3% | 0,1% (5) | 97,6% |
| Dra. Karin Ried até 99 anos, 73% comorbidades, av. 63 anos | Peru | 237 | 0,4% (1) | 82,8% | ||
| Pacientes do Dr. Roman Rozencwaig até 86 anos | Canadá | 80 | 0,0% (0) | 100,0% | ||
| Dr. Vipul Shah | Índia | 8.000 | 0,1% (5) | 97,5% | ||
| Dr. Vladimir Zelenko | EUA | 2.200 | 0,5% (12) | 98,6% | 0,1% (2) | 96,3% |
| Melhora média com protocolos de tratamento precoces | 220.213 | Hospitalização | 95,1% | Mortalidade | 93,5% |
Tabela 4. Resultados do médico com protocolos de tratamento precoce em comparação com nenhum tratamento precoce.
(*) Dr. Uip teria prescrito tratamento precoce para si mesmo, mas não para os pacientes
[ medicospelavidacovid19.com.br ] .
Análise de gráfico de funil. Tradicionalmente, gráficos de funil têm sido usados para analisar o viés de publicação. Isso é inválido para testes de tratamento agudo com COVID-19 – as suposições subjacentes são inválidas, o que podemos demonstrar com um exemplo simples. Considere um conjunto de tentativas perfeitas hipotéticas sem viés.
Figura 25o gráfico A mostra um gráfico de funil para uma simulação de 80 ensaios perfeitos, com tamanhos de grupos aleatórios e o resultado de cada paciente amostrado aleatoriamente (10% de probabilidade de evento de controle e um tamanho de efeito de 30% para tratamento). A análise não mostra assimetria (p > 0,05). No gráfico B, adicionamos uma única variação típica nos ensaios de tratamento com COVID-19 – atraso no tratamento. Considere que a eficácia varia de 90% para tratamento em 24 horas, reduzindo para 10% quando o tratamento é atrasado 3 dias. No gráfico B, o atraso de tratamento de cada ensaio é selecionado aleatoriamente. A análise agora mostra assimetria altamente significativa,
p < 0,0001, com seis variantes do teste de Egger mostrando p < 0,05
[ Egger , Harbord , Macaskill , Moreno , Peters, Rothstein , Rücker , Stanley ] . Observe que esses testes falham mesmo que o atraso do tratamento seja distribuído uniformemente. Na realidade, o atraso no tratamento é mais complexo — cada ensaio tem uma distribuição diferente de atrasos entre os pacientes, e a distribuição entre os ensaios pode ser tendenciosa (por exemplo, ensaios de tratamento tardios podem ser mais comuns). Da mesma forma, muitas outras variações nos ensaios podem produzir assimetria, incluindo dose, administração, duração do tratamento, diferenças no SOC, comorbidades, idade, variantes e viés no projeto, implementação, análise e relatório.
Figura 25. Exemplo de análise de gráfico de funil para tentativas perfeitas simuladas.
Evidências in vitro sobre a concentração necessária. Algumas pessoas afirmam que
[ Caly ] mostra que as concentrações terapêuticas não são facilmente alcançadas em humanos. Isso está incorreto. Os autores explicam por que seu estudo
in vitro não pode ser usado para determinar a dose efetiva
in vivo e afirmam que é muito improvável que a concentração necessária seja um problema
[ Wagstaff ]. O estudo utilizou células renais de macaco (a única opção na época dos experimentos), que não possuem respostas imunes adaptativas e não produzem interferon. Os autores também observam que a ivermectina se acumula no pulmão e em outros tecidos, que experimentos subsequentes com células pulmonares mostram concentrações muitas vezes maiores e que a concentração pulmonar média mostrada em estudos de modelagem excede o nível efetivo mostrado em suas pesquisas. Os autores observam que a ivermectina funciona com o sistema imunológico e é improvável que seja necessária uma proporção de 1:1 de medicamento para vírus. Em
[ Bray ], o autor responde que “o principal alvo direto da ivermectina em células de mamíferos não é um componente viral, mas uma proteína do hospedeiro importante no transporte intracelular; o fato de ser um agente direcionado ao hospedeiro (HDA) é quase certamente a base de sua ampla atividade do espectro contra vários vírus de RNA diferentes in vitro. A forma como um HDA pode reduzir a carga viral é inibindo um processo celular chave que o vírus sequestra para aumentar a infecção, suprimindo a resposta antiviral do hospedeiro. Reduzindo a carga viral em uma quantidade modesta, usar um HDA em baixa dose no início da infecção pode ser a chave para permitir que o sistema imunológico do corpo comece a montar a resposta antiviral completa antes que a infecção assuma o controle”. Em pesquisas adicionais, os autores observam que encontram eficácia para uso profilático,
[ Wagstaff ] .
Strongyloides. Uma teoria para o efeito benéfico da ivermectina para COVID-19 está relacionada aos estrongiloides e ao uso de esteroides – pacientes do grupo controle com estrongiloides podem estar em risco devido ao uso de esteroides, enquanto os pacientes com ivermectina estão protegidos. Embora esse mecanismo possa contribuir para a eficácia em alguns casos, ele é inconsistente com os dados. Se este fosse o caso, esperaríamos ver maiores benefícios em estudos de estágio final, onde os esteróides são usados com mais frequência, e esperaríamos ver maiores benefícios para os resultados que ocorrem após o uso de esteróides. No entanto, vemos um efeito oposto muito forte para o tempo de tratamento e vemos eficácia comparável ou mais forte para resultados anteriores.A teoria ganhou interesse renovado com base em uma nova análise
[ Bitterman ] . No entanto, esta análise é confundida pelo atraso do tratamento, dose, conflitos de interesse e outros fatores, e o efeito desaparece ao analisar todos os estudos, todos os ECRs ou todos os resultados de mortalidade, conforme mostrado na
Figura 26 .Embora o primeiro autor tenha respondido aos confundidores no Twitter, não vemos menção deles no artigo. O autor também está ciente de que os conjuntos maiores de todos os ensaios, todos os ensaios clínicos randomizados ou todos os resultados de mortalidade não mostram o efeito, no entanto, também não vemos isso mencionado no artigo. Essas omissões sugerem viés do investigador. O autor alega que não pôde discutir esses problemas devido a atrasos na publicação, no entanto, o artigo foi aceito em 31 de janeiro de 2022 e o autor estava ciente dos problemas meses antes, por exemplo, discutindo atraso e dose do tratamento em novembro de 2021. Esses fatores de confusão também são básicos e não é realmente possível perder.A meta-análise para
[ Hashim ] inclui pacientes críticos, no entanto, esses pacientes sempre foram alocados no braço de tratamento por razões éticas, portanto, incluí-los não é lógico e introduz viés substancial. De acordo com a resposta do autor, isso parece ter sido conhecido, sugerindo viés do investigador. Os autores incluem
[ Shahbaznejad ] onde a única morte foi um paciente crítico que morreu dentro de 24 horas após a admissão.Embora os autores observem seguir as diretrizes do PRISMA, não vemos o registro do protocolo ou sua discussão. Observamos que o protocolo atual é o resultado de várias alterações na metodologia original, conforme postado no Twitter: de 3 grupos para 2 grupos, alterando os estudos incluídos e mudando de usar uma fonte para estimativas de prevalência para selecionar fontes de estimativa em um por estudo base, o que permite um potencial viés na seleção. Notavelmente, isso resultou na mudança do Together Trial (Brasil) para a categoria de baixa prevalência.Os resultados do autor baseiam-se em ensaios com um número muito pequeno de eventos de mortalidade – o grupo de alta prevalência de strongoides tem ensaios com 1, 3, 4 e 13 eventos. Os autores mencionam limitações devido ao pequeno número de eventos e à confiabilidade das estimativas de Strongyloides.Os autores não indicam conflitos de interesse, no entanto, o primeiro autor foi investigador em um estudo da Pfizer, que pode ser NCT04092452, mostrando conclusão em janeiro de 2022
[ clinicaltrials.gov , openpaymentsdata.cms.gov ] .
Figura 26. Meta-regressão de efeitos mistos mostrando eficácia em função da prevalência de Strongyloides para todos os estudos, todos os ECRs e todos os resultados de mortalidade.O seguinte refere-se à análise do primeiro autor postada anteriormente no Twitter. O autor selecionou 10 dos 85 estudos, com 3 em um grupo de alta prevalência de Strongyloides onde um maior benefício é visto. Isso foi usado para tirar conclusões fortes sobre o mecanismo de eficácia da ivermectina.Existem várias limitações para esta análise. Um dos 3 estudos não menciona esteróides na lista de medicamentos SOC, enquanto um segundo relata uso de 6% para o grupo controle. O autor adicionou um quarto artigo em um agrupamento revisado com 11 estudos.Realizamos uma análise semelhante para todos os estudos (exceto os 2 estudos ecológicos), que não mostra efeito significativo, com o grupo de alta prevalência realmente apresentando melhora menor (51%
[36-63%] vs. 69%
[61-76%] para o grupo de baixa prevalência). Os detalhes podem ser encontrados nos
dados suplementares . Os resultados são semelhantes quando restritos a resultados de mortalidade ou quando restritos a ECRs.Por que a análise menor com 11 estudos mostra um benefício maior em regiões de alta prevalência de Strongyloides? O efeito é baseado em relativamente poucos eventos – 1, 3, 4 e 13 respectivamente para o grupo de alta prevalência. Mais importante, o resultado é confundido pelo atraso do tratamento e pela dose.
Atraso no tratamento. Todas as meta-análises combinam estudos heterogêneos, o que resulta em limitações. Por exemplo, na análise agrupada, combinamos hospitalização e mortalidade. Em termos de avaliação da eficácia dos tratamentos com COVID-19, a redução na hospitalização leva razoavelmente à redução da mortalidade para populações de alto risco. Ambos são indicadores de eficácia e ambos são valiosos. Na maior série de ensaios de tratamento com COVID-19, as estimativas de hospitalização e mortalidade são muito semelhantes. O mesmo não se aplica ao atraso no tratamento dos antivirais. Um estudo que mostra eficácia com tratamento precoce não fornece informações sobre tratamento tardio, e um estudo que não apresenta eficácia com tratamento tardio não fornece informações sobre tratamento precoce. Ivermectina, como em muitos tratamentos COVID-19,O grupo de alta prevalência na análise de 11 estudos tem mais ensaios de tratamento precoce, e o grupo de baixa prevalência tem mais ensaios de tratamento tardio. O resultado é confundido pelo atraso do tratamento e reflete a maior eficácia do tratamento precoce.Apenas um ensaio no grupo de alta prevalência é classificado como tratamento tardio, I-TECH, que ficou muito próximo do ponto de corte. Além disso, de todos os ensaios na análise de 11 ensaios, este usa a dose mais alta.
Dose . A dosagem média usada no grupo de alta prevalência é cerca de duas vezes a dose no grupo de baixa prevalência, e seria cerca de três vezes maior se o ensaio conjunto não fosse movido para o grupo de baixa prevalência. O resultado é confundido pela dose e reflete a maior eficácia de dosagens mais altas.
Variantes . A eficácia pode variar com base nas variantes. Notavelmente, a variante Gamma foi mais comum para um estudo no grupo de baixa prevalência. Esta variante mostra características dramaticamente diferentes
[ Zavascki ] , e os médicos relatam que é necessária uma dosagem significativamente maior e/ou tratamento precoce, como pode ser esperado para variantes em que o pico de carga viral é significativamente maior e/ou atingido mais cedo
Conflitos de interesse . Dois ensaios têm conflitos de interesse negativos muito altos (> $US1B) que podem introduzir viés para efeitos nulos. O estudo no grupo de baixa prevalência mostra um tamanho de efeito menor. O estudo no grupo de alta prevalência também mostra um tamanho de efeito menor para o desfecho primário. Este estudo mostra um efeito de mortalidade maior, no entanto, com apenas um evento, isso tem significância muito baixa.
Resumo . Em resumo, o maior benefício em regiões de alta prevalência de Strongyloides é observado apenas com o pequeno subconjunto de 11 ensaios e não é observado em todos os ensaios, ou após restrição aos resultados de mortalidade ou restrição a ECRs. Dentro da amostra de 11 ensaios, todos os ensaios, exceto um no grupo de baixa prevalência, apresentam fatores de confusão devido ao atraso no tratamento e/ou baixa dosagem, onde um tamanho de efeito menor é esperado. O único estudo restante no grupo é inédito, tem um atraso de tratamento desconhecido (uma porcentagem significativa de pacientes pode ter sido tratada muito tarde), tem conflitos de interesse negativos muito altos e a variante Gamma foi a mais comum, além de
Conflitos de interesse. Ensaios de medicamentos farmacêuticos geralmente têm conflitos de interesse em que os patrocinadores ou a equipe do ensaio têm interesse financeiro em que o resultado seja positivo. A ivermectina para COVID-19 não tem isso porque não é patenteada, tem muitos fabricantes e tem um custo muito baixo. Em contraste, a maioria dos ensaios de ivermectina COVID-19 foi realizada por médicos na linha de frente com o interesse principal de encontrar os melhores métodos para salvar vidas humanas e minimizar os danos colaterais causados pelo COVID-19. Embora as empresas farmacêuticas tenham o cuidado de realizar ensaios em condições ideais (por exemplo, restringindo os pacientes àqueles com maior probabilidade de se beneficiar, incluindo apenas pacientes que podem ser tratados logo após o início, quando necessário, garantindo a dosagem precisa), muitos ensaios de ivermectina não representam a solução ideal. condições de eficácia.Dois ensaios de ivermectina até o momento envolvem conflitos de interesse financeiros muito grandes
[ López-Medina , Reis ] – empresas intimamente envolvidas com o ensaio ou organizadores podem perder bilhões de dólares se a eficácia da ivermectina se tornar mais amplamente conhecida. O desenho destes ensaios favorece a produção de um resultado nulo conforme detalhado em
[ López-Medina , Reis ] . Observe que é difícil influenciar um RCT para produzir um resultado falso positivo (suprimir eventos adversos é relativamente fácil
[ Evans ]), mas influenciar um ensaio para produzir um resultado falso negativo é muito fácil — por exemplo, em um ensaio de um antiviral que funciona nas primeiras 24 horas do início dos sintomas, os organizadores do ensaio só precisam evitar tratar as pessoas nas primeiras 24 horas; ou com uma doença como o COVID-19, os organizadores só precisam selecionar uma população de baixo risco, onde a maioria das pessoas se recupera rapidamente sem tratamento. Observamos que, mesmo sob os desenhos muito subótimos, esses ensaios produziram resultados positivos, embora sem significância estatística.
Projetado para falhar. Ensaios futuros adicionais, incluindo ACTIV-6, COVID-OUT e PRINCIPLE, foram projetados de uma maneira que favorece a ausência de efeito, com vários métodos, incluindo tratamento tardio, seleção de pacientes de baixo risco, administração em jejum, medicação de conflito de interesse muito alto fonte e dosagem abaixo da prática clínica atual. Para discussão veja
[ Goodkin ] .O COVID-OUT está inscrevendo pacientes de risco relativamente baixo (idade média de 46 anos, 0,45 comorbidades médias), inclui pacientes assintomáticos e tem um longo atraso entre os sintomas e o tratamento com base no atraso da coleta da amostra em
[ Bramante ] .A PRINCIPLE interrompeu a inscrição em dezembro de 2021, alegando que havia um problema de fornecimento
[ Henderson ] , no entanto, o fabricante que forneceu o teste informou que não estava enfrentando problemas de fornecimento. Em 27 de janeiro de 2022, o julgamento foi interrompido sem explicação. Em 11 de fevereiro de 2022, o estudo foi aberto de forma intermitente (duas vezes ao dia entre domingo e quinta-feira), o que diminuiria ainda mais as chances de os participantes receberem tratamento relativamente precoce.Um paciente relatou sua experiência com um dos ensaios ambulatoriais remotos de ivermectina/fluvoxamina: eles receberam a inscrição 7 dias após os sintomas (o recebimento da medicação seria ainda mais tarde), receberam US$ 400 para participar e supostamente visavam pessoas saudáveis
[ twitter.com ] . O ACTIV-6 também supostamente não envia os medicamentos do estudo no fim de semana, adicionando atrasos adicionais
[ twitter.com (B) ] .Se esses estudos fornecerem resultados para pacientes de alto risco estratificados por atraso no tratamento, incluindo pacientes tratados dentro de 1, 2 e 3 dias do início dos sintomas (incluindo qualquer atraso no envio), eles podem ser informativos mesmo com dosagem limitada.
Precoce/tardio vs. leve/moderado/grave. Algumas análises classificam o tratamento com base na administração precoce/tardia (como fazemos aqui), enquanto outras distinguem entre casos leves/moderados/graves. Observamos que a carga viral não indica o grau de sintomas – por exemplo, os pacientes podem ter uma carga viral alta enquanto são assintomáticos. No que diz respeito aos tratamentos que possuem propriedades antivirais, o momento do tratamento é crítico – a administração tardia pode ser menos útil, independentemente da gravidade.
Notas. Os 85 estudos são de 77 equipes de pesquisa independentes. 4 estudos comparam com outros tratamentos em vez de placebo. Atualmente a ivermectina apresenta melhores resultados do que esses outros tratamentos, porém a ivermectina pode apresentar uma melhora maior quando comparada ao placebo. 17 de 85 estudos combinam tratamentos, por exemplo ivermectina + doxiciclina. Os resultados da ivermectina isoladamente podem diferir. 4 dos 36 ECRs usam tratamento combinado, três com doxiciclina e um com iota-carragenina. 1 de 85 estudos atualmente tem detalhes publicados mínimos disponíveis.
Meta-análises. Meta-análises típicas envolvem critérios de seleção subjetivos, regras de extração de efeitos e avaliação de viés de estudo, que podem ser usados para enviesar os resultados para um resultado específico. Para evitar viés, incluímos todos os estudos e usamos um método pré-especificado para extrair os resultados de todos os estudos (também apresentamos resultados após exclusões). Os resultados até o momento são extremamente positivos, muito consistentes e muito insensíveis a possíveis critérios de seleção, regras de extração de efeitos e/ou avaliação de viés. Meta-análises adicionais confirmando a eficácia da ivermectina podem ser encontradas em
A Figura 27 mostra uma comparação dos resultados de mortalidade entre metanálises.
[ Kory] também revisam dados epidemiológicos e fornecem esquemas de tratamento sugeridos.00.250.50.7511.251.51.752+Kory et al.69%0.31 [0.20-0.47]Improvement, RR [CI]Bryant et al.62%0.38 [0.19-0.73]Lawrie et al.83%0.17 [0.08-0.35]Nardelli et al.79%0.21 [0.11-0.36]Hariyanto et al.69%0.31 [0.15-0.62]WHO (OR)81%0.19 [0.09-0.36]ivmmeta52%0.48 [0.37-0.62]Ivermectin meta analysis mortality resultsivmmeta.com Jun 2022Favors ivermectinFavors control
Figura 27. Comparação dos resultados de mortalidade de diferentes metanálises. OR convertido para RR para
[ Kory , Nardelli ] . OU exibido para
[ WHO ] . A OMS fornece dois resultados, um baseado em 5 estudos e outro baseado em 7, sem explicação para a diferença. O resultado baseado em 7 estudos é mostrado aqui, para os quais os detalhes necessários para calcular o RR não são fornecidos.
Base de evidências. As evidências que apoiam a ivermectina para COVID-19 excedem em muito a quantidade típica de evidências usadas para a aprovação de tratamentos.
[ Lee ] mostra que apenas 14% das diretrizes da Infectious Diseases Society of America foram baseadas em ECRs.
A Tabela 5 e a
Tabela 6 comparam a quantidade de evidências da ivermectina em comparação com a usada para outras aprovações da COVID-19 e a usada pela OMS para a aprovação da ivermectina para sarna e estrongiloidíase.
A Tabela 7 compara as recomendações do CDC dos EUA para ibuprofeno e ivermectina.
| Indicação | Estudos | Pacientes | Status |
| Estrongiloidíase [ Kory (C) ] | 5 | 591 | Aprovado |
| Sarna [ Kory (C) ] | 10 | 852 | Aprovado |
| COVID-19 | 85 | 131.529 | Pendente |
| ECRs COVID-19 | 36 | 8.828 |
Tabela 5. Status de aprovação da ivermectina pela OMS.
| Medicamento | Estudos | Pacientes | Melhoria | Status |
| Molnupiravir (Reino Unido) | 1 | 775 | 50% | Aprovado |
| Budesonida (Reino Unido) | 1 | 1.779 | 17% | Aprovado |
| Remdesivir (EUA EUA) | 1 | 1.063 | 31% | Aprovado |
| Casiri/imdevimab (EUA EUA) | 1 | 799 | 66% | Aprovado |
| Evidência de ivermectina | 85 | 131.529 | 63% [55-70%] | Pendente |
Tabela 6. Base de evidências usada para outras aprovações de COVID-19 em comparação com a base de evidências de ivermectina.
| Ibuprofeno | Ivermectina (para sarna) | Ivermectina (para COVID-19) | |
| Vidas salvas | 0 | 0 | >500.000 |
| Mortes por ano | ~450 | <1 | <1 |
| CDC recomendado | Sim | Sim | Não |
| Baseado em | 0 ECR | 10 RCTs 852 pacientes | 36 ECRs 8.828 pacientes |
Tabela 7. Comparação das recomendações do CDC
[ Kory (C) ] .OMS, Merck, FDA, NIHAnálise da OMS.A OMS atualizou suas recomendações de tratamento em 30/03/2021
[ OMS ] . Para a ivermectina, eles relataram uma razão de chances de mortalidade de 0,19 [0,09-0,36] com base em 7 estudos com 1.419 pacientes. Eles não especificam quais ensaios eles incluíram. O relatório é inconsistente, com um gráfico de floresta que mostra apenas 4 estudos com resultados de mortalidade. A recomendação da OMS não é atualizada há
440 dias.Apesar desse resultado extremamente positivo, recomendaram apenas o uso de ivermectina em ensaios clínicos. A análise contém muitas falhas
[ Kory (D) ] :
•Dos 85 estudos (36 ECRs), eles incluíram apenas 16.
•Eles excluíram todos os 16 estudos de profilaxia (3 RCTs).
•Não houve protocolo para exclusão de dados.
•Os ensaios incluídos no protocolo de pesquisa original da UNITAID foram excluídos.
•Eles excluíram todas as evidências epidemiológicas, embora a OMS tenha considerado tais evidências no passado.
•Eles combinam estudos de tratamento precoce e tardio e não fornecem informações sobre heterogeneidade. Como acima, o tratamento precoce é mais bem-sucedido, portanto, reunir estudos de tratamento tardio obscurecerá a eficácia do tratamento precoce. Eles optaram por não fazer análise de subgrupo por gravidade da doença em todos os ensaios, embora o atraso no tratamento seja claramente um fator crítico no tratamento com COVID-19, a análise é feita facilmente (como acima) e é sabido que os estudos para ivermectina e muitos outros tratamentos mostram claramente maior eficácia para o tratamento precoce.
•A OMS rebaixou a qualidade dos ensaios em comparação com a equipe de revisão sistemática da UNITAID e um grupo separado de diretrizes de especialistas internacionais que trabalha há muito tempo com a OMS
[ Bryant ] .
•Eles desconsideraram suas próprias diretrizes que estipulam que as avaliações de qualidade devem ser atualizadas quando há evidências de um efeito de grande magnitude (o que existe) e quando há evidências de uma relação dose-resposta (o que existe). Eles afirmam que não há relação dose-resposta, enquanto a equipe de revisão sistemática da UNITAID encontrou uma relação clara, juntamente com estudos individuais
[ Babalola ] .
•Suas avaliações de risco de viés não correspondem ao risco real de viés nos estudos. Por exemplo, eles classificam
[ López-Medina ] como de baixo risco de viés, no entanto, este estudo tem muitos problemas, tornando os resultados não confiáveis
[ Análise Covid ] , mesmo levando a uma carta aberta de mais de 170 médicos concluindo que o estudo é fatalmente falho
[ Carta Aberta ] .
[ Beltrão González ]também é classificado como de baixo risco de viés, mas é um estudo com pacientes graves com alta comorbidade em estágio muito tardio. Existe uma relação clara entre o atraso e a resposta do tratamento e não se espera que o tratamento em estágio muito avançado seja tão eficaz quanto o tratamento inicial. Por outro lado, estudos de qualidade muito superior foram classificados como de alto risco de viés.
•Embora a análise da OMS seja chamada de “diretriz de vida”, raramente é atualizada e está muito desatualizada. Em 14 de maio de 2021, quatro dos ECRs ausentes são conhecidos pela OMS e rotulados como “ECRs pendentes de extração de dados”
[ COVID-NMA ] . Adicionamos esses 4, 4, 2 e um mês antes.
•Uma única pessoa serviu como Presidente de Métodos, membro do Comitê de Colaboração de Apoio à Orientação e membro da equipe de Revisão Sistemática Viva/NMA.
•Declarações públicas de pessoas envolvidas na análise sugerem um viés substancial. Por exemplo, um co-presidente teria dito que “os dados disponíveis eram escassos e provavelmente baseados no acaso”
[ Reuters ] . Como acima, os dados são abrangentes e estimamos a probabilidade de um tratamento ineficaz gerar resultados tão positivos quanto os observados em 1 em 43 bilhões. O líder da equipe clínica refere-se à análise da ivermectina como “combatendo esse uso excessivo de terapias não comprovadas … sem evidências de eficácia”
[ Reuters ], apesar da extensa evidência de eficácia dos 85 estudos de 852 cientistas com 131.529 pacientes. As pessoas envolvidas podem ser mais favoráveis ao tratamento em estágio avançado do COVID-19, por exemplo, o copresidente recomendou o tratamento do COVID-19 grave com remdesivir
[ Rochwerg ] .Em resumo, embora a análise da OMS preveja que mais de 2 milhões de pessoas a menos estariam mortas se a ivermectina fosse usada desde o início da pandemia, eles recomendam não usar ensaios externos. Isso parece se basear principalmente na exclusão da maioria das evidências e na atribuição de estimativas de viés que não correspondem ao risco real de viés nos estudos.O uso no início da pandemia foi proposto pela Universidade Kitasato, incluindo o co-descobridor da ivermectina, Dr. Satoshi Ōmura. Eles solicitaram que a Merck realizasse ensaios clínicos de ivermectina para COVID-19 no Japão, porque a Merck tem prioridade para enviar um pedido de expansão das indicações da ivermectina. A Merck recusou
[ Yagisawa ] .Análise Merck.A Merck recomendou contra a ivermectina
[ Merck ] , porém essa recomendação não foi atualizada por
494 dias.Eles afirmaram que
“não há base científica para um potencial efeito terapêutico contra o COVID-19 a partir de estudos pré-clínicos” . Isso é contrariado por muitos artigos e estudos, incluindo
[ Arévalo , Bello , Choudhury , de Melo , DiNicolantonio , DiNicolantonio (B) , Errecalde , Eweas , Francés-Monerris (B) , Heidary , Jans , Jeffreys , Kalfas , Kory , Lehrer , Li , Mody ,Mountain Valley MD , Qureshi , Saha , Surnar , Udofia , Wehbe , Yesilbag , Zaidi , Zatloukal ] .Eles afirmam que
“não há evidências significativas de atividade clínica ou eficácia clínica em pacientes com doença de COVID-19” . Isso é contrariado por vários estudos, incluindo
[ Alam , Aref , Babalola , Baguma , Behera , Behera (B) , Bernigaud , Budhiraja , Bukhari , Chaccour (B) , Chahla , Chahla (B) , Chowdhury , de Jesús Ascencio-Montiel , Elalfy , Espitia-Hernandez , Faisal, Ghauri , Hashim , Huvemek , Kerr , Khan , Lima-Morales , Loue , Mahmud , Manomaipiboon , Mayer , Merino , Mohan , Mondal , Morgenstern , Mourya , Okumuş , Ravikirti (B) , Seet , Shimizu ] .Eles também afirmam que há
“uma preocupante falta de dados de segurança na maioria dos estudos” . A análise de segurança é encontrada em
[ Descotes , Errecalde , Guzzo , Kory , Madrid ] , e os dados de segurança podem ser encontrados na maioria dos estudos, incluindo
[ Abd-Elsalam , Ahmed , Aref , Babalola , Behera (B) , Bhattacharya , Biber , Bukhari , Camprubí , Carvallo (C) , Chaccour (B) , Chahla (B), Chowdhury , Elalfy , Espitia-Hernandez , George , Ghauri , Gorial , Hazan , Huvemek , Khan , Kishoria , Krolewiecki , Lima-Morales , Loue , López-Medina , Mahmud , Mohan , Morgenstern , Mourya , Okumuş , Pott-Junior , Seet , Shahbaznejad , Shouman ,Spoorthi , Szente Fonseca , Vallejos , Zubair ] .A Merck tem vários conflitos de interesse:
•A Merck se comprometeu a distribuir ivermectina gratuitamente
“tanto quanto necessário, pelo tempo que for necessário” no Programa de Doação de Mectizan®
[ Merck (B) ] , para ajudar a eliminar a oncocercose.
•A Merck tem seus próprios novos tratamentos COVID-19 MK-7110 (anteriormente CD24Fc)
[ Adams ] e Molnupiravir (MK-4482)
[ Jayk Bernal , Wikipedia ] . A Merck tem um acordo de ~$US1.2B para fornecer molnupiravir ao governo dos EUA, se receber EUA ou aprovação
[ Khan (B) ] . Mais de US$ 10 bilhões em pedidos de curto prazo são esperados se aprovados
[ Genetic Engineering and Biotechnology News ] .
•A ivermectina não está patenteada, existem muitos fabricantes e é improvável que a Merck consiga competir com fabricantes de baixo custo.
•Promover o uso de medicamentos não patenteados de baixo custo em relação a novos produtos pode ser indesejável para alguns acionistas.
•O Japão solicitou que a Merck realizasse testes clínicos no início da pandemia e eles recusaram. A Merck pode estar relutante em admitir esse erro
[ Yagisawa ] .Para outras preocupações com relação à declaração da Merck e ações anteriores relacionadas ao Vioxx, consulte
[ Scheim ] .Análise FDA.A FDA dos EUA recomendou contra a ivermectina em 5 de março de 2021, no entanto, eles afirmaram que
“A FDA não revisou dados para apoiar o uso de ivermectina em pacientes com COVID-19 para tratar ou prevenir a COVID-19” . Ainda não há indicação de que o FDA revisou os ensaios clínicos
465 dias depois.A FDA observa que eles
“receberam vários relatórios de pacientes que precisaram de suporte médico e foram hospitalizados após se automedicarem com ivermectina destinada a cavalos” . O número de relatórios foi 4
[ Pfeiffer ] . Para comparação, a overdose de acetaminofeno resulta em ~33.000 hospitalizações anuais nos EUA (~12.000 não intencionais)
[ Charilaou ] . A recomendação do FDA pode aumentar os casos de automedicação com ivermectina animal, pois reduz o percentual de médicos prescritores.Eles afirmam que
“Ivermectina não é um anti-viral” , no entanto muitos estudos contradizem isso
[ Ahmed , Aref , Babalola , Biber , Bukhari , Buonfrate , Caly , Chowdhury , Elalfy , Espitia-Hernandez , Khan , Mahmud , Mohan , Mourya , Okumuş , Rezk , Thairu ] , incluindo 10 ECRs.Eles observam que
“algumas pesquisas iniciais estão em andamento” , no entanto, muitos estudos foram concluídos e publicados antes da recomendação da FDA
[ Ahmed , Alam , Babalola , Behera , Beltran Gonzalez , Bernigaud , Biber , Budhiraja , Bukhari , Cadegiani , Camprubí , Carvallo (C) , Chaccour (B) , Chachar , Chahla (B) , Chowdhury , Elalfy , Espitia-Hernandez ,Ghauri , Gorial , Hashim , Hellwig , Khan , Lima-Morales , López-Medina , Mahmud , Mohan , Okumuş , Podder , Rajter , Ravikirti (B) , Shouman , Spoorthi ] , incluindo 17 ECRs.
3 de setembro de 2021 : A FDA revisou ligeiramente sua declaração. Eles removeram a falsa alegação de que a invermectina não é um antiviral e removeram a declaração de que não revisaram os dados. No entanto, ainda não há nada que indique que eles revisaram os ensaios clínicos. De fato, eles afirmam que “os dados atualmente disponíveis não mostram que a ivermectina é eficaz contra o COVID-19” e “a ivermectina não se mostrou segura ou eficaz para essas indicações”, ambas falsas.Análise do NIH.
Atualização: O NIH atualizou a recomendação, baseada fortemente no Together Trial, sem mencionar os dados impossíveis, cegamento, randomização e falhas de protocolo , ou que o co-investigador principal relatou em particular que “Há um sinal claro de que o IVM funciona em pacientes com COVID”.O NIH relatou que não há evidências suficientes para recomendar a favor ou contra a ivermectina
[ NIH ] . Uma tabela com resumos de 7 estudos é fornecida, datada de 16 de dezembro de 2021, e eles fazem referência a outros 23 estudos sem análise, porém existem 85 estudos até o momento. Nenhuma análise quantitativa é fornecida. A recomendação do NIH é “evidência insuficiente”, indicando que eles devem revisar novas evidências imediatamente. A falta de atualizações sugere viés.Os prováveis membros do painel foram revelados por pedidos da FOIA
[ Yim (B) ] . Na primeira solicitação, todos os nomes de membros, exceto dois, foram editados
[ drive.google.com ] , mas todos estão visíveis em uma segunda solicitação
[ drive.google.com (B) ] . Grandes conflitos de interesse foram relatados
[ trialsitenews.com , Yim (B) ] . 7 dos 9 membros do painel parecem ter conflitos de interesse.
Enviar correções ou atualizações
| Profa. Adaora Adimora(adimora@med.unc.edu) | •Merck : conselho consultivo, consultor, apoio à pesquisa [ covid19treatmentguidelines.nih.gov , trialsitenews.com (B) ]•Gilead (fabricante do remdesivir): consultor, apoio à pesquisa [ files.covid19treatmentguidelines.nih.gov , tandfonline.com ] “Aadimora AA recebeu honorários de consultoria da Viiv, e Gilead e sua instituição receberam financiamento da Gilead para sua pesquisa”•Open Payments mostra US$ 62.000 da Merck e US$ 88.000 da Gilead [ openpaymentsdata.cms.gov (B) ] |
| Prof. Roger Bedimo(roger.bedimo@va.gov) | •Merck : conselho consultivo [ covid19treatmentguidelines.nih.gov , trialsitenews.com (B) ]•Gilead : honorários [ files.covid19treatmentguidelines.nih.gov ]•Open Payments mostra US$ 149.000 da Merck , US$ 76.000 da Sanofi e US$ 23.000 da Gilead [ openpaymentsdata.cms.gov (C) ] |
| Prof. Rajesh Gandhi(rgandhi@mgh.harvard.edu) | •Gilead : subsídios, conselho consultivo, honorários pessoais [ nejm.org , rmed.acponline.org ] “Dr. Gandhi relata subsídios e honorários pessoais da Gilead, honorários pessoais da Merck, subsídios e honorários pessoais da Theratechnologies, subsídios da ViiV, subsídios da Janssen.”•Merck : conselho consultivo e honorários pessoais [ files.covid19treatmentguidelines.nih.gov , nejm.org , rmed.acponline.org ]•Janssen : concessões [ nejm.org ]•Open Payments mostra US$ 45.000 da Merck e US$ 10.000 da Gilead [ openpaymentsdata.cms.gov (D) ] |
| Prof. David Glidden(david.glidden@ucsf.edu) | •Merck : conselho consultivo [ covid19treatmentguidelines.nih.gov , trialsitenews.com (B) ]•Gilead : consultor [ covid19treatmentguidelines.nih.gov , files.covid19treatmentguidelines.nih.gov ] |
| Prof. Roy Gulick(rgulick@med.cornell.edu) | •Merck : grants [ web.archive.org ] (excluído da versão atual [ medscape.org ] ) “Roy M. Gulick, MD, MPH, revelou que recebeu doações para pesquisa clínica da Abbott, Boehringer Ingelheim, Merck, Pfizer , Schering e Tibotec, e recebeu doações para atividades educacionais da Gilead e Monogram. O Dr. Gulick também revelou que atuou como consultor ad hoc para Abbott, Boehringer Ingelheim, Bristol-Myers Squibb, Gilead, GlaxoSmithKline , Pfizer, Schering e Tibotec” , investigador principal do A5391 com financiamento em parte da Merck [ actgnetwork.org ]•Pfizer : subvenções e consultor ou consultor ad-hoc [ web.archive.org ] (excluído da versão atual [ medscape.org ]•Gilead : subsídios e conselheiro ou consultor ad-hoc [ web.archive.org ] (excluído da versão atual [ medscape.org ]•GlaxoSmithKline : consultor ou consultor ad-hoc [ web.archive.org ] (excluído da versão atual [ medscape.org ]•NIAID/NIH : bolsas [ acpjournals.org , vivo.weill.cornell.edu ] |
| Profª Susanna Naggie(susanna.naggie@duke.edu) | •Gilead : subsídios, apoio para viagens/reuniões [ covid19treatmentguidelines.nih.gov , files.covid19treatmentguidelines.nih.gov , rmed.acponline.org ]•AbbVie, NIH : concessões [ rmed.acponline.org ]•Vir Biotechnology : conselho consultivo, acionista [ covid19treatmentguidelines.nih.gov ]•Subsídio experimental de ivermectina : subsídio de US$ 155 milhões após a recomendação de evidências insuficientes [ trialsitenews.com (B) ]•Open Payments mostra US$ 2,4 milhões da AbbVie, US$ 1,2 milhão da Gilead , US$ 34.000 da Janssen e US$ 19.000 da Merck [ openpaymentsdata.cms.gov (E) ] |
| Prof. André Pavia(andy.pavia@hsc.utah.edu) | •Merck : consultor [ files.covid19treatmentguidelines.nih.gov , rmed.acponline.org ]•Genentech : consultor [ files.covid19treatmentguidelines.nih.gov ]•GlaxoSmithKline : consultor [ rmed.acponline.org ]•Open Payments mostra $ 14.000 da Pfizer , $ 5.000 da Merck e $ 4.000 da Janssen [ openpaymentsdata.cms.gov (F) ] |
ConclusãoA ivermectina é um tratamento eficaz para o COVID-19. O tratamento é mais eficaz quando usado precocemente. A meta-análise usando o desfecho mais grave mostra 63%
[52-71%] e 83%
[74-89%] de melhora para
tratamento e profilaxia precoces , com resultados semelhantes após
análise de sensibilidade baseada em exclusão , para
desfechos primários , para
estudos revisados por pares , e para
ECRs . Melhorias estatisticamente significativas são observadas para
casos e
depuração viral . Todos permanecem significativos após as
exclusões . 55 estudos de 50 equipes independentes em 22 países diferentes mostram melhorias estatisticamente significativas isoladamente (39 para resultados primários e 36 para o resultado mais grave). Os resultados são muito robustos — na análise de sensibilidade de exclusão de pior caso, 54 de 85 estudos devem ser excluídos para evitar encontrar eficácia estatisticamente significativa.Respostas
Metanálises inconclusivas.[ Popp , Roman ] fornecem meta-análises que mostram efeitos positivos sem atingir significância estatística. Os principais métodos usados que resultam em falta de significância estatística são a exclusão da maioria da base de evidências e a divisão do subconjunto restante. Para mais detalhes, consulte as
Análise de resultado primário.Usamos a extração de efeito pré-especificado fixo para evitar viés e focar nos resultados clinicamente mais relevantes. Para comparação, também realizamos análises usando o resultado primário dos estudos (mostrado nos
dados suplementares), com resultados mostrando tamanhos de efeito semelhantes. Os resultados da profilaxia são muito semelhantes com 100% (16 de 16) efeitos positivos. O tratamento precoce mostra 94% (31 de 33) de efeitos positivos, melhorados devido à contagem de eventos muito pequena, os resultados graves negativos em Krolewiecki, Vallejos e Buonfrate não têm mais prioridade. O tratamento tardio mostra 72% (26 de 36) efeitos positivos, ligeiramente reduzidos, principalmente devido aos resultados da eliminação viral serem o resultado primário em alguns estudos, e a eliminação viral ser menos bem sucedida com o tratamento tardio. No geral, a análise do resultado primário mostra 86% (73 de 85) efeitos positivos, em comparação com 85% (72 de 85) na análise do protocolo principal.
A meta-análise não deve combinar estudos heterogêneos.Todas as meta-análises combinam estudos heterogêneos, porque todos os estudos diferem de uma ou mais maneiras, incluindo dados demográficos do paciente, distribuição de atraso no tratamento, efeito medido, variantes de SARS-CoV-2 e regimes de tratamento (observe que isso é diferente da heterogeneidade causada por viés) . A combinação de estudos heterogêneos pode obscurecer a eficácia – por exemplo, se o tratamento em 24 horas for duas vezes mais eficaz que o tratamento em 48 horas e incluirmos estudos com tratamento posterior; ou se um tratamento é eficaz na redução da mortalidade, mas não tem efeito na depuração viral e incluímos estudos de depuração viral. A inclusão de estudos mais distantes da situação de tratamento ideal reduzirá o tamanho do efeito observado. Isso pode ser visto na análise do atraso do tratamento – o tratamento tardio é menos eficaz e a inclusão de estudos de tratamento tardio reduz o tamanho do efeito. Para qualquer meta-análise negativa, devemos considerar se o tratamento é eficaz, mas apenas em um subconjunto das situações cobertas pelos estudos (ou uma situação não coberta por nenhum estudo, por exemplo, poucos tratamentos têm estudos com atraso de tratamento <= 24 horas ).
Resposta da BBC.Atualização: os autores indicaram que seus dados estariam disponíveis “em breve” a partir de 14 de setembro de 2021, no entanto, não foram divulgados mais de 271 dias depois, portanto, não é possível analisar seus métodos em relação à pesquisa de ivermectina em detalhes. No entanto, o Dr. Sheldrick postou acusações falsas e difamatórias sobre um médico altamente respeitado que salvou inúmeras vidas antes e durante a pandemia. Nesse caso, métodos detalhados foram publicados, revelando uma análise altamente falha e um mal-entendido básico das estatísticas, conforme detalhado por vários estatísticos [ Fenton , twitter.com (C) ] . O autor excluiu a postagem do blog e tornou sua conta do Twitter privada. Além disso, notamos que o descaso da equipe por grandes problemas com oJuntos , López-Medina et al. , e Beltran Gonzalez et al. sugerem um viés substancial.Um artigo da BBC levanta questões devido a problemas de dados em alguns estudos, com base em uma análise de uma equipe de pesquisadores. Um dos pesquisadores relata que os dados em alguns ensaios podem ter sido manipulados, embora observe que o erro humano não pode ser descartado. Outros membros da equipe acusam diretamente os autores de má conduta. Independentemente da causa, a preocupação com esses estudos é válida. Atualmente, 2 estudos foram retirados, um foi retirado por um servidor de pré-impressão e outro foi relatado como pendente de retratação, embora o periódico relate que nenhuma retratação está pendente. Nenhum desses estudos está em nossa análise.A existência de alguns estudos de qualidade inferior é típica em grandes bases de evidências. A porcentagem de estudos com problemas não é maior do que as médias relatadas e não está perto de remover evidências de eficácia (e pode realmente melhorar as evidências conforme detalhado abaixo). Realizamos uma análise de sensibilidade absoluta de pior caso, onde os estudos positivos são excluídos em ordem de tamanho do efeito, com o maior efeito primeiro.
64%, ou 54 de 85 estudos devem ser excluídos para evitar encontrar eficácia estatisticamente significativa (isto é, além dos quatro artigos que não estão nesta análise).As estatísticas resumidas da meta-análise necessariamente obscurecem a maioria das informações na base de evidências. Para aqueles que leram toda a pesquisa, o conhecimento da eficácia é apoiado por extensas informações adicionais, incluindo, por exemplo, relações entre resultados dentro de um estudo, relações dose-resposta dentro e entre estudos, relações atraso-eficácia do tratamento dentro e entre estudos, variante -relações de eficácia, etc. Notavelmente, a remoção de Elgazzar, Samaha e Niaee melhora as relações atraso-eficácia e dose-resposta e pode aumentar ainda mais a confiança ao considerar todas as informações.Preocupações sobre
[ Cadegiani , Carvallo , Carvallo (B) , Carvallo (C) ] também foram relatadas. Todos esses estudos são excluídos em nossa análise de exclusão.
| Estudos | Profilaxia | Tratamento precoce | Tratamento tardio | Pacientes | Autores | |
| Com exclusões GMK/BBC | 58 | 82% [68-89%] | 69% [61-76%] | 53% [33-68%] | 116.680 | 632 |
| RCTs com GMK/BBC exc. | 30 | 84% [25-96%] | 66% [54-75%] | 29% [4-47%] | 6.706 | 370 |
| Melhoria percentual com tratamento com ivermectina após a exclusão de todos os estudos relatados por esta equipe |
Observamos que, embora a má conduta não possa ser descartada, as preocupações relatadas também podem ser causadas por erros de digitação, erros de coleta de dados que não afetam os resultados analisados e resultados esperados de vários testes. Os autores, sem nenhum registro prévio ou plano de análise estatística, realizam milhares de testes estatísticos nos dados dos estudos e relatam os resultados sem corrigir vários testes. Por exemplo, relatar a ocorrência de um evento de 1 em 1.000 como evidência de falha de randomização, ao realizar mais do que esse número de testes em todos os estudos.Esse grupo muitas vezes descarta estudos com base em um limiar de significância estatística arbitrária para um resultado específico, um mal-entendido de estatísticas
[ Amrhein ] e indefensável como um pré-filtro na meta-análise.Este grupo fez muitas alegações não suportadas pelos dados. Para Niaee, um autor afirmou que o estudo
“fez uma enorme diferença” . Não tem efeito no tratamento precoce ou profilaxia. Para o tratamento tardio, que não é recomendado, a mudança foi relativamente pequena. Para Elgazzar, o autor afirmou que poderia ser
“a fraude médica mais conseqüente já cometida” . Quase não houve diferença em nossa análise após a remoção deste artigo (excluir 1 de 88 estudos tem muito pouco efeito, e a exclusão realmente melhora a relação atraso-resposta do tratamento).As declarações do grupo sugerem um viés significativo. O autor principal se referiu pela primeira vez à ivermectina como “algo mais para desmascarar” em dezembro de 2020 e, mais tarde, como um “vermífugo de cavalos”. Outro membro do grupo pediu que os cientistas que recomendam a vitamina D sejam acusados de
“crimes contra a humanidade” .O grupo fez reivindicações sobre todas as evidências de ivermectina com base na existência de alguns estudos com problemas. É inapropriado generalizar sobre todo o grupo de 852 cientistas e pesquisadores com base nos erros ou ações de alguns indivíduos.Este grupo se concentrou em encontrar problemas em artigos que relatam grandes efeitos positivos, o que introduz um viés significativo. Notavelmente, os poucos estudos que mais contribuem para minimizar os efeitos na meta-análise incluem estudos com conflitos de interesse muito altos e muitas violações de protocolo e problemas de dados relatados, no entanto, esse grupo desconsidera todas essas questões.O artigo afirma que
“O maior e mais alto estudo de ivermectina publicado até agora é o ensaio Together”, que
“não encontrou nenhum benefício” , no entanto, este estudo não foi publicado, é um dos
ensaios de menor qualidade com muitos projetos, execução e análise documentados questões , tem conflitos de interesse extremamente altos, há um histórico de
relatórios imprecisos antes da publicação para um tratamento anterior no mesmo estudo, e o estudo realmente relatou uma mortalidade 18% menor (sem significância estatística).O artigo relata que 26 estudos foram examinados, no entanto, existem 88 estudos, os autores não relataram seus resultados para todos os 26 e os autores não forneceram seus dados após solicitações repetidas. Atualmente, eles nem forneceram uma lista dos 26 estudos.O grupo tem um foco excessivo em ECRs, que têm um viés fundamental contra encontrar um efeito para intervenções como a ivermectina que são amplamente conhecidas e facilmente disponíveis – pacientes que acreditam que precisam de tratamento são mais propensos a recusar a participação e fazer o tratamento
[ Yeh ] ( isso não se aplica ao teste farmacêutico típico de um novo medicamento que de outra forma não está disponível e não é familiar).O principal autor do grupo também é contra a vitamina D. Dos 81 estudos de tratamento com vitamina D COVID-19, o autor sugere que apenas um estudo vale a pena ser analisado
[ Murai ] . Isso nos dá um caso simples para examinar o viés potencial.
[ Murai ] é um pequeno ensaio que não fornece efeitos estatisticamente significativos (mortalidade
p = 0,43, outros resultados são positivos, mas também não significativos). O autor reconhece que o estudo é muito pequeno para uma conclusão. Mais importante, este estudo não fornece informações sobre se a vitamina D reduz o risco de um caso grave de COVID-19, porque os pacientes neste estudo já tinham um caso grave de COVID-19 (90% já em tratamento com oxigênio na linha de base). O autor não menciona isso. O estudo também tem braços mal pareados em termos de gênero, etnia, hipertensão, diabetes e ventilação basal, todos favorecendo o grupo controle. Além disso, este estudo usa uma forma inadequada de vitamina D – colecalciferol. Na realidade, os médicos usariam calcifediol ou calcitriol com tratamento em estágio avançado, porque evitam um atraso muito grande para a conversão. Não temos conhecimento de uma razão para usar colecalciferol neste caso (além de produzir um resultado nulo). Em resumo, o estudo escolhido pelo autor é o estudo que fornece as informações menos úteis dos 81 estudos de tratamento com vitamina D até o momento, sugerindo uma análise tendenciosa.Apoiamos totalmente o esforço desta equipe para limpar a base de evidências. Isso é extremamente valioso e melhora a integridade da base de evidências (e a precisão se feita igualmente para todos os estudos). Esperamos que esta ou outras equipes possam fazer o mesmo para todos os tratamentos. No entanto, o plano de análise deve ser publicado, os detalhes de todos os testes devem ser fornecidos, os resultados devem ser corrigidos para vários testes, os resultados de todos os estudos e testes devem ser fornecidos e a mesma atenção deve ser dada a estudos com resultados não estatisticamente significativos, especialmente aqueles com grandes problemas de dados relatados que foram desconsiderados por esta equipe (por exemplo, dados que sugerem violações substanciais do protocolo, incluindo confusão por tempo em
[ Reis ] e uso do braço de controle de tratamentos em
[López-Medina ] ).Para a cobertura de outros erros no artigo da BBC, e iluminação do forte contraste entre a resposta do Dr. Lawrie à BBC antes da publicação e o que eles escolheram para relatar, veja
[ BiRD Group , Campbell , Elijah , Lawrie (B) ] .Mais detalhes podem ser encontrados na resposta a seguir sobre o autor principal deste grupo.
Resposta GMK.Atualização: a GMK indicou que seus dados seriam divulgados “em breve” a partir de 14 de setembro de 2021, mas não foram divulgados mais de 271 dias depois. Além disso, notamos que o desrespeito da GMK por questões importantes com o Together Trial , López-Medina et al. , e Beltran Gonzalez et al. sugerem um viés substancial.Declarações incorretas, enganosas, hiperbólicas e sem suporte foram feitas por uma influente personalidade anti-tratamento do Twitter, jornalista e estudante de doutorado conhecida por
defender o Monsanto Roundup contra alegações cancerígenas (mais tarde liquidado por US $ 11 bilhões). O autor é notável como o único pesquisador conhecido que relata ter lido a maioria dos 88 estudos (incluindo retratados), mas não considera a evidência positiva. No entanto, sua opinião parece ter sido formada antes de ler os estudos – eles primeiro se referiram à ivermectina como
“algo mais para desmascarar”. Observamos que o autor fez contribuições valiosas identificando problemas significativos com alguns estudos, o que ajudou a melhorar a qualidade da base de evidências da ivermectina e melhorou as relações dose-resposta e tratamento atraso-resposta.A análise com as exclusões recomendadas pela GMK pode ser encontrada nos
dados complementares , que mostram 45%
[29-57%] de melhora,
p = 0,0000051.O autor foi pago para escrever artigos anti-tratamento e também se referiu à ivermectina como um
“vermífugo de cavalos” . O autor passou por uma tragédia pessoal com vários membros da família que morreram de COVID-19, o que pode introduzir um viés contra o reconhecimento de erros no aconselhamento de tratamento.A tentativa do autor de desacreditar a pesquisa com ivermectina centra-se na afirmação fundamentalmente falsa de que a exclusão de um pequeno número de ensaios de qualidade inferior resulta em um resultado negativo. Deve ficar claro a partir da parcela da floresta que isso não é possível, mas podemos ser mais específicos. Realizamos uma análise de sensibilidade de pior caso, onde os estudos positivos são excluídos em ordem de tamanho do efeito, com o maior efeito primeiro. Quantos estudos precisamos excluir antes que a meta-análise RR tenha um intervalo de confiança superior a 1,0?
64%, ou 54 de 85 estudos devem ser excluídos para evitar encontrar eficácia estatisticamente significativa.Tal como acontece com todos os dados neste documento, esta análise será atualizada automaticamente à medida que a base de evidências evoluir. Observe também que isso ocorre após a exclusão de artigos retirados – um nunca esteve nesta análise, o segundo foi removido no mesmo dia em que foi retirado e os outros dois foram removidos antes da retratação com base na notificação do autor de que a retratação está pendente ( apenas um foi retratado, a revista de Niaee et al.O autor afirma que incluímos vários artigos que já foram excluídos nas 10 análises de exclusão.Autor afirma que há uma porcentagem maior de estudos de baixa qualidade para ivermectina e COVID-19 em comparação com outros tratamentos. Isso não é suportado para uma base de evidências tão grande e não corresponde a estudos anteriores.O autor muitas vezes comete um erro básico ao igualar efeitos positivos que não são estatisticamente significativos em um nível específico com “nenhum efeito”, um mal-entendido das estatísticas
[ Amrhein ] . Por exemplo, se um estudo relata 50% de melhora com um valor de
p de 0,1, não podemos dizer que o estudo mostra que o tratamento é ineficaz ou, nas palavras do autor, não mostra “nenhum benefício”. O autor repetidamente faz alegações falsas dessa maneira.Em 14 de setembro de 2021, o autor indicou que sua equipe havia revisado cerca de 30 estudos de ivermectina e seus dados estariam disponíveis em breve, mas não foram divulgados oito meses depois.O autor parece favorecer estudos afiliados/operados por empresas farmacêuticas. Por exemplo, o autor não tem problemas com a falta de IPD para muitos ensaios farmacêuticos COVID-19 afiliados que apoiam as posições de tratamento do autor, mas considera problemática a falta de IPD em um ensaio positivo de ivermectina. O autor acredita que o Together Trial, afiliado à indústria farmacêutica, é o estudo da mais alta qualidade até agora, mas não apenas os autores se recusaram a liberar o IPD que prometeram liberar anteriormente, como também não havia uma pré-impressão quando a GMK fez a declaração, e o estudo tem
muitos pontos críticos . e falhas graves , conflitos de interesse extremamente altos e um histórico de
relatórios imprecisosantes da publicação para outro braço de tratamento. A GMK publicou posteriormente um artigo com um dos co-líderes originais do Together Trial (que mais tarde se juntou ao julgamento DSMC).O autor desconsidera o atraso do tratamento na análise, o que resulta em conclusões incorretas. Por exemplo, o autor afirma que o estudo RECOVERY provou que outro tratamento não é eficaz e forneceria dados definitivos se o mesmo fosse feito para a ivermectina. O estudo forneceu dados valiosos sobre o uso muito tardio (9 dias após os sintomas) com uma dose excessivamente alta e pacientes em estágio muito avançado. No entanto, não forneceu informações sobre o tratamento precoce. O oseltamivir, por exemplo, geralmente só é considerado eficaz para influenza quando usado dentro de 0-36 ou 0-48 horas
[ McLean , Treanor ]. Paxlovid foi testado com um máximo de 3 dias a partir do início dos sintomas (o atraso médio é desconhecido). Para a ivermectina, o autor acredita que o estudo PRINCIPLE fornecerá dados sólidos sobre a eficácia, no entanto, este estudo inclui pacientes de baixo risco com menos de 15 dias do início dos sintomas e pode fornecer apenas informações sobre o tratamento tardio em uma população de baixo risco.
A Figura 28 mostra uma meta-regressão de efeitos mistos para eficácia em função do atraso no tratamento em estudos de COVID-19 de
42 tratamentos . A eficácia diminui rapidamente com o atraso do tratamento.Os resultados tardios do tratamentonão são representativos
Figura 28. A GMK acredita que os resultados para o tratamento com atraso de 9 dias desde o início dos sintomas fornecem informações definitivas sobre a eficácia do tratamento, no entanto, o tratamento precoce é conhecido por ser crítico para os antivirais, conforme confirmado pela meta-regressão de estudos de
O autor tem um foco injustificado em um resultado específico (mortalidade) e um subconjunto específico de ensaios (ECRs). Isso seria razoável em muitos casos quando dados suficientes de alta qualidade estivessem disponíveis, no entanto, esse não é o caso de ensaios de tratamento com COVID-19 sem patente, em que os ECRs geralmente envolvem atraso no tratamento, pacientes de baixo risco onde a mortalidade é rara ou muito altos conflitos de interesse. Tratamentos amplamente aceitos e eficazes (para variantes específicas) como casirivimab/imdevimab, bamlanivimab e sotrovimab foram todos aprovados sem benefícios de mortalidade estatisticamente significativos. Outros resultados também são importantes – acelerar a eliminação viral e reduzir casos, hospitalização, admissão em UTI, ventilação etc. e reduzindo a carga sobre o sistema de saúde. Esses resultados também provavelmente se correlacionam com a redução da mortalidade entre populações maiores ou de maior risco. Observamos que há extensa evidência para o desfecho mortalidade quando não se restringe a ECRs. Os ECRs foram realizados principalmente com populações de risco relativamente baixo, onde a mortalidade é baixa, levando a uma significância estatística limitada. No entanto, os ECRs são inerentemente tendenciosos para a baixa mortalidade e para não encontrar um efeito neste caso – a ivermectina é conhecida por ser benéfica para o COVID-19 e está facilmente disponível, portanto, os participantes que acreditam que podem estar em sério risco têm maior probabilidade de diminuir participação no ECR e tomar os medicamentos recomendados. Os pacientes que optam por participar também são mais propensos a ter baixa adesão.O autor sugere que escolhemos o resultado errado em alguns casos. Embora erros sejam possíveis, por exemplo, corrigimos erros com
Jain et ai. , as alegações feitas sugerem que o autor não leu os estudos e/ou nosso protocolo com atenção. Os detalhes estão abaixo. Observamos que o autor desconsidera a existência das
análises de desfechos individuais e a análise
de desfechos primários .A maioria dos erros não foi corrigida mais de dez meses depois. Muitas declarações falsas, enganosas e difamatórias continuam disponíveis, altamente classificadas nos resultados de pesquisa e altamente influentes. Outros erros incluem:
•que excluindo Elgazzar et al. altera completamente os resultados e pode ser
“a fraude médica mais conseqüente já cometida” . A exclusão de 1 de 88 estudos tem muito pouco efeito, e a exclusão melhora a relação atraso-resposta do tratamento.
•que Niae et al.
“fez uma enorme diferença” . Não tem efeito no tratamento precoce ou profilaxia. Para o tratamento tardio, que não é recomendado, a mudança foi relativamente pequena, e a exclusão melhora a relação atraso-resposta do tratamento.
•cometer erros básicos sugerindo uma leitura muito superficial dos estudos, por exemplo, alegar que o RR em Szente Fonseca é o risco de ser tratado.
•cometer erros básicos sugerindo uma leitura muito superficial deste artigo, por exemplo, alegar que um resultado para estudos de profilaxia é baseado no número de pacientes de todos os estudos.
•equiparar um alto grau de COVID-19 em um país que adota parcialmente um tratamento com falta de eficácia, desconsiderando fatores de confusão óbvios, como áreas fortemente afetadas sendo mais propensas a adotar o tratamento (análise de resultados em regiões ou períodos de tempo que adotam o tratamento, embora não equivalentes para estudos controlados, é mais informativo e mostra eficácia
[ Chamie-Quintero , Chamie-Quintero (B) , Merino , Ontai ] ).
•heterogeneidade confusa devido à dose, atraso no tratamento, etc. e devido ao viés.
•desconsiderando o atraso do tratamento para diluir ou obscurecer os efeitos incluindo o tratamento tardio (o autor também usou este método com outros tratamentos).
•desconsiderando a existência de análises de resultados específicos, análise de ECR e análise de sensibilidade baseada em exclusão.
•sugerindo que a eficácia por períodos mais longos não é possível porque a ivermectina tem uma meia-vida de
“cerca de um dia” . O autor desconsidera a eficácia conhecida para outras condições por períodos muito mais longos e descaracteriza a meia-vida. A eficácia antiparasitária pode persistir por vários meses após uma dose única
[ Canga ] . A meia-vida plasmática é mais longa em alguns estudos, e uma concentração plasmática significativa pode persistir por mais de 2 semanas em alguns pacientes
[ Muñoz ] . Mais importante, a ivermectina é altamente lipofílica e pode se acumular no pulmão e em outros tecidos onde as concentrações podem ser muitas vezes maiores
[ Chaccour (C) , Chiu ] .
•mal-entendido análise de enredo de funil e explicações que não sejam relatórios seletivos (e não fornecendo evidências de estudos negativos não relatados, enquanto há evidências substanciais de dificuldade em publicar estudos positivos
[ Jerusalém Post , Kory (B) ] ).
•sugerindo que é impossível combinar evidências de mortalidade e hospitalização (por exemplo), mas combinar tratamento tardio e tratamento precoce para obscurecer a eficácia (se um tratamento reduz a gravidade da doença exigindo hospitalização, a mortalidade reduzida em populações de risco segue logicamente, enquanto a falta de eficácia vários dias após o início não pode ser extrapolada para o tratamento precoce – os tratamentos para uma infecção viral geralmente são menos eficazes quando atrasados).
•fazer alegações sérias sobre estudos individuais sem entrar em contato com os autores (por exemplo, alegar que os pacientes foram excluídos por atingir o desfecho muito rapidamente em um estudo, enquanto os autores relatam exclusões devido ao status negativo inicial).
•O autor não tem conhecimento de diferentes variantes, sugerindo que os resultados devem ser idênticos para o tratamento em um determinado atraso, mesmo quando as variantes predominantes têm carga viral de pico, tempo para carga viral de pico
[ Faria , Karita , Nonaka ] marcadamente diferentes e mortalidade (por exemplo Gama vs. não Gama aHR 4,73 [1,15-19,41]
[ Zavascki ] ).Os casos em que o autor sugere que escolhemos o resultado errado indicam que o autor não leu os estudos e/ou nosso protocolo com atenção:
•sugerindo que o risco de um bom resultado deve ser usado seletivamente em vez do risco de um mau resultado (o autor gostaria de fazer isso quando reduz o tamanho do efeito). Isso é semelhante a usar o risco de sobrevivência em vez do risco de morte. A sobrevivência de 99% pode ser apenas uma melhoria de 4% sobre a sobrevivência de 95%, mas a maioria das pessoas apreciaria o risco de morte 80% menor.
•sugerindo que o tempo de internação deve ser utilizado para recuperação sintomática em um estudo em que a alta é baseada na eliminação viral (e testada apenas semanalmente).
•sugerindo que um sintoma específico como tosse deve ser usado (o autor preferiria um resultado menos positivo para o estudo).
•sugerindo que a carga viral é mais importante do que os resultados sintomáticos.
•sugerindo que a mortalidade deve ser usada em populações com mortalidade zero (para populações de baixo risco sem mortalidade, a redução da mortalidade não é possível, isso não significa que a redução da hospitalização, por exemplo, não seja valiosa).
•sugerindo que os resultados não ajustados devem ser usados em um estudo em que os ajustes claramente fazem uma diferença significativa (o autor deseja selecionar os resultados da tosse não ajustados).
•sugerindo que, por exemplo, em um estudo de carga viral em que todos os pacientes se recuperam, não é valioso se os pacientes tratados se recuperarem mais rapidamente (ou forem menos propensos a transmitir o vírus a outras pessoas).
•sugerindo que os resultados selecionados do estudo devem ter prioridade em vez de usar um protocolo pré-especificado consistente, desconsiderando o viés adicionado e o fato de que isso realmente melhora os resultados para a ivermectina (por exemplo, a contagem de eventos muito pequenos resultados graves negativos em Krolewiecki, Vallejos e Buonfrate deixaria de ter prioridade).
•sugerindo que a tosse é um sintoma mais importante do que a baixa SpO
2 ou febre. A tosse pode persistir por um longo tempo após a resolução dos sintomas mais graves, e a tosse persistente pode ser causada por muitas condições.
•sugerindo que os resultados do tratamento com baixa dose combinada devem ser usados em um estudo que teve um braço combinado de ivermectina/doxiciclina (dose única de ivermectina, 5 dias de doxiclina) e um braço de ivermectina com tratamento por 5 dias.Observamos que essa personalidade tem um extenso histórico de conselhos incorretos, incluindo, por exemplo:
•alegando que a gripe é mais perigosa que o COVID-19
•alegando que o SARS-CoV-2 não é transportado pelo ar
•alegando que é impossível melhorar o funcionamento do sistema imunológico
•mesmo acreditando e propagando uma história inventada que alegava que a overdose de ivermectina estava fazendo com que as vítimas de tiros esperassem em um pronto-socorroO autor assumiu uma posição pública contra os primeiros tratamentos para COVID-19 desde pelo menos julho de 2020. Dada essa posição negativa de longa data e influente, eles podem tender a visualizar informações com um filtro negativo e viés de confirmação e podem relutar em admitir erros. Eles reconhecem não ter lido todos os estudos (e parecem ter lido outros muito superficialmente). Eles enviaram zero feedback para nós, sugerindo que eles sabem que seus comentários estão incorretos ou que eles têm outra motivação além de corrigir erros. O autor afirma que não conseguiu entrar em contato conosco, no entanto, existem mais de 50 links de feedback ao longo deste artigo. Também observamos que o autor não está aberto a comentários críticos e bloqueia rotineiramente os usuários do Twitter corrigindo erros ou expressando algo crítico em seu feed. Os relatórios sugerem que o autor também bloqueia preventivamente pessoas que nem interagiram com eles, mas estão conectadas a outros usuários relatando seus erros. O autor reconhece o uso de uma ferramenta chamada MegaBlock que bloqueia todas as pessoas que curtiram um tweet específico.O autor também é contra a vitamina D. Dos 81 estudos de tratamento com vitamina D COVID-19, o autor sugere que apenas um estudo vale a pena ser analisado
[ Murai ] . Isso nos dá um caso simples para examinar o viés potencial.
[ Murai ] é um pequeno ensaio que não fornece efeitos estatisticamente significativos (mortalidade
p = 0,43, outros resultados são positivos, mas também não significativos). O autor reconhece que o estudo é muito pequeno para uma conclusão. Mais importante, este estudo não fornece informações sobre se a vitamina D reduz o risco de um caso grave de COVID-19, porque os pacientes neste estudo já tinham um caso grave de COVID-19 (90% já em tratamento com oxigênio na linha de base). O autor não menciona isso. O estudo também tem braços mal pareados em termos de gênero, etnia, hipertensão, diabetes e ventilação basal, todos favorecendo o grupo controle. Além disso, este estudo usa uma forma inadequada de vitamina D – colecalciferol. Na realidade, os médicos usariam calcifediol ou calcitriol com tratamento em estágio avançado, porque evitam um atraso muito grande para a conversão. Não temos conhecimento de uma razão para usar colecalciferol neste caso (além de produzir um resultado nulo). Em resumo, o estudo escolhido pelo autor é aquele que fornece as informações menos úteis dos 81 estudos até o momento, sugerindo uma análise tendenciosa.Com base em muitos comentários, o autor parece se concentrar em critérios superficiais, como composição e qualidade da escrita. Embora muitos dos estudos tenham sido realizados por falantes não nativos de inglês com orçamentos mínimos, isso não significa que os pesquisadores sejam menos confiáveis. De fato, o autor é altamente crítico em relação ao programa usado para criar um gráfico, por exemplo, mas é incapaz de ver falhas em testes de alto orçamento e alto conflito de interesses, mesmo quando eles pedem que mais de 100 cientistas escrevam uma carta aberta solicitando retratação
[ Abrir Carta ] .Dez meses depois, o autor ainda não entrou em contato conosco, fazendo comentários sem conteúdo no Twitter, como nos chamar de
“sh*tty” . Outros indivíduos que apontam erros com feedback detalhado e cuidadoso recebem tratamento semelhante, como ser chamado de
“d * ckhead” e ser bloqueado.Mais detalhes podem ser encontrados na
Resposta de Scott Alexander.A análise do SSC / Scott Alexander tem uma série de questões importantes.A análise com as exclusões recomendadas pelo SSC pode ser encontrada nos
Atualização: após exclusões escolhidas por SSC, exclusões por GMK, excluindo todos os tratamentos tardios e excluindo todos os estudos de profilaxia, SSC encontrou os resultados na
Figura 29 , mostrando eficácia estatisticamente significativa da ivermectina com
p = 0,04. O método para calcular este valor
p não é especificado. Usamos os mesmos resultados de eventos e realizamos a meta-análise de DerSimonian e Laird de variância inversa de efeitos aleatórios, como mostrado na
Figura 30 , encontrando significância muito maior com
p= 0,005. Observamos que a extração do efeito parece tendenciosa contra a ivermectina, escolhendo o braço de dose excessiva em Buonfrate e usando a exclusão post-hoc em López-Medina. A contagem de tratamento Krolewiecki parece ter sido dimensionada para os diferentes tamanhos de grupo. Não sabemos de onde são as contagens de Mahmud do SSC.
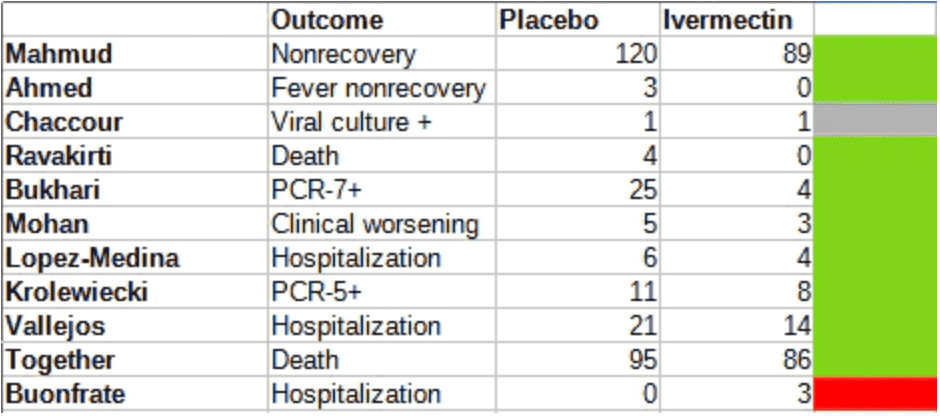
Figura 29. Análise do SSC. SSC relata
p = 0,04, com método não especificado.
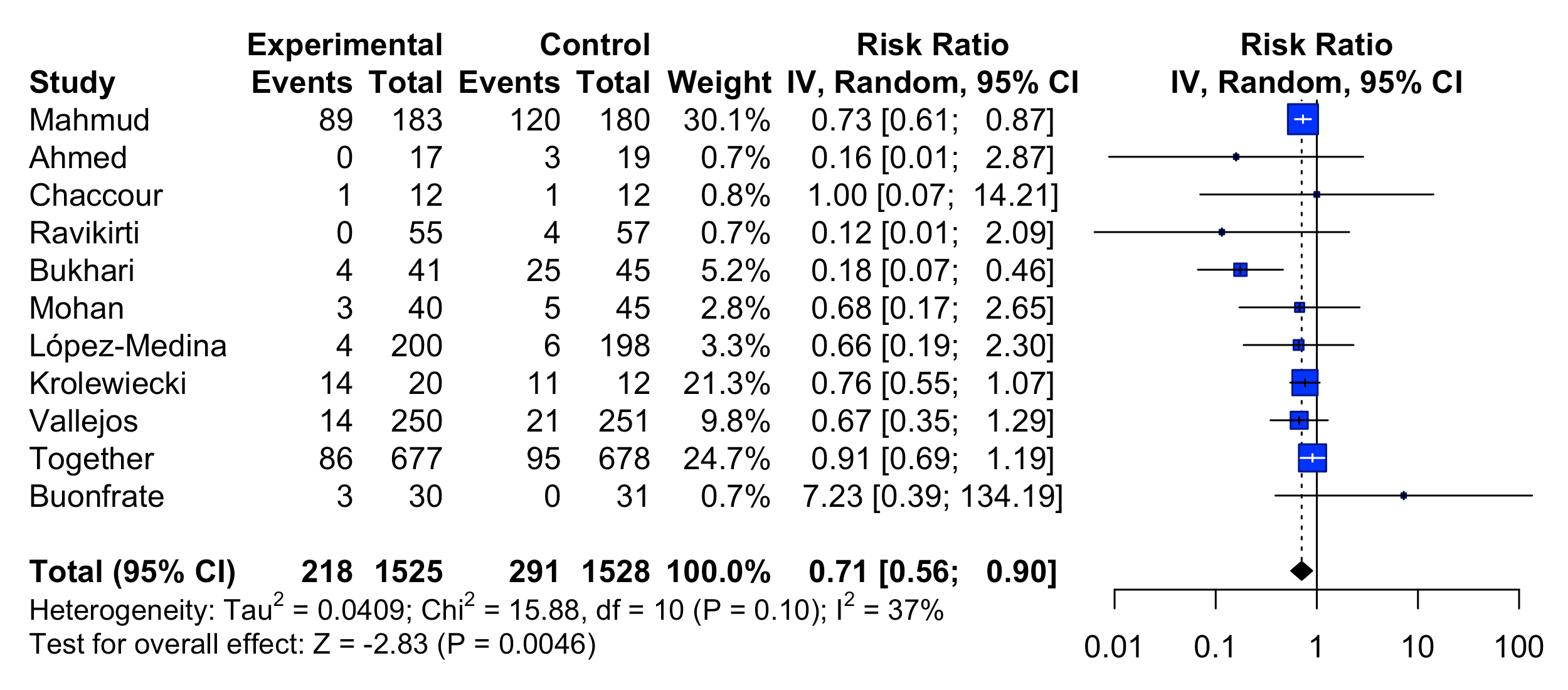
Figura 30. Meta-análise de efeitos aleatórios por resultados escolhidos do SSC, encontrando significância muito maior.O autor parece ser contra todos os tratamentos, rotulando-os como
“não ortodoxos” e
“controversos” , mesmo aqueles aprovados pelas autoridades de saúde ocidentais, incluindo casirivimab/imdevimab, bamlanivimab, sotrovimab e paxlovid.
Atualizar: o artigo original do autor ainda se refere a todos os tratamentos que seguimos como não ortodoxos e controversos, no entanto, eles relatam que realmente recomendam fluvoxamina, paxlovid, casirivimab/imdevimab, bamlanivimab/etesevimab e sotrovimab, e sugerem que eles apóiam todos os tratamentos aprovados pelas autoridades de saúde ocidentais que inclui adicionalmente remdesivir, budesonida, bebtelovimab, tixagevimab/cilgavimab e molnupiravir. O autor também tem comentários positivos para o zinco (mas relata que não há provas). ou seja, o autor parece realmente apoiar pelo menos 11 dos 42 tratamentos que seguimos. Notamos que a metodologia é a mesma para todos os tratamentos.Incentivamos o autor a pelo menos direcionar os leitores para tratamentos aprovados pelo governo, para os quais existem vários no
país do autor e muitos outros em
outros países (incluindo ivermectina). Embora os tratamentos aprovados em um país específico possam não ser tão eficazes (ou tão baratos) quanto os atuais protocolos baseados em evidências que combinam vários tratamentos, eles são melhores do que descartar tudo como
“não ortodoxo” . A eliminação do COVID-19 é uma corrida contra a evolução viral. Nenhum tratamento, vacina ou intervenção está 100% disponível e eficaz para todas as variantes – precisamos adotar todos os meios seguros e eficazes.A análise de terceiros que o autor faz referência para a teoria do Strongyloides é confundida pelo atraso do tratamento e dosagem – o grupo de alta prevalência tem mais ensaios de tratamento precoce e uma dose média mais alta, ou seja, a análise reflete a maior eficácia do tratamento precoce e a maior eficácia de maior dosagem. Mais detalhes podem ser encontrados na
seção Strongyloides .O autor refere-se a estudos com resultados positivos, mas não estatisticamente significativos, como
“negativos” [ Mohan ] ou
“[o] resultado original também teria mostrado que a ivermectina não funcionava” [ López-Medina ] , que são conclusões incorretas
[ Amrhein ] .
Atualizar: o autor acredita que isso significa que abandonamos a significância estatística. Não sabemos de onde isso vem – todos os nossos resultados relatam intervalos de confiança, e as duas primeiras palavras deste artigo são “estatisticamente significativas”. O que é incorreto é tirar uma conclusão negativa com base em um resultado insignificante. Por exemplo, se um estudo relata uma mortalidade 50% menor sem atingir significância estatística, isso não significa que o tratamento seja inútil. Considere se houver 10 estudos todos relatando uma mortalidade ~50% menor, a evidência combinada pode ser forte, mesmo que cada resultado individual não seja estatisticamente significativo.O autor observa que:
“se você disser algo a favor da ivermectina será expulso da civilização e jogado no círculo do inferno social reservado aos membros da Klan e 1/6 insurretos” , sugerindo um ambiente que pode enviesar a informação de que o autor vê, e pode inconscientemente enviesar a análise. Observamos que ambientes semelhantes influenciam o design, operação e publicação de alguns ensaios existentes (e muitos futuros) de ivermectina.O autor analisa 29 dos 85 estudos, que notamos ser muito melhor do que a maioria dos comentadores, mas ainda ignora a maioria dos estudos, incluindo os estudos de profilaxia.O autor encontra eficácia em
p = 0,04 em sua análise de 11 dos 29 estudos analisados. Observamos que simplesmente olhar para os outros 56 estudos resultará em uma confiança muito maior na eficácia. Também observamos que mesmo em
p = 0,04 com 11 estudos independentes, uma análise racional de risco-benefício resulta em adoção imediata em protocolos (pendente de dados mais fortes com outras combinações de tratamentos) e coleta imediata de mais dados de fontes sem conflitos de interesse.No entanto, em última análise, o autor apoia pelo menos parcialmente as duas teorias predominantes que são comumente usadas por aqueles contra o tratamento. Essas teorias exigem desconsiderar extensas evidências contraditórias:As etapas necessárias para aceitar o resultado
sem efeito significativo são extremas – é preciso encontrar uma razão para excluir a maioria dos estudos, desconsiderar a forte relação de resposta ao atraso do tratamento e desconsiderar todos os estudos de profilaxia. Mesmo depois disso, o resultado ainda é positivo, mas não estatisticamente significativo. Isso não suporta uma recomendação negativa. Tratamentos amplamente aceitos e eficazes (sujeitos à dependência de variantes virais) como casirivimab/imdevimab, bamlanivimab e sotrovimab foram todos aprovados sem benefícios de mortalidade estatisticamente significativos.As etapas necessárias para aceitar a conclusão
apenas do mecanismo de Strongyloides também são extremas – precisamos desconsiderar a maioria dos resultados que ocorrem antes do uso de esteróides e desconsiderar a forte relação de resposta ao atraso do tratamento, que é contraditória.
A Figura 26 mostra a análise por prevalência de Strongyloides. A análise de terceiros referenciada pelo autor é confundida pelo
atraso do tratamento e dosagem .O autor parece inclinado contra acreditar em qualquer tamanho de efeito grande. Observamos que grandes tamanhos de efeito foram observados em vários tratamentos COVID-19 aprovados pelas autoridades de saúde ocidentais, incluindo o paxlovid, sobre o qual o autor é muito positivo, e também que melhores resultados podem ser esperados quando os estudos combinam vários tratamentos eficazes com mecanismos de ação complementares (como os médicos que tratam o COVID-19 precocemente normalmente fazem).
Atualização : o autor confirma esse viés, mas parece desconsiderá-lo para paxlovid.O autor suspeita de um estudo baseado no país dos pesquisadores e também parece tendencioso contra falantes não nativos, com comentários como
“ilegível” para um artigo, comparado a
“escrito muito bem em inglês real” para outro.
Atualização : o autor confirma ser tendencioso contra certos países.O autor chama um médico que relatou zero mortes e 5 hospitalizações com 2.400 pacientes com COVID-19 de
“uma pessoa louca” que
“coloca seus pacientes em todos os medicamentos estranhos que ele poderia pensar” .O autor desconsidera a mortalidade dramaticamente mais alta para variantes Gamma vs não Gama (aHR 4.73 [1.15-19.41]
[ Zavascki ] ), em vez disso, concluindo que a mortalidade mais alta indica fraude em um caso, enquanto em outro caso assume que a confusão relacionada ao tempo no O julgamento em conjunto não é significativo.A revisão do autor dos 29 estudos parece relativamente superficial, por exemplo, o autor parece não saber que a dosagem de ivermectina é muito diferente no braço de ivermectina + doxiciclina de
[ Ahmed ] .O autor parece aceitar a análise e as acusações da GMK como corretas, mas esse autor
geralmente está incorreto .O autor está preocupado que detalhemos os problemas com
[ López-Medina ] , enquanto observa corretamente que os resultados neste estudo são realmente positivos e a favor da ivermectina (embora não sejam estatisticamente significativos isoladamente).O autor está preocupado que comentemos especificamente sobre
[ López-Medina , Reis ] . Observamos que foram outros que se concentraram nesses ensaios – comentamos sobre eles porque receberam atenção especial, inclusive sendo apresentados como única evidência que substitui todos os outros ensaios, apesar de terem grandes problemas.Autor afirma que ninguém pode encontrar problemas com
[ Vallejos ] , o que sugere que eles não leram o estudo ou nossa
análise .
Resposta AT.Um blog de tecnologia publicou um artigo com declarações incorretas e sem suporte. O artigo refere-se ao
c19ivermectin.com (que é apenas um banco de dados de pesquisa de ivermectina), mas faz comentários sobre essa análise. A maioria dos comentários neste artigo já foram abordados acima.O autor observa corretamente que a maioria dos resultados é positiva e que não importa como você segmente os dados, os resultados são positivos, mas parece descartar a razão óbvia sem examinar as evidências.O autor acredita que, como existem outros tratamentos eficazes, e porque também os abordamos, deve haver um viés positivo. No entanto, para a ivermectina, encontramos evidências de um viés de publicação negativo e, apesar da enorme atenção mundial, não há evidências de ensaios negativos ausentes, enquanto há evidências substanciais de ensaios positivos sendo atrasados pelos editores (revistas aceleram resultados nulos, mantendo positivos julgamentos e depois devolvê-los sem revisão). Também observamos que muitos dos tratamentos eficazes são adotados por governos em todo o mundo, incluindo vários no país do autor. Os tratamentos aprovados incluem sotrovimab, casirivimab, imdevimab, bamlanivimab, etesevimab, budesonida, favipiravir e plasma convalescente (embora não mostre eficácia em nossa análise),
[ Miller ] .O autor considera a heterogeneidade na dosagem, tempo de tratamento, etc. preocupante. Essa heterogeneidade é benéfica e nos dá muito mais informações sobre as situações em que o tratamento é eficaz e a dosagem ideal. Os resultados de um único estudo se aplicam apenas às condições desse estudo e não podem ser extrapolados para outras condições – o autor comete esse erro alegando que outro tratamento é ineficaz com base em evidências definitivas, mas essa evidência se aplica apenas ao tratamento muito tardio em uma população muito doente com dosagem excessiva – não o uso ideal de um antiviral para COVID-19. Embora não possamos usar a maior base de evidências para prever uma situação específica, por exemplo, mortalidade em pacientes de alto risco com atraso no tratamento e dosagem específicos, podemos usar a maior base de evidências como evidência a favor/contra a eficácia,O autor refere-se ao estudo Elgazzar retirado (removido desta análise no mesmo dia) como um grande desenvolvimento, porém não houve mudança significativa. A exclusão de 1 de 88 estudos tem muito pouco efeito, e a exclusão realmente melhora a relação atraso-resposta do tratamento. 54 de 85 estudos precisam ser excluídos para evitar encontrar eficácia estatisticamente significativa em uma análise de sensibilidade de pior caso.O autor está preocupado que alguns estudos usem o tratamento combinado, no entanto 68 não usam o tratamento combinado, e a maioria das adições são tratamentos independentemente conhecidos por não terem eficácia significativa isoladamente.Também notamos que o autor nunca nos contatou.
Como o resultado deve ser interpretado ao agrupar os efeitos?Na análise combinada, o resultado é uma média ponderada da melhora no resultado mais grave relatado. As análises específicas devem ser usadas para resultados específicos. Observe que uma redução na mortalidade decorre logicamente de uma redução na hospitalização, que decorre de uma redução nos casos sintomáticos, etc. Observe que temos que considerar todas as informações para criar a previsão mais precisa de eficácia. Embora existam maneiras mais sofisticadas de combinar todas as informações, a vantagem do método usado aqui é a simplicidade e a transparência. Observe que os resultados altamente significativos observados não incorporam informações adicionais que aumentariam ainda mais a confiança, como a relação atraso-resposta do tratamento.
Elgazzar.Este estudo foi retirado e removido desta análise no mesmo dia. Não houve mudança significativa (excluir 1 de 88 estudos tem muito pouco efeito, e a exclusão realmente melhora a relação atraso-resposta do tratamento).
Samaha.Este estudo foi removido desta análise dentro de uma hora após a notificação de que estava pendente de retratação. Não houve mudança significativa nos resultados, e a exclusão melhora a relação dose-resposta.
Merino.Esta pré-impressão foi censurada pelo host da pré-impressão original. Os censores afirmam que o programa de tratamento do governo, que usou medicamentos aprovados e salvou mais de 500 pessoas da hospitalização, era antiético. Em parte, eles também indicam que os estudos dos “efeitos de um medicamento no desfecho de uma doença” estão fora do escopo de seu site.A resposta do autor (não fornecida pelos censores) pode ser encontrada aqui:
[ twitter.com (D) ] . Os autores fornecem os dados e o código do estudo, e os resultados foram verificados independentemente.
Pott-Júnior.Este artigo parece ter sido censurado a pedido do editor fundador da revista
[ pubmed.ncbi.nlm.nih.gov ] . Uma revisão externa é mencionada, mas não é fornecida, e não há resposta dos autores ou indicação de que os autores foram notificados. As conclusões deste estudo são limitadas devido ao pequeno tamanho, no entanto, devemos considerar todas as informações no contexto do corpo completo da pesquisa.
Efimenko.A publicação da conferência para esta análise foi autocensurada pelos autores, não devido a qualquer erro na análise, mas porque os autores acreditam que a ivermectina “se mostrou ineficaz em ensaios clínicos”. Isso é incorreto, 55 estudos mostram resultados positivos estatisticamente significativos para um ou mais resultados (29 estudos prospectivos e 26 retrospectivos, incluindo 20 ensaios clínicos randomizados).
Carvallo.Preocupações foram levantadas sobre
[ Carvallo ] . Parece haver algumas preocupações válidas com possíveis problemas de dados, e este estudo foi excluído da
análise de exclusão . Não há mudança significativa nos resultados, com apenas uma pequena redução na eficácia da profilaxia para 82%
[68-89%]. No entanto, é difícil confiar nas informações da personalidade que relata as preocupações. O autor sugere que o estudo pode não ter acontecido, alegando, por exemplo, que a equipe não poderia pagar os medicamentos sem financiamento e que um médico ocupado não teria tempo suficiente. No entanto, com apenas verificações básicas, o autor saberia que uma empresa farmacêutica confirmou a doação dos medicamentos, que confirmou que a autorização para o estudo foi recebida, que o hospital principal para o estudo solicitou suprimentos adicionais e que o hospital confirmou a aprovação do comitê de ética . Para detalhes adicionais veja
[ O’Reilly ]. Também observamos que o tratamento combinado neste estudo demonstrou ser eficaz de forma independente, e os mecanismos complementares de ação suportam uma eficácia melhorada da combinação
[ Figueroa ] .Notas de estudoPara discussão de todos os estudos, consulte
c19ivermectin.com . Alguns estudos receberam atenção especial, com alguns considerando-os como evidências muito fortes que se sobrepõem aos outros 84 estudos. Observamos as limitações desses estudos aqui.
Muitos problemas importantes, incluindo vários números impossíveis, falha de ocultação, falha de randomização e muitas violações de protocolo , conforme detalhado abaixo.
Enviar atualizações ou correçõesVeja também:
Fraudulent Trial On Ivermectin Publicado pelo The World’s Top Medical Journal .. ,
Parte 1 ,
As Declarações Falsas, Sinistras e Duplicadas dos Investigadores do Ensaio de Ivermectina , e
10 Perguntas para os Investigadores do Ensaio .Comentários privados:
“Há um sinal claro de que o IVM funciona em pacientes com COVID .. isso seria significativo se mais pacientes fossem adicionados . stevekirsch.substack.com ] .
“Não estou interessado nesta questão, pois não é a maneira correta de interpretar o resultado” – Ed Mills, respondendo a uma solicitação de contagem de mortes por protocolo [ pierrekory.substack.com ] .
“Foda-se” “Foda-se” “Glória a Satã” “Você é um desses filhos da puta…” “Seu filho da puta” — Ed Mills, respondendo a vários e-mails sobre o julgamento e a ivermectina pesquisa [ pierrekory.substack.com ] .Comentários públicos:
“Não houve indicação de que a ivermectina seja clinicamente útil” – Ed Mills, co-investigador principal do Together Trial.
“.. a questão de saber se este estudo foi interrompido muito cedo à luz das ramificações políticas da necessidade de demonstrar que a eficácia é realmente inexpressiva.. realmente poderia ser levantada ..” – Frank Harrell, “Concordo totalmente com Frank” – Ed Mills [ vimeo.com ] .
5 de abril: O jornal foi atualizado silenciosamente, sem indicação ou explicação das mudanças. As alterações incluem: faixa etária, descrição do placebo, contagem por protocolo e contagem de óbitos (detalhes abaixo).
5 de maio: O jornal foi atualizado silenciosamente novamente. Um novo resumo observa que os autores
tentaram rastrear o uso anterior de ivermectina, contradizendo tanto a seção de discussão, onde os autores afirmam não
garantir o uso
para COVID-19 , quanto os critérios de exclusão e formulários de entrevista, que não especificam o uso de ivermectina.
Atualização de 30 de maio: ainda não há resposta às solicitações de dados, e os autores continuam mantendo silêncio de rádio sobre os muitos problemas sérios [ twitter.com (E) ] .
Demorado > 6 meses. O papel foi atrasado mais de 6 meses sem explicação. O braço de fluvoxamina complementar, concluído ao mesmo tempo, foi publicado em 23 de agosto de 2021. O artigo foi submetido ao NEJM em setembro de 2021
[ vimeo.com (B) ] . Os formulários COI sugerem que autores adicionais foram adicionados após a submissão e o autor correspondente mudou de Prof. Mills para Dr. Rayner
[ doyourownresearch.substack.com ] , cujos conflitos incluem Pfizer, Merck, a Fundação Gates e o Governo Australiano.
Sem resposta ao pedido de dados. O registro do estudo afirma que os dados deveriam estar disponíveis no término e mediante solicitação
[ clinicaltrials.gov (B) ] , no entanto, os autores não responderam a uma solicitação de dados. Mesmo os financiadores do estudo não conseguiram acessar os dados
[ odysee.com ] . As solicitações podem ser enviadas para thetogethertrial@gmail.com, deixe-nos saber o resultado.
O ICODA relata nunca ter os dados. Os investigadores relatam que os dados estão disponíveis via ICODA:
“O conjunto de dados final do estudo estará acessível mediante solicitação por escrito aos investigadores principais do estudo (G Reis ou EJ Mills). Não há acordos contratuais para limitar o acesso aos dados finais do estudo. Todos os dados coletados by the TOGETHER Trial será compartilhado com a International COVID-19 Data Alliance” . Não apenas não houve relatos de acesso bem-sucedido aos dados, mas um gerente do ICODA relata que eles nunca tiveram os dados
[ t.me ] .
Os comprimidos placebo podem não corresponder aos comprimidos de tratamento. Os autores não especificam a aparência dos comprimidos de placebo, sugerindo que eles podem não corresponder aos comprimidos de tratamento, fornecendo uma razão adicional para o fracasso do cegamento. Um investigador brasileiro relata que, na época do estudo, havia apenas um provável fabricante de placebo, e eles supostamente não receberam uma solicitação para produzir comprimidos de placebo idênticos
[ doyourownresearch.substack.com (B) ] . Eles também relatam que a ivermectina manipulada no Brasil é considerada não confiável.
Três contagens de mortes diferentes. No artigo original, a Tabela 3 mostra 21 e 24 mortes, enquanto a Tabela S6 mostra 20 e 25
[ twitter.com (F) ] . Na Tabela 3, os eventos de morte e grau 5 mostraram os mesmos números 21/24, mas diferentes tamanhos de efeito, sendo 0,81 mais próximo das contagens 20/25 e do número relatado anteriormente. Isso é consistente com uma morte sendo movida entre os braços após a geração do manuscrito, mas não atualizada na Tabela S6 ou na Tabela 3 AE RR. Isso não pode ser explicado pela população de segurança excluindo pacientes com dose zero porque as mortes de controle de EA são maiores. Por e-mail, um co-investigador principal sugeriu que a discrepância se devia a uma das mortes por COVID-19 e a outra por todas as causas
[ stevekirsch.substack.com] . Essa explicação não se ajusta aos dados porque um braço aumenta enquanto o outro diminui. Ambos os co-investigadores principais relatam no artigo que
“eles tiveram acesso total a todos os dados do estudo e garantem a precisão e integridade dos dados e a fidelidade do estudo ao protocolo”. Um terceiro conjunto de contagens de mortes, 20 e 24, com RR 0,84, foi apresentado por um co-investigador principal em 18 de março de 2022
[ vimeo.com (C) ]. No total, foram apresentados 4 riscos relativos de morte diferentes: apresentação de 18 de março de 2022: 0,84, artigo de 30 de março: 0,88 (T3), 0,81 (T3 AE) e 0,80 (TS6, apresentado como 20 e 25 apenas sem tamanhos de grupo) . 6 dias após a publicação, o artigo foi atualizado, sem nenhuma informação sobre o que foi alterado. Nesta versão, uma morte por “distúrbios respiratórios, torácicos e mediastinais” foi removida do braço de controle e uma morte por “infecções e infestações” foi adicionada ao braço de ivermectina. O trabalho ainda indica RR 0,81 para óbito AE.
O julgamento não foi cego. O cegamento da ivermectina/placebo foi feito atribuindo-se uma letra a cada grupo que era conhecida apenas pelo farmacêutico. Se um paciente recebeu um tratamento de 3 doses, os investigadores sabem imediatamente que é mais provável que o paciente esteja no grupo de tratamento do que no grupo de controle, porque o placebo de 3 doses foi relativamente raro (~46% do PP). Se um paciente não recebeu tratamento de 3 dias, os investigadores sabem imediatamente que o paciente não é um paciente em tratamento com ivermectina. Além disso, observando a frequência das alocações, os investigadores podem facilmente determinar qual letra corresponde ao tratamento de 3 dias com ivermectina ativa, removendo assim todo o cegamento. Por exemplo, considere 3-dose-ivermectina e 3-dose-placebo sendo identificados pelas letras G e K. Se as alocações até o momento foram G:11 e K:20, há uma probabilidade muito alta de que K seja ivermectina. Observe que essa falha cegante é óbvia apenas porque a revista exigiu que os autores se restringissem ao grupo placebo de 3 dias. Observe também que seria trivial evitar, se desejado, por exemplo, usando um identificador exclusivo para todos os frascos de medicamentos. Observe que pode haver razões adicionais para falha de ocultação, por exemplo, o papel especifica garrafas de formato idêntico, mas não parece especificar comprimidos de aparência idêntica
[ doyourownresearch.substack.com (B) ] .
As contagens de pacientes não correspondem ao gráfico de inscrição divulgado anteriormente. Os autores afirmam que os pacientes com ivermectina e controle foram todos a partir de 23 de março de 2021, no entanto, análises independentes do gráfico de inscrição (contido nesta apresentação
[ dcricollab.dcri.duke.edu ] ) exigem a inclusão de pacientes anteriores a essa data para atingir o números relatados
[ doyourownresearch.substack.com (C) , longhaulwiki.com ] . O gráfico de inscrição mostra uma inscrição muito maior para ivermectina perto do início do estudo. A única maneira que o número de pacientes placebo pode ser o mesmo que o número de pacientes em tratamento é se os pacientes placebo foram retirados de um período anterior
[ Marinos ], que cria um grupo de controle não concorrente
[ nejm.org (B) ] e confusão substancial por tempo conforme abaixo.
Contagens conflitantes de braços placebo nos braços IVM/FLV. O braço placebo IVM tem 679 pacientes e o braço FLV tem 756. Os 679 devem ser compartilhados entre os braços, com 77 pacientes extras para FLV. Para FLV, havia 34 pacientes placebo necessitando de ventilação mecânica, para IVM havia apenas 25, indicando que 9 dos 77 pacientes placebo extras para FLV tiveram ventilação mecânica, uma porcentagem muito maior durante um período que teve menores mortes e CFR (e incluiu pacientes vacinados). A hospitalização por todas as causas com placebo mostra 95/679 para IVM e 99/756 para FLV, ou seja, apenas 4 dos 77 pacientes extras foram hospitalizados, mas o artigo relata mais 9 pacientes com ventilação mecânica.

Para FLV, houve 11 EAs grau 1, para IVM foram 12, com 77 pacientes a menos.Para FLV, houve 50 EAs de grau 3, para IVM também houve 50, o que significa que os 77 pacientes extras tiveram 0% de EAs de grau 3 versus 7,4% esperadosPara FLV, havia 54 pacientes com DRC conforme Figura 3 e eTabela1 (2 conforme Tabela 1). Para IVM houve 5.
DSMC não independente. O revisor 1 do protocolo observa que o DSMC não é independente
[ gatesopenresearch.org ] . O Prof. Thorlund é vice-presidente da organização de pesquisa contratada (CRO, Cytel), professor da universidade patrocinadora e autor do protocolo. Dr. Häggström é um funcionário do CRO.
[ doyourownresearch.substack.com (C) , twitter.com (G) ] revela muitos outros conflitos. O Prof. Thorlund escreveu mais de 100 artigos com o Prof. Mills. O Prof. Singh escreveu 29 artigos com o Prof. Mills. O Prof. Orbinski escreveu 9 artigos com o Prof. Mills. A primeira versão do site mostrava o Prof. Mills e o Prof. Thorlund como líderes conjuntos. Os e-mails apontavam para uma empresa MTEK Sciences, fundada pelo Prof. Mills e Prof. Thorlund (a hipótese de MTEK significa Mills, Thorlund, Edward, Kristian). A MTEK recebeu doações da Fundação Gates. A MTEK também empregou o Dr. Häggström. A MTEK foi adquirida pela Cytel em 2019. O Dr. Häggström trabalha para a Fundação Gates. Dois membros do DSMC publicaram um artigo com membros de um conhecido grupo de pesquisa anti-ivermectina
[ Thorlund ] e o Dr. Hill, cuja meta-análise tem relatos de influência externa
[ c19ivermectin.com , c19ivermectin.com (B) , twitter.com (H) ] . O protocolo do estudo relata que
“será estabelecido um DSMC independente, composto por cientistas de reputação e experiência incomparáveis, sem envolvimento com este protocolo de pesquisa”.
Randomização desigual, confusão significativa por tempo. O estudo relata randomização 1:1:1:1, no entanto, a análise independente mostra uma inscrição muito maior no braço de tratamento com ivermectina no início do estudo
[ c19ivermectin.com (C) , longhaulwiki.com ] . Isso introduz uma confusão muito significativa por tempo devido à grande mudança na distribuição de variantes.
[ Zavacki ]mostram mortalidade dramaticamente mais alta para variantes Gama vs não Gama (mortalidade de 28 dias a partir do início dos sintomas aHR 4,73 [1,15-19,41]). Muito mais pacientes foram randomizados para ivermectina versus placebo nas primeiras semanas, por exemplo, a primeira semana mostra 82 ivermectina versus 28 pacientes com placebo, 2,9 vezes mais. O período de inscrição em excesso de ivermectina coincide de perto com um período de mortes e CFR significativamente maiores no Brasil.
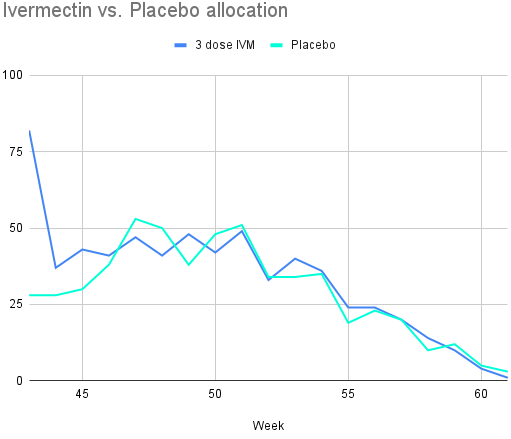
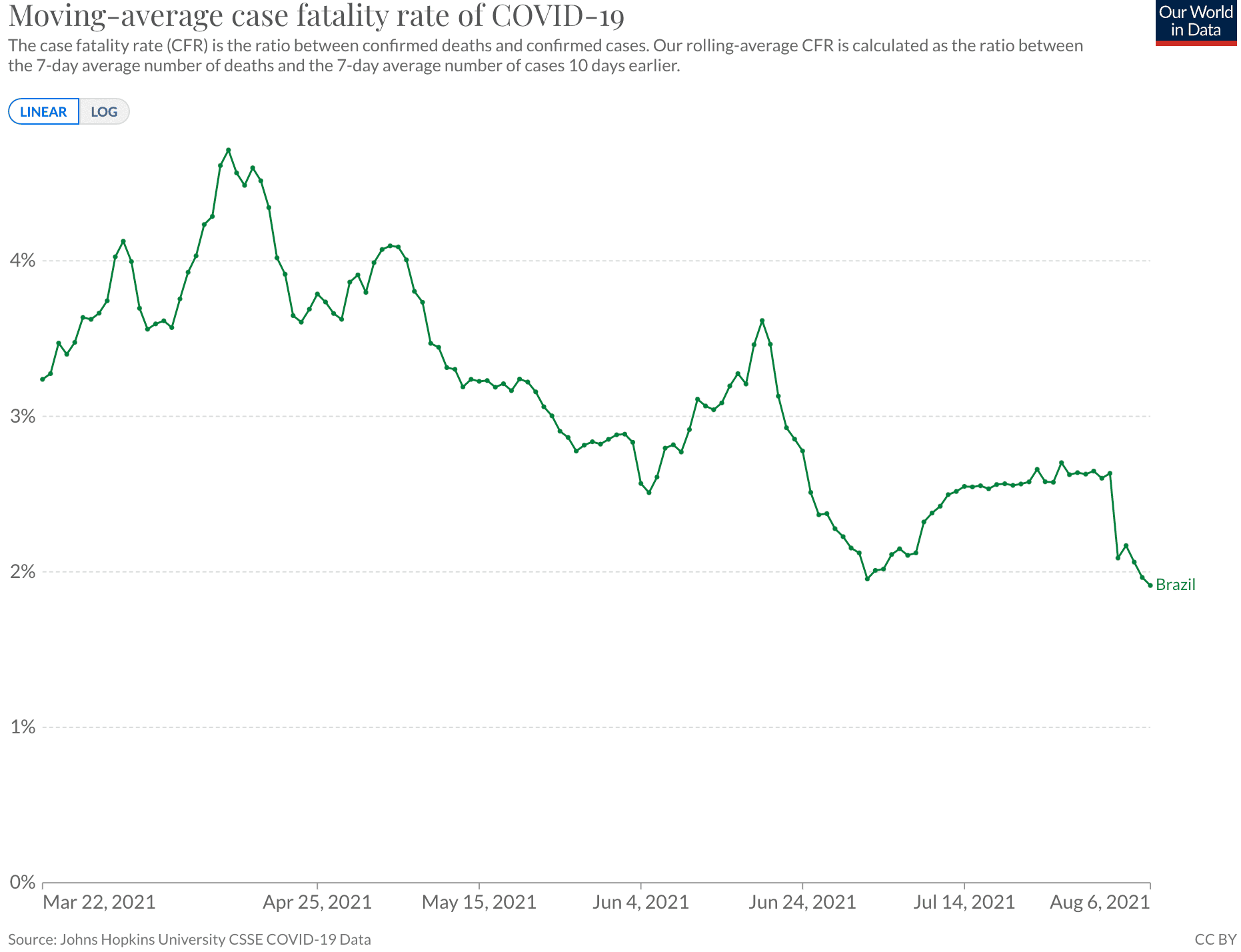
O tempo perdido desde o início dos pacientes mostra eficácia estatisticamente significativa. Para os subgrupos de tempo conhecido desde o início, ambos os grupos mostram resultados piores do que os resultados gerais
[ twitter.com (I) ] , com os 317 pacientes ausentes mostrando eficácia significativa RR 0,51, p = 0,02 (comparado a 1,00 e 1,14 para pacientes conhecidos) .
Pacientes com início desconhecido foram inscritos, resultados de subgrupos opostos a estudos anteriores. Após a imputação, o percentual de pacientes no subgrupo de tratamento tardio passou de 46% para 56%. Previa-se que 87% dos pacientes desconhecidos estavam no grupo tardio. Isso é razoável e esperado – pacientes que não se lembram de quando foi o início são mais propensos a ter um início mais distante no passado. O que não está claro é como esses pacientes podem ser incluídos no estudo, quantos desses pacientes tiveram início > 7 dias, como esse subgrupo de 317 pacientes muito tardios pode mostrar eficácia muito maior como acima e por que os autores não relataram esse resultado, analise isso com mais detalhes ou recomende pesquisas adicionais.
Perfil de efeitos colaterais consistente com muitos pacientes em tratamento que não receberam ivermectina autêntica e/ou pacientes de controle que receberam ivermectina. Os efeitos colaterais (por exemplo, efeitos colaterais gastrointestinais foram menores no braço de ivermectina) sugerem que muitos pacientes com ivermectina podem não ter recebido ivermectina autêntica, ou que pacientes placebo podem ter tomado ivermectina. Para comparação, houve uma incidência 3,6 vezes maior de diarréia no braço de tratamento em
[ Lim ] .Um investigador brasileiro local relata que, no momento do estudo, havia apenas um provável fabricante de placebo, e eles supostamente não receberam uma solicitação para produzir comprimidos de placebo idênticos
[ doyourownresearch.substack.com (B) ] . Eles também relatam que a ivermectina manipulada no Brasil é considerada não confiável. O protocolo informa que
“o medicamento em estudo utilizado será proveniente de plantas farmacêuticas que possuem autorização comercial para sua produção, já aprovada pela ANVISA”.
Alterações na inclusão da vacina. O estudo mudou de incluir pacientes vacinados para excluí-los em 21 de março de 2021
[ clinicaltrials.gov (C) , twitter.com (J) ] e em 5 de julho a exclusão foi alterada para especificar >14 dias. Como acima, atender às contagens de placebo relatadas provavelmente requer o uso de pacientes com placebo do período anterior, que tem um fator de confusão muito significativo devido a alterações de variantes e, adicionalmente, de confusão devido à vacinação. Ambos favorecem o grupo placebo. O critério de inclusão da vacina original é incomum, mas é mostrado tanto no protocolo quanto no registro do clinicaltrials.gov
[ clinicaltrials.gov (D) , togethertrial.com ]. Isso pode ter sido escolhido para reduzir o potencial de eficácia. Para mais informações sobre inclusão de vacinação, veja
[ twitter.com (K) ] .

Conclusão incorreta. A conclusão afirma que a ivermectina
“não resultou em menor incidência de [hospitalização] ou de [observação no pronto-socorro >6h]” . Isso é incorreto, a hospitalização foi 17% menor, o que não é estatisticamente significativo com o tamanho da amostra e análise estatística típica. Para a análise bayesiana que os autores utilizam, a probabilidade de superioridade do ITT para a ivermectina foi de 79,4%, o que é um resultado positivo, o contrário da conclusão.
Uso de ivermectina amplamente difundido na comunidade. O uso recente de ivermectina não estava nos critérios de exclusão. A ivermectina estava disponível sem receita, foi recomendada pelo governo para o COVID-19 e teve vendas nove vezes maiores
[ twitter.com (L) ] . Os autores afirmam que garantiram que os pacientes não usaram ivermectina por meio de “triagem extensa”, mas não explicam por que esse não foi um critério de exclusão ou como essa exclusão não escrita foi garantida, embora haja muitos dados ausentes relacionados aos critérios de exclusão escritos. Exclusões não escritas semelhantes não foram mencionadas para outros braços
[ twitter.com (M) ] , um investigador principal afirmou anteriormente que tal exclusão não deveria ser um problema
[ twitter.com (N) ], e não é mencionado nas folhas de entrevista
[ osf.io ] . Após a publicação, um co-investigador principal teria escrito que
“mesmo que alguns pacientes tivessem acesso à IVM, o fato de estar cego ainda deve manter o equilíbrio” , o que é incorreto, espera-se que os pacientes com placebo em uso de ivermectina melhorem, pacientes em tratamento que já têm distribuições teciduais significativas podem ter respostas positivas, neutras ou negativas ao tratamento adicional.
O recrutamento de dose única continuou após a mudança. O estudo havia solicitado a mudança para o tratamento com 3 doses até 15/19 de fevereiro, quando apenas 19 pacientes haviam sido recrutados, mas o estudo continuou recrutando mais 59 pacientes para o tratamento com dose única
[ twitter.com (O) ] .
População por protocolo diferente do braço de fluvoxamina contemporânea. Os números por protocolo da Tabela 2 mostram 92% dos pacientes por protocolo para ivermectina e apenas 42% para controle. Esta parece ser uma mudança post-hoc selecionando apenas pacientes de placebo de 3 dias, enquanto uma seleção semelhante não parece ter sido feita para o estudo de fluvoxamina (mostrando 74% e 82% de pacientes por protocolo para fluvoxamina e controle)
[ Reis (B) ] .
Vários protocolos de randomização conflitantes. [ twitter.com (P) ] revisou o protocolo de randomização, encontrando três algoritmos diferentes e versões conflitantes nos artigos.
Tempo de início, necessário para inclusão, ausente para 317 pacientes. Para o braço de fluvoxamina acompanhante, 24% dos pacientes tiveram um tempo desconhecido desde o início, incluindo 179 dos pacientes controle
[ Reis (B) ] . Neste estudo, 0 pacientes têm um tempo de início não especificado na Tabela 1, devido à imputação. No entanto, a Figura 2 revela que o tempo de início é desconhecido para 317 pacientes, semelhante ao papel da fluvoxamina. No entanto, o tempo de início é necessário para os critérios de inclusão. De acordo com a Figura 2, a idade e o IMC também apresentam valores omissos.
Contagens de comorbidade conflitantes. O braço de fluvoxamina complementar ocorreu de 20 de janeiro a 5 de agosto de 2021, enquanto este estudo ocorreu de 23 de março a 6 de agosto de 2021 – a maioria dos pacientes de controle deve ser compartilhada, com um adicional de 10% para fluvoxamina desde o início anterior. A apresentação de 6 de agosto, que tem uma data de 9:38 am 6 de agosto, horário local do teste
[ doyourownresearch.substack.com (D) ] , mostra 678 pacientes com placebo, indicando que 0 ou 1 pacientes com placebo foram randomizados em 6 de agosto. deveria ter sido randomizado em 6 de agosto, porque os autores não podem adicionar pacientes após a revelação.O braço de controle da fluvoxamina mostra 16/756 pacientes de controle com asma. O braço de controle da ivermectina tem um subgrupo desses pacientes (679), mas mostra uma prevalência muito maior de asma (60 pacientes). Isso pode ser possível devido à imputação se houver uma porcentagem muito alta de dados ausentes, no entanto, a imputação não parece ser uma boa explicação. Por exemplo, a DRC placebo vai de 2 a 5 (FLV->IVM). Primeiro, não é lógico imputar a DRC em pacientes com base nas outras variáveis. Em segundo lugar, o protocolo especifica a imputação apenas com até 20% de dados ausentes, tornando improvável que a imputação adicione 150% dos pacientes com DRC. Terceiro, o grau de mudança entre FLV e IVM varia drasticamente, com IVM relatando 666%, 275%, 150% e 43% mais pacientes para DPC, asma, DRC e CCD,
Inscrição de destino conflitante. Há números de inscrição de destino conflitantes. O protocolo mostrou 800 pacientes por braço em 21 de março de 2021 (após o início do estudo)
[ static1.squarespace.com , twitter.com (Q) ] , o co-investigador principal relatou 800 por braço em uma entrevista publicada em 14 de junho, 2021
[ halifaxexaminer.ca ] , e o protocolo mudou para 681 em 22 de junho
[ static1.squarespace.com (B) ] . No entanto, o registro do estudo de janeiro indica 2.724 (681*4) pacientes
[ clinicaltrials.gov (D) ], sugerindo que a meta de 800 foi mais tarde, e foi mantida para fluvoxamina, mas revertida para ivermectina. O braço de fluvoxamina que começou dois meses antes foi encerrado ao mesmo tempo, e foi encerrado devido à superioridade
[ Reis (B) ] após 741/756 pacientes. Observe que o Gamma estava diminuindo significativamente em torno do ponto de término, o que provavelmente favorece a melhoria da eficácia se o estudo continuasse, devido ao tratamento tardio e à dosagem usada. O co-investigador principal relata três razões diferentes para interromper o estudo
[ twitter.com (R) ] : a) porque ficou sem dinheiro, b) porque terceiros não apoiaram e c) foi feito pelo DSMC e estava fora de seu controle.
Supostamente encerrado por futilidade, embora o limite de futilidade não tenha sido atingido. O julgamento foi encerrado devido à futilidade
[ twitter.com (S) ] , no entanto, os limites de futilidade foram 20%, 40% e 60%, e todas as probabilidades publicadas são > 60% (ITT 79,4%). Além disso, o braço da fluvoxamina não teve o limiar mais alto de 60%, usando apenas 40%. Observe que o DSMC não era independente como abaixo.
Triagem para atraso no tratamento. A maioria dos protocolos do Together Trial mostra um atraso adicional de um dia no tratamento já tardio para a maioria dos pacientes. O protocolo de 5 de agosto de 2021 publicado com o artigo de metformina
[ ars.els-cdn.com ] mostra a administração do tratamento um dia após a triagem, linha de base e randomização (Tabela 2, cronograma de atividades do estudo). Isso também pode ser encontrado no protocolo datado de 11 de março de 2021
[ drive.google.com (C) ] . O protocolo anexo ao papel da ivermectina, datado de 15 de fevereiro de 2021, mostra um cronograma diferente, informando que o tratamento
deveser administrado no mesmo dia da randomização. Não há explicação de quando essa mudança foi feita, como os braços sobrepostos de metformina e ivermectina podem usar horários diferentes ou como essa mudança foi implementada (há muitas tarefas na triagem e nas visitas de linha de base). Não há relato de quantos pacientes receberam tratamento no mesmo dia. O formulário para a primeira consulta de tratamento pergunta se houve eventos clínicos, incluindo visitas de emergência >6 horas desde a consulta inicial, o que não seria possível se essa consulta fosse imediatamente após a randomização. A hora do primeiro tratamento foi registrada
[ osf.io ] , mas nenhuma informação foi relatada. De acordo com
[ Forrest ], mensagens de WhatsApp e vídeo foram usados para o recrutamento, levantando a questão de como a medicação era entregue nos casos em que o recrutamento era feito online.
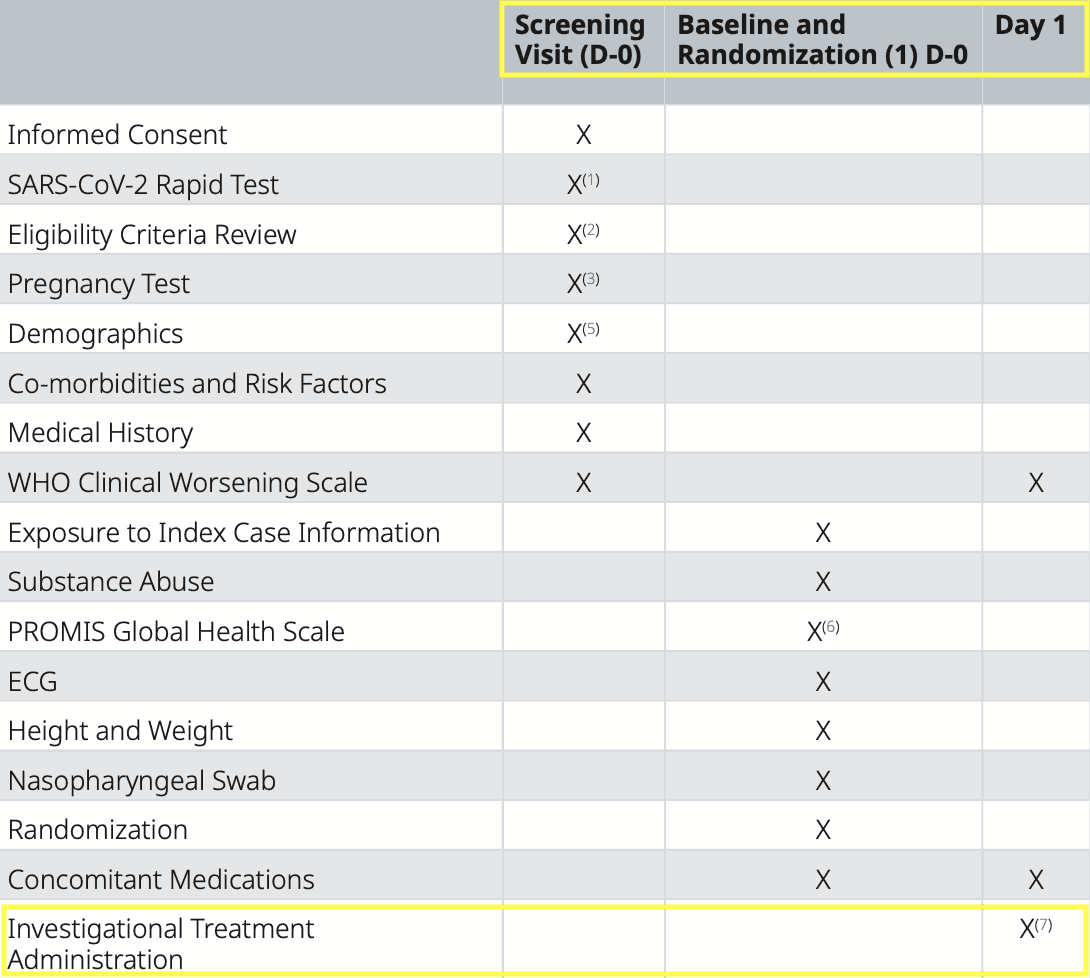
Atraso médio. O número médio relatado de dias desde os sintomas até a randomização provavelmente inclui apenas pacientes com início conhecido e, portanto, provavelmente subestima significativamente a média real, além de não incluir o tempo entre a randomização e o tratamento.
Carga viral não informada. O protocolo tem como resultado a alteração da carga viral, no entanto, apenas a depuração viral é relatada e sem detalhes (por exemplo, usar um valor alto de Ct teria relevância limitada).
Relato de dose incorreto, muitos pacientes com maior risco devido ao IMC podem ter recebido doses mais baixas por kg e apresentar menor eficácia. O artigo relata 400μg/kg por 3 dias, no entanto, o protocolo indica que isso foi apenas até 90kg, o que significa que a dose recebida para pacientes com alto IMC de alto risco foi ainda mais reduzida em relação à dosagem que já está muito abaixo das recomendações médicas para os pacientes dominantes. variante
[ twitter.com (T) ] . 50% dos pacientes tinham IMC ≥30. Eficácia muito maior foi observada no subgrupo de baixo IMC (RR 0,77 vs 0,98).
Concentração plasmática abaixo do valor eficaz conhecido. [ Krolewiecki ] mostram um efeito antiviral apenas com concentrações plasmáticas acima de 160ng/mL. A Figura S5 mostra que os autores esperavam que a concentração média ficasse bem abaixo desse nível
[ twitter.com (U) ]. As necessidades de dosagem provavelmente variam significativamente dependendo de muitos fatores, incluindo a variante encontrada, tempo de administração, modo de administração, genética do paciente, medicamentos concomitantes, SOC e a distribuição da infecção em diferentes tecidos. No entanto, a dose utilizada está muito abaixo do que é recomendado pelos médicos para o tratamento pós-infecção com a variante Gamma – cerca de 2,5 a 6,5 vezes menor, dependendo da recomendação e de qual estimativa de administração em jejum/alimentação é usada. O estudo utilizou administração em jejum, no entanto, as informações do produto da Merck relatam que
“a administração de 30 mg de ivermectina após uma refeição rica em gordura resultou em um aumento de aproximadamente 2,5 vezes na biodisponibilidade em relação à administração de 30 mg de ivermectina em jejum”. [ merck.com] . Além disso, o Dr. Craig Rayner, investigador sênior do estudo, publicou anteriormente uma pesquisa indicando que uma dose mais alta é necessária
[ sciencedirect.com ] , levantando a questão de por que a dose e a administração em jejum foram escolhidas, especialmente para o regime inicial de dose única.
Resultado primário fácil de jogar, selecionado após o braço de uma dose de ivermectina. O critério subjetivo “consulta de emergência por > 6 horas” mostra maior risco (RR 1,16), enquanto a hospitalização é menor (RR 0,83 por todas as causas, RR 0,84 COVID-19). Os resultados do desfecho primário foram definidos em 21 de março de 2021, após o braço de dose única de ivermectina. Dado o conhecido preconceito público de alguns pesquisadores, isso pode ter sido escolhido especificamente para reduzir a eficácia. Autores afirmam que o limite de 6h não incluiu o tempo de espera, porém a ficha de atendimento de emergência não menciona o tempo de espera, apenas registrando os tempos de apresentação e alta
[ osf.io ] .
Incluindo pacientes com doença renal crônica contraindicada. “Doença renal crônica em estágio IV ou em diálise” foi um critério de inclusão, no entanto, a ivermectina é contraindicada com doença renal
[ Arise , en.wikipedia.org , Nunes ] (nem sempre reconhecida e pode ser menos crítica com o uso de doses muito baixas para outros condições). De acordo com a Tabela 1 havia apenas 7 pacientes com DRC, porém dois números conflitantes são fornecidos no artigo da fluvoxamina
[ Reis (B) ] : A Tabela 1 relata 2 pacientes com DRC placebo – não está claro como a DRC foi imputada para mais 3 pacientes no menor grupo IVM. Além disso, a Figura 3 mostra 54 pacientes com DRC placebo para FLV.
Exigência de teste de antígeno. O protocolo indica que os pacientes com teste negativo podem ser incluídos se se tornarem positivos alguns dias depois, potencialmente resultando em um longo atraso não relatado entre a randomização e o tratamento, dependendo de como os investigadores interpretaram o protocolo. A exigência de um teste de antígeno positivo exclui a possibilidade de tratamento precoce em muitos casos – os testes têm taxas de falsos negativos muito altas nos estágios iniciais da infecção, e os sintomas podem aparecer antes que o teste se torne positivo.
Análise de subgrupo inconsistente. A análise de subgrupo apresentada é inconsistente com os planos e com o artigo de fluvoxamina, incluindo não apresentar subgrupos pré-especificados, apresentar subgrupos que não foram pré-especificados, apresentar subgrupos diferentes do artigo contemporâneo de fluvoxamina e modificar definições de subgrupos
[ twitter.com (V ) ] .
Falta análise. Os autores não fornecem a análise do tempo desde o início para mortalidade ou hospitalização, apenas a medida combinada, incluindo as visitas ao pronto-socorro, onde são observados resultados anômalos. Os autores não fornecem resultados por protocolo ou mITT para mortalidade ou hospitalização. Os resultados de mortalidade por protocolo foram fornecidos para o estudo complementar com fluvoxamina.
Faltam resultados. Muitos resultados especificados no protocolo parecem estar ausentes, incluindo o resultado co-primário de mortalidade por COVID-19 (apenas mortalidade por todas as causas é fornecida, detalhes específicos de EA não fornecidos), tempo até a falha clínica, dias com sintomas respiratórios, mortalidade devida a complicações pulmonares, mortalidade cardiovascular, avaliação da escala de sintomas COVID-19, avaliação da escala de piora clínica da OMS e mortalidade em 14 dias.
Erro de imputação. No artigo, os autores usam imputação na Tabela 1, mas não na Figura 2. Os autores também lançaram uma versão da Figura 2 com imputação
[ togethertrial.com (B) ] , onde os números para idade e IMC agora correspondem aos números imputados na Tabela 1. No entanto, os números de tempo desde o início são muito diferentes, com o braço de tratamento mostrando 302 pacientes por 0-3 dias, e a versão imputada da Figura 2 mostrando 367
[ doyourownresearch.substack.com (E) ] .
Falta informação de idade. De acordo com a Figura 2, faltam informações de idade em 98 pacientes
[ twitter.com (W) ] .
Reivindicação de financiamento desmentida pelo financiador. Um co-investigador principal relatou que o estudo foi interrompido porque eles ficaram sem financiamento, no entanto, isso é desmentido pela Rainwater Foundation, que informou que eles teriam dado mais dinheiro para terminar o estudo se os investigadores tivessem pedido
[ pierrekory.substack .com (B) ] .
Deturpação da recomendação de dosagem. Os investigadores deturparam um e-mail da FLCCC sobre a dosagem recomendada
[ pierrekory.substack.com (B) ] .
Diferenças inesperadas em dados ausentes. A idade é desconhecida para 98 pacientes, no entanto, de acordo com a Figura 2, o IMC está ausente para apenas 11 pacientes, o tabagismo é desconhecido para apenas 2 pacientes, a doença pulmonar é desconhecida para apenas um paciente e a doença cardiovascular é conhecida para todos os pacientes.
Alterações de protocolo no meio do estudo. Houve várias mudanças no protocolo no meio do estudo em 5 de julho de 2021
[ clinicaltrials.gov (E) ] . O número de pacientes para análise de carga viral foi reduzido, apenas para o braço de ivermectina. Os desfechos de morte por todas as causas, cardiovasculares e respiratórias foram excluídos (todas as causas foram relatadas). As exclusões foram modificadas para permitir a inscrição de pacientes vacinados nos últimos 14 dias. Os critérios de inclusão foram modificados para permitir a inscrição de jovens saudáveis — o critério
“febre >38C no início do estudo” foi adicionado, permitindo a inscrição independente do risco aumentado.
Plano de análise estatística datado após o início do estudo. O plano de análise estatística parece ser datado após o início do julgamento
[ twitter.com (X) ] .
O placebo por protocolo resulta muito diferente. O placebo de 3 doses parece ter sido muito mais eficaz
[ Marinos , twitter.com (Y) ] . Isso pode ser consistente com pacientes que receberam placebo acidentalmente recebendo tratamento.
Violação do protocolo de imputação. O protocolo especifica a imputação múltipla com até 20% de dados ausentes, porém a imputação foi feita com o tempo desde o início dos sintomas, que possui >23% de dados ausentes
[ twitter.com (Z) ] .
Duas contagens diferentes por protocolo. A Figura 1 mostra 228 por protocolo para o braço de controle, enquanto a Tabela 2 mostra 288. Isso foi modificado na atualização de 5 de abril sem explicação.
Contagens de eventos adversos conflitantes. As contagens de eventos adversos da Tabela 3 e da Tabela S6 não correspondem a nenhum grau, por exemplo, grau 1/2 na Tabela S6 mostra 82 para IVM, enquanto a Tabela 3 mostra 65
[ twitter.com (AA) ] . A atualização de 5 de abril alterou os eventos do grau 5 sem explicação, porém os outros graus permanecem conflitantes.
Pacientes com dosagem de 3 dias antes de 23 de março desaparecidos. O co-investigador principal escreveu em 6 de março que a dosagem de 3 dias estava sendo administrada e que a entrada dos ensaios clínicos estava desatualizada naquele momento
[ twitter.com (AB) ] . Este início precoce do braço de 3 doses resolveria uma grande inconsistência. A análise da randomização do estudo mostra que atingir a contagem de placebo de 3 dias requer pacientes a partir de 4 de março
[ doyourownresearch.substack.com (F) ], e seria lógico que o placebo de 3 dias e os braços ativos de 3 dias tivessem começado no mesmo dia. Isso reforça as preocupações existentes sobre quais pacientes foram incluídos na análise e adiciona perguntas adicionais sobre o que aconteceu com os pacientes antes de 23 de março e se os pacientes foram tratados antes da aprovação ética. A aprovação ética para a mudança de dose foi recebida em 21 de março de acordo com o artigo
[ twitter.com (AC) ] , com o documento do regulador datado de 15 de março
[ twitter.com (AD) ] .
Várias declarações falsas de investigadores. Houve várias declarações falsas de investigadores levantando questões sobre sua ética e a confiabilidade de seu trabalho
[ pierrekory.substack.com ] .
Os investigadores não respondem às preocupações. Depois que os detalhes dos principais erros de dados e violações de protocolo se tornaram conhecidos, os investigadores parecem ter parado de responder a todos os pesquisadores sobre sérias preocupações com o estudo
[ pierrekory.substack.com , twitter.com (E) ] (e ainda não nos responderam) .
Possivelmente o maior conflito de interesse financeiro de qualquer julgamento até hoje. Os conflitos de interesse divulgados incluem: Pfizer, Merck, Fundação Bill & Melinda Gates, Governo Australiano, Desenvolvimento de Medicamentos para Saúde Global, Novaquest, Regeneron, Astrazeneca, Daichi Sankyo, Organização de Pesquisa e Ciência da Commonwealth e Pesquisa de Cartões. Muitos conflitos de interesse parecem não relatados. Por exemplo, a Unitaid é um patrocinador
[ Harper , togethertrial.com (C) ] .
Análise feita por uma empresa que recebe pagamento e trabalha em estreita colaboração com a Pfizer. Todas as análises foram feitas por Cytel. A Cytel é uma empresa de modelagem estatística que ajuda as empresas farmacêuticas a obter aprovação — elas trabalham em estreita colaboração com a Pfizer
[ cytel.com ] . O software e os serviços da Cytel são usados pelas 30 maiores empresas farmacêuticas
[ cytel.com (B) ] .Um co-investigador principal trabalha para a Cytel e a Fundação Gates
[ empendium.com ] :
“A maior parte do tempo eu trabalho para uma empresa chamada Cytel, onde desenvolvo ensaios clínicos, predominantemente para a Fundação Bill & Melinda Gates”.Alegadamente, o centro do primeiro autor é financiado por empresas farmacêuticas, e investigadores independentes tentaram participar do estudo, mas foram negados
[ odysee.com (B) ] .A Fundação Gates é uma sócia fundadora da GAVI, que tirou anúncios do Google dizendo às pessoas para não usarem ivermectina
[ twitter.com (AE) ] e um dos principais financiadores da Unitaid, que pode ter modificado os resultados da meta-análise de Hill em um maneira que impediu a adoção
[ c19ivermectin.com , c19ivermectin.com (B) , twitter.com (H) ] .
Associado à MMS Holdings. O teste está associado à MMS Holdings
[ dcricollab.dcri.duke.edu ] , cuja missão inclui ajudar as empresas farmacêuticas a obter aprovação e projetar estudos científicos que as ajudem a obter aprovação. Um de seus clientes é a Pfizer
[ mmsholdings.com ] .
Certa. Um dos investigadores seniores foi o Dr. Craig Rayner, Presidente de Desenvolvimento Integrado de Medicamentos da Certara – outra empresa com uma missão semelhante à MMS Holdings. Eles afirmam em seu site que: “Desde 2014, nossos clientes receberam mais de 90% das aprovações de novos medicamentos e produtos biológicos pela FDA”. Um de seus clientes é a Pfizer
[ certara.com ] .
A variante local apresenta características muito diferentes. O julgamento ocorreu em uma área do Brasil onde a variante Gamma era proeminente. Clínicos brasileiros relatam que essa variante é muito mais virulenta e que é necessária uma dosagem significativamente maior e/ou tratamento precoce, como pode ser esperado para variantes em que o pico de carga viral é significativamente maior e/ou atingido mais cedo
Lista de financiamento incorreta . O artigo não inclui a Fundação Bill e Melinda Gates ou Unitaid como financiadores, no entanto, o protocolo mostra a Fundação Gates
[ gatesopenresearch.org (B) ] e o site mostra Unitaid
[ togethertrial.com (C) ] .
Faltam os resultados do braço de dose única. Os resultados para o braço de dose única de ivermectina não foram relatados.
Resultados anômalos da mesma região. Um investigador brasileiro local relata que o estudo foi conduzido quase no mesmo horário e local que o componente brasileiro do estudo do molnupiravir. Notavelmente, os EUA do molnupiravir se basearam na eficácia extraordinariamente mais alta observada no Brasil.
Projetado por Cytel. O teste foi desenvolvido pela Cytel, uma empresa que ajuda empresas farmacêuticas a obter aprovação e que trabalha em estreita colaboração com a Pfizer
[ cytel.com , cytel.com (C) ] . O software e os serviços da Cytel são usados pelas 30 maiores empresas farmacêuticas
[ cytel.com (B) ] .
Probabilidade Bayesiana de superioridade escondida no apêndice. A probabilidade bayesiana de figura de superioridade, apresentada no artigo principal para FLV, MET, HCQ, estava escondida no apêndice para IVM
[ twitter.com (AF) ] .
Razões conflitantes para mudança de dose. Foram dadas razões conflitantes para a mudança da dosagem de 1 dia para 3 dias. Em e-mail de 6 de março, o co-investigador principal diz que a mudança foi “baseada em ensaios emergentes da síntese de Andrew Hill”
[ twitter.com (AG) ] . O jornal diz que a mudança foi feita “com base no feedback de grupos de defesa”. Nenhum deles corresponde ao relatório de que a mudança de dosagem foi feita a pedido de um dos financiadores do estudo
[ pierrekory.substack.com ] .
Placebo não especificado. O placebo parece não estar especificado no artigo e no protocolo. O anúncio do teste inicial indicou que o placebo era a vitamina C
[ cytel.com (C) ] , que seria um tratamento ativo de acordo com os
resultados de 45 estudos (mortalidade RR 0,72 [0,59-0,88]). O braço de metformina relata o uso de talco, no entanto, a fluvoxamina e a ivermectina não parecem relatar detalhes do placebo, que podem ser diferentes, por exemplo, com base nas limitações do fabricante para combinar os comprimidos de tratamento ativo.
Alterações de protocolo anteriores. Existem dois protocolos publicados anteriormente, ambos são chamados de “versão 1”, nos referimos a eles como 1A (3/11/21
[ drive.google.com (C) ] ) e 1B (8/5/21
[ gatesopenresearch.org ] .1B exclui a análise de subgrupo por atraso no tratamento e exclui uma declaração exigindo aprovação prévia para alterações. 1B acrescenta a declaração: “nós hipotetizamos que pacientes mais jovens se beneficiarão mais do que pacientes mais velhos”.Os pacientes com 50 anos foram divididos em diferentes grupos na Tabela 1 e Figura 2 (≤50 vs. <50).Maior eficácia foi observada para pacientes >50 (RR 0,77) vs. pacientes ≤50 (RR 1,01).
Fonte de ivermectina não especificada. Os autores não especificam a fonte da ivermectina usada no estudo, mas especificam a fonte para o braço da fluvoxamina (Luvox, Abbott). Dependendo da fonte, a ivermectina tem sido relatada como de qualidade não confiável no Brasil.
100% de adesão relatada para placebo de 3 dias. Os números relatados indicam que houve 100% de adesão entre 288 pacientes atribuídos ao placebo de 3 dias, o que é inesperado
[ doyourownresearch.substack.com (F) , pierrekory.substack.com ] .
Os comentários a seguir são anteriores à publicação. Observamos que os autores afirmam que não incluíram pacientes antes do período de tempo para os pacientes com 3 doses de ivermectina, no entanto, isso entra em conflito com os dados relatados anteriormente, conforme as análises acima.O gráfico de randomização do ensaio não corresponde ao protocolo, sugerindo grandes problemas e indicando confusão substancial por tempo. Por exemplo, a semana de teste 43, a primeira semana para 3 doses de ivermectina, mostra ~3x pacientes atribuídos a ivermectina versus placebo
[ reddit.com ] . A eficácia do tratamento pode variar significativamente ao longo do tempo, por exemplo, devido à melhoria geral nos protocolos, mudanças na distribuição de variantes ou mudanças na conscientização do público e atrasos no tratamento.
[ Zavascki ] mostram mortalidade dramaticamente mais alta para variantes Gamma vs não Gamma (mortalidade de 28 dias desde o início dos sintomas aHR 4,73 [1,15-19,41]), e a prevalência da variante Gamma variou drasticamente ao longo do estudo
[ ourworldindata.org] . Isso introduz confusão por tempo, o que é comum em estudos retrospectivos de COVID-19 e muitas vezes obscurece a eficácia (muitas retrospectivas têm mais pacientes no grupo de tratamento mais cedo, quando os protocolos gerais de tratamento foram significativamente piores).De acordo com esta análise
[ reddit.com ] , o número total de pacientes para os grupos de ivermectina e placebo não parece corresponder aos totais na apresentação (os números para a correspondência de braço de fluvoxamina) – alcançar o número relatado para ivermectina exigiria incluir alguns dos pacientes atribuídos a uma dose única de ivermectina. Atingir o número de placebo requer a inclusão de pacientes com placebo do período de dose única de ivermectina muito anterior e do período inicial de duas semanas, quando os pacientes com zero ivermectina foram designados. Se esses participantes anteriores fossem acidentalmente incluídos no grupo de controle, isso mudaria drasticamente os resultados em favor do grupo de controle de acordo com as mudanças na prevalência da variante Gamma.
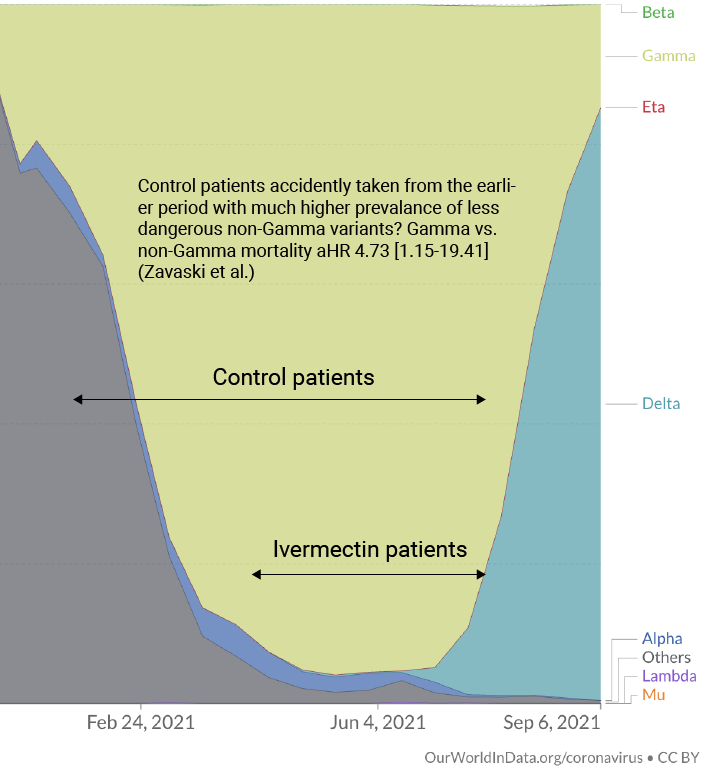 Um investigador do Brasil observa que a variante gama tornou-se predominante no estado de Minas Gerais mais tarde do que no resto do país, com a época em que a gama prevaleceu para os locais de teste sendo mais alinhada com o início do braço da ivermectina
Um investigador do Brasil observa que a variante gama tornou-se predominante no estado de Minas Gerais mais tarde do que no resto do país, com a época em que a gama prevaleceu para os locais de teste sendo mais alinhada com o início do braço da ivermectina
[ ufmg. br ] . Devido às diferenças substanciais no curso da doença e risco entre as variantes, os autores precisam considerar apenas os pacientes recrutados durante o mesmo período de tempo.O atraso no tratamento é atualmente desconhecido, no entanto, o protocolo permite a inclusão muito tardia e um estudo complementar relatou principalmente o tratamento tardio. A mortalidade geral é alta para pacientes ambulatoriais com mais de 18 anos. Os resultados podem ser afetados pelo tratamento tardio, SOC pobre e podem ser específicos para variantes locais
[ Faria , Nonaka , Sabino ] . O tratamento foi administrado com o estômago vazio, reduzindo bastante a concentração tecidual esperada
[ Guzzo ] e tornando a dose efetiva cerca de 1/5 da prática clínica atual. O estudo foi realizado em Minas Gerais, Brasil, que teve uso comunitário substancial de ivermectina
[ otempo.com.br ], e o uso prévio de ivermectina não está listado nos critérios de exclusão.Este estudo usa um resultado primário suave, facilmente sujeito a viés e inflação de eventos em ambos os braços (por exemplo, observar > 6 horas independente da indicação). Há também um critério de inclusão incomum: “pacientes com internação prevista de <= 5 dias”. Isso é semelhante a “pacientes com menor probabilidade de precisar de tratamento além do SOC para se recuperar” e facilitaria muito a redução do efeito observado. Isso não está em nenhum dos protocolos publicados.Os ECRs têm um viés fundamental contra encontrar um efeito para intervenções amplamente disponíveis – os pacientes que acreditam que precisam de tratamento são mais propensos a recusar a participação e aceitar a intervenção
[ Yeh ] , ou seja, os ECRs são mais propensos a inscrever participantes de baixo risco que não precisam de tratamento para se recuperar (isso não se aplica ao teste farmacêutico típico de um novo medicamento que, de outra forma, não está disponível). Este estudo foi realizado em uma comunidade onde a ivermectina é amplamente conhecida e usada.Os resultados do mesmo estudo para um tratamento anterior foram inicialmente relatados como RR 1,0 [0,45-2,21]
[ ajtmh.org ] , enquanto o artigo final relatou algo muito diferente — HR 0,76 [0,30-1,88]
[ jamanetwork.com ] .O projeto, a análise e a apresentação do estudo, juntamente com declarações públicas e privadas anteriores, sugerem viés do investigador. Desenho: incluindo tratamento muito tardio, dia adicional antes da administração, operação em região com alto uso comunitário, especificando administração com o estômago vazio, limitando o tratamento a 3 dias, usando critério de inclusão suave e resultado primário suave, facilmente sujeito a viés. Análise: os autores realizam análises excluindo eventos logo após a randomização para fluvoxamina, mas não para ivermectina, e relatam resultados de carga viral para fluvoxamina, mas não para ivermectina. Apresentação: descrevendo falsamente efeitos positivos, mas não estatisticamente significativos, como “nenhum efeito, seja o que for”
[ Amrhein , odysee.com (C) ] . Declarações anteriores:
[odysee. com (C) ] .O investigador local brasileiro também relata que a nitazoxanida foi testada no mesmo local, no entanto, muito poucos pacientes relataram descoloração da urina, enquanto 100% devem apresentar esse efeito colateral; e que a observação de 6 horas é uma má escolha porque é quase impossível ficar menos de 6 horas no Brasil.Para questões adicionais, consulte:
[ covid19criticalcare.com , doyourownresearch.substack.com (G) , longhaulwiki.com , Marinos , Marinos (B) , stevekirsch.substack.com , trialsitenews.com (C) , twitter.com (AH) , twitter.com (AI) , twitter.com (AJ) , twitter.com (AK) ] . Protocolos, aprovações e planos de análise estatística podem ser encontrados aqui
[ togethertrial.com (D) ] .NCT04727424.
Envie correções ou atualizações .
López-Medina et al.Uma carta aberta, assinada por mais de 100 médicos, concluindo que este estudo é fatalmente falho, pode ser encontrada em
[ jamaletter.com ] .
Este é um RCT baseado em pesquisa telefônica com pacientes de baixo risco, 200 ivermectina e 198 controles, mostrando menor mortalidade, menor progressão da doença, menor escalada de tratamento e resolução mais rápida dos sintomas com o tratamento, sem atingir significância estatística. Os autores acham que os resultados deste estudo por si só não suportam o uso de ivermectina. No entanto, os efeitos são todos positivos, especialmente para desfechos graves que não conseguem alcançar significância estatística com o número muito pequeno de eventos na população de baixo risco.Os ECRs têm um viés fundamental contra encontrar um efeito para intervenções amplamente disponíveis – os pacientes que acreditam que precisam de tratamento são mais propensos a recusar a participação e fazer a intervenção
[ Yeh ] , ou seja, os ECRs são mais propensos a inscrever participantes de baixo risco que fazem não precisa de tratamento para se recuperar (isso não se aplica ao teste farmacêutico típico de um novo medicamento que de outra forma não está disponível). Este estudo foi realizado em uma comunidade onde a ivermectina estava disponível sem receita e muito conhecida e usada.Com a população de pacientes de baixo risco, há pouco espaço para melhora com um tratamento eficaz – 59/57% (IVM/controle) recuperou nos primeiros 2 dias para “sem sintomas” ou “não hospitalizado e sem limitação de atividades”; 73/69% em 5 dias. Menos de 3% de todos os pacientes já se deteriorou.O desfecho primário foi alterado no meio do estudo, originalmente era deterioração clínica, que é mais significativa e mostra maior benefício. O novo desfecho de resolução dos sintomas inclui “não hospitalização e nenhuma limitação de atividades” como um desfecho negativo e não é muito significativo em termos de avaliar o quanto o tratamento reduz desfechos graves. O uso dessa medida pode invalidar completamente os resultados – por exemplo, um tratamento que elimina todos os sintomas do COVID-19, mas tem um evento adverso menor temporário, pode ser visto como pior.Os autores afirmam que “relatórios preliminares de outros ensaios randomizados de ivermectina como tratamento para COVID-19 com resultados positivos ainda não foram publicados em periódicos revisados por pares”, no entanto, havia 8 ECRs revisados por pares com efeitos positivos publicados antes deste artigo( e 19 estudos revisados por pares com efeitos positivos).Os autores aconselharam tomar ivermectina com o estômago vazio, reduzindo a concentração do tecido pulmonar em ~ 2,5x
[ Guzzo ] .76 pacientes foram excluídos devido a pacientes controle que receberam ivermectina. No entanto, houve uma porcentagem semelhante de eventos adversos como diarreia, náusea e dor abdominal em ambos os grupos de tratamento e controle. Estes são potenciais efeitos colaterais não graves do tratamento e sugerem que é possível que muito mais pacientes controle tenham recebido algum tipo de tratamento.A ivermectina foi amplamente utilizada na população e disponível OTC no momento do estudo. O protocolo do estudo excluiu apenas pacientes com uso prévio de ivermectina dentro de 5 dias, no entanto, outros estudos frequentemente monitoram os efeitos 10+ dias após a última dose
[ osf.io (B) ] .Este estudo supostamente tem uma questão ética em que os participantes foram informados que a droga do estudo era “D11AX22”
[ trialsitenews.com (D) ] . O editor-chefe do JAMA inicialmente se ofereceu para ajudar com esse problema, mas depois indicou que “o JAMA não revisa os formulários de consentimento”, no entanto, o autor principal confirmou o problema
[ francesoir.fr , trialsitenews.com (E) , trialsitenews .com (F) ] .O protocolo do estudo permite especificamente “o uso de outros tratamentos fora dos ensaios clínicos”. O artigo não fornece informações sobre quais outros tratamentos foram usados, mas outros tratamentos eram comumente usados na época. Além disso, o grupo controle se saiu cerca de 5x melhor do que o previsto para deterioração, sugerindo também que os pacientes controle usaram algum tipo de tratamento. Os pacientes que se inscrevem em tal estudo podem ter maior probabilidade de aprender e usar outros tratamentos, especialmente porque não sabem se estão recebendo a medicação do estudo.O protocolo do estudo foi alterado 4 vezes. As alterações 2-4 são apresentadas, mas a alteração 1 está em falta. A alteração 2 aumentou os critérios de inclusão para dentro de 7 dias após o início, incluindo mais pacientes em estágio avançado e reduzindo a eficácia esperada. O protocolo do estudo lista “a duração do oxigênio suplementar” como resultado, mas os resultados para esse resultado estão ausentes.Subsídios e/ou honorários pessoais, inclusive em alguns casos durante a realização do estudo, foram fornecidos pela Sanofi Pasteur, GlaxoSmithKline, Janssen, Merck e Gilead. Para mais detalhes veja
[ trialsitenews.com (G) ] .Para outras questões confusas veja
[ osf.io (C) ] e questões adicionais podem ser encontradas nos comentários do artigo
[ jamanetwork.com (B) ] . A reanálise dos dados brutos mostrou um efeito positivo significativo
[ twitter.com (AL) ] .
Envie correções ou atualizações .
Vallejos et ai.Com apenas 7% de hospitalização, este estudo é fraco. O estudo inclui principalmente pacientes de baixo risco que se recuperam rapidamente sem tratamento, deixando espaço mínimo para melhorias com o tratamento. 74 pacientes apresentaram sintomas por >= 7 dias e mais de 25% dos pacientes foram hospitalizados em 1 dia (Figura S2). Entre os 7 pacientes que necessitaram de ventilação, os autores observam que a necessidade mais precoce no grupo de ivermectina pode ser devido àqueles pacientes com maior gravidade no início do estudo. No entanto, os autores sabem a resposta para isso – não está claro por que não é relatado. Houve mais eventos adversos no grupo placebo do que no grupo ivermectina, sugerindo um possível problema com a dispensação ou uso de medicação não experimental.O ensaio de profilaxia complementar
[ IVERCOR PREP ] , que relatou resultados mais positivos, ainda não foi publicado formalmente, sugerindo um viés de publicação negativo.Os autores pré-especificam a análise multivariada, mas não a apresentam, porém a análise multivariada pode alterar significativamente os resultados. Considere, por exemplo, se apenas alguns pacientes extras no grupo da ivermectina estivessem em estado grave com base na SpO2 basal. A menor SpO2 média no grupo da ivermectina e o menor tempo de ventilação são consistentes com este caso. Além disso, há 14% mais pacientes do sexo masculino no grupo da ivermectina.Uma porcentagem extremamente grande de pacientes (55%) foi excluída com base no uso de ivermectina nos últimos 7 dias. No entanto, a ivermectina pode manter a eficácia por muito mais tempo (por exemplo, a atividade antiparasitária pode persistir por meses
[ Canga ] ). Um número significativo de pacientes também pode deturpar seu uso anterior e futuro – a população está claramente ciente da ivermectina, e pacientes com doença em progressão podem ser motivados a tomá-la, sabendo que podem estar no grupo de controle. Outro relatório afirma que 12.000 pacientes foram excluídos por uso recente de ivermectina
[ scidev.net ] ).Os ECRs têm um viés fundamental contra encontrar um efeito para intervenções amplamente disponíveis – os pacientes que acreditam que precisam de tratamento são mais propensos a recusar a participação e fazer a intervenção
[ Yeh ] , ou seja, os ECRs são mais propensos a inscrever participantes de baixo risco que fazem não precisa de tratamento para se recuperar (isso não se aplica ao teste farmacêutico típico de um novo medicamento que de outra forma não está disponível). Este ensaio foi realizado em uma comunidade onde a ivermectina era amplamente conhecida e usada.Para outras questões, veja
[ trialsitenews.com (H) ] .
Envie correções ou atualizações .
Beltran Gonzalez et ai.Outro estudo relata resultados em um grupo maior de pacientes no mesmo hospital, mostrando mortalidade de ivermectina RR 0,81 [0,53-1,24]
[ Guzman ] .Questões foram levantadas sobre este estudo e o término antecipado do estudo e descontinuação dos tratamentos, porque as estatísticas do hospital mostram uma taxa de mortalidade de casos dramaticamente menor (~ 75%) durante o período do estudo
[ web.archive.org (B) ] (dados de
[ gob.mx ] ).
| Encontro | Casos | Mortes | CFR |
| 3/2020 | 2 | 1 | 50% |
| 4/2020 | 4 | 1 | 25% |
| 5/2020 | 13 | 1 | 8% |
| 6/2020 | 37 | 2 | 5% |
| 7/2020 | 65 | 5 | 8% |
| 8/2020 | 79 | 23 | 29% |
| 9/2020 | 54 | 12 | 22% |
| 10/2020 | 62 | 21 | 34% |
| 11/2020 | 80 | 26 | 33% |
| 12/2020 | 41 | 13 | 32% |
Várias outras inconsistências foram relatadas
[ Chamie ] .Embora os dados deste estudo estejam disponíveis e tenham sido compartilhados com um grupo anti-tratamento, pesquisadores independentes não conseguiram obter os dados para verificação
[ Chamie , twitter.com (AM) ] .
Envie correções ou atualizações .
Popp et ai.Esta meta-análise foi projetada para excluir a maioria dos estudos. Os autores selecionam um pequeno subconjunto de estudos, com a maioria dos resultados baseados em apenas 1 ou 2 estudos. Os autores dividem os estudos que dilui os efeitos e resulta em falta de significância estatística para a maioria dos desfechos. Os autores realizam mais de 16 meta-análises com muito poucos estudos em cada análise e não combinam as evidências de todos os estudos. No entanto, podemos considerar a probabilidade dos resultados observados em todos os resultados.Os autores encontram resultados positivos para 11 dos 12 desfechos primários de eficácia com eventos, ou 16 dos 18 incluindo desfechos secundários. Um dos resultados primários e dois dos resultados secundários mostram melhorias estatisticamente significativas isoladamente. Se assumirmos independência, a probabilidade de que 11+ dos 12 resultados primários de eficácia sejam positivos para um tratamento ineficaz é
p = 0,003. Para 16+ de 18 resultados, obtemos
p = 0,0007. Essa análise simples não leva em consideração a magnitude dos efeitos positivos ou a dependência devido a alguns estudos que contribuem com múltiplos resultados, no entanto, a observação sugere que uma análise completa das evidências combinadas provavelmente mostrará eficácia.O estudo é inteiramente retrospectivo na versão atual. O protocolo é datado de 20 de abril de 2021, e o estudo mais recente incluído é de 9 de março de 2021. O protocolo foi modificado após a publicação para incluir um resultado próximo a nulo (
[ Beltran Gonzalez ] “pacientes que receberam alta sem deterioração respiratória ou óbito em 28 dias”), portanto, o protocolo atual é datado de 28 de julho de 2021.Os autores excluíram muitos estudos por exigirem resultados em um momento específico, por exemplo, mortalidade, ventilação, etc. exigiram resultados exatamente em 28 dias. Os autores excluíram todos os estudos de profilaxia exigindo resultados exatamente em 14 dias.Estudos comparativos com outros medicamentos foram excluídos, porém esses estudos confirmam a eficácia da ivermectina. O único caso em que eles podem exagerar a eficácia da ivermectina é se o outro medicamento for prejudicial. Há alguma evidência disso para dosagem excessiva/uso em estágio muito tardio, no entanto, isso não se aplica a nenhum dos estudos aqui.Foram excluídos os estudos que utilizaram o tratamento combinado, mesmo quando se sabe que os outros componentes têm efeito mínimo ou nenhum. 3 de 4 ECRs com tratamento combinado usam doxiciclina em adição
[ Butler ] . Outros estudos foram excluídos por exigirem confirmação por PCR.Os autores são inconsistentes em relação aos comparadores ativos. Eles afirmam que a hidroxicloroquina “não funciona”, mas excluíram ensaios comparando a ivermectina a um medicamento que eles consideram inativo. Por outro lado, o remdesivir foi um comparador aceitável, embora seja considerado um padrão de tratamento eficaz em alguns locais
[ Fordham ] .Os autores não reconhecem que os domínios do Risco de Viés (RoB), como o cegamento, são muito menos importantes para o resultado objetivo da mortalidade.Os autores incluem
[ Beltran Gonzalez ] como COVID-19 “moderado”, no entanto, os pacientes neste estudo estavam em estado grave (linha de base SatO2 83).
[ Fordham ] resume vários problemas:
•afirmações não comprovadas de reações adversas à ivermectina e a afirmação desatualizada de que uma dosagem insegura seria necessária para ser eficaz;
•uma demanda por PCR ou teste de antígeno, sem análise de confiabilidade e não disponível universalmente mesmo em países desenvolvidos no início da pandemia;
•contradições nos critérios de exclusão, incluindo placebo e comparadores aprovados de SoC, mas rejeitando a hidroxicloroquina, embora considerada ineficaz (e um SoC aprovado em algumas jurisdições);
•inclusão de comparadores “considerados ativos” excluindo os “potencialmente ativos”;
•exclusão de terapias combinadas, embora a norma entre os clínicos;
•a rejeição de outros ECRs quando o objetivo é um “perfil de evidência completo”;
•pontos de tempo arbitrários para medidas de resultados, excluindo ensaios não conformes;
•fragmentação dos dados por local de atendimento sob diversos critérios de internação;
•o foco resultante em uma pequena fração da evidência clínica disponível, com a maioria das comparações baseadas em estudos únicos sem meta-análise possível;
•uma comparação de mortalidade de pacientes internados resultante com menos pacientes do que um estudo combinado com fatores de confusão de junho de 2020;
•nenhuma conclusão sobre o desfecho principal da mortalidade, quando várias linhas de evidência de outros lugares (incluindo a OMS) apontam para uma vantagem significativa na mortalidade.A Cochrane era respeitável no passado, mas agora é controlada por interesses farmacêuticos. Por exemplo, veja as notícias relacionadas à expulsão do fundador Dr. Gøtzsche e a renúncia em massa associada de membros do conselho em protesto
[ blogs.bmj.com , bmj.com , en.x-mol.com ] . Para outro exemplo de viés, veja
[ ebm.bmj.com ] .O grupo BiRD fez o seguinte comentário inicial: “A revisão Cochrane de ontem surpreendentemente não adota uma abordagem pragmática comparando ivermectina versus não ivermectina, como na maioria das outras revisões existentes. Ela usa uma abordagem granular semelhante à da OMS e do falho Roman et al. artigo, dividindo os estudos e, assim, diluindo os efeitos. Consequentemente, as conclusões incertas não acrescentam nada à base de evidências. Uma ofuscação adicional das evidências sobre a ivermectina e um exemplo de desperdício de pesquisa. Conflitos de financiamento de interesses dos autores e da revista em questão devem ser examinado.”
Envie correções ou atualizações .
Romano et ai.Esta é uma meta-análise severamente falha. Uma carta aberta assinada por 40 médicos detalhando erros e falhas e solicitando retratação pode ser encontrada em
[ trialsitenews.com (I) ] . Veja também
[ bird-group.org ] .Os autores escolhem incluir apenas 4 estudos relatando mortalidade diferente de zero e inicialmente alegaram um RR de mortalidade de 1,11 [0,16-7,65]. No entanto, eles relataram valores incorretos para Niaee et al., alegando um RR de 6,51 [2,18-19,45], quando o RR correto para Niaee et al. é 0,18 [0,06-0,55]. Após a correção, seus estudos selecionados mostram uma redução de mortalidade >60%, no entanto, os autores não corrigiram a conclusão.Da mesma forma, para a depuração viral e NCT04392713, eles relatam 20/41 de tratamento, 18/45 de controle, enquanto os números corretos de depuração do dia 7 são 37/41 e 20/45 (soma da depuração @ 72 horas e @ 7 dias), ou 17/ 41 e 2/45 @ 72 horas.O tempo de internação de Niaee et al. também é relatado incorretamente, mostrando uma duração menor para o grupo controle.Todos os erros estão em uma direção – relatando incorretamente eficácia inferior à real para a ivermectina. Os autores afirmam incluir todos os ECRs excluindo a profilaxia, no entanto, eles incluem apenas 10 dos 24 ECRs sem profilaxia (28 incluindo a profilaxia no momento da publicação). Os autores realmente fazem referência a meta-análises que incluem os ECRs ausentes, portanto, eles devem estar cientes dos ECRs ausentes.A estratégia de pesquisa do PubMed fornecida está sintaticamente incorreta. Para erros adicionais, consulte
[ pubpeer.com ] . Veja também
[ roundingtheearth.substack.com ] .Os autores afirmam que não têm conflitos de interesse no medRxiv, porém a afiliação do Dr. Pasupuleti é a Cello Health, cujo site
[ cellohealth.com ] observa que eles fornecem serviços como
“estratégia comercial de marca e portfólio para biotecnologia e farmacêutica” e que seus clientes são
“24 das 25 maiores empresas farmacêuticas” .
Envie correções ou atualizações .
Envie atualizações e correções na parte inferior desta página.12/06: Adicionamos
[ Naggie ] .01/06: Atualizamos a
análise do Together Trial .30/05: Adicionamos
[ George ] .30/05: Atualizamos a
análise do Together Trial .27/05: Adicionamos
[ Rocha ] .25/04:
Atualizações da discussão do SSC .17/04: Adicionamos uma seção sobre pesquisa pré-clínica.16/04: Adicionamos a discussão da
recomendação do NIH .09/04: Atualizamos a
análise do Together Trial .08/04: Adicionamos
[ Ravikirti ] .4/5: Adicionamos discussão de pré-impressão com base em
[ Zeraatkar ] e atualizamos a
análise do Together Trial .4/2: Atualizamos a
análise do Together Trial .30/03: Atualizamos
[ Reis ] para a versão da revista.21/03: Atualizações da discussão sobre
Strongyloides .3/3: Atualizamos
[ Beltran Gonzalez ] para a versão da revista.3/2: Adicionamos
[ Soto ] .28/02: Adicionamos
[ Efimenko ] .25/02: Adicionamos
[ Thairu ] .23/02: Atualizamos
[ Mayer ] para a versão da revista.18/02: Atualizamos
[ Lim ] para a versão da revista.2/2: Adicionamos
[ Manomaipiboon ] .28/01: Adicionamos
[ de Jesús Ascencio-Montiel ] .21/01: Adicionamos
[ Zubair ] .17/01: Adicionamos uma explicação de por que a
análise de gráfico de funil não é válida neste caso.1/16: Adicionamos a análise de depuração viral RCT e corrigimos os resultados de casos sintomáticos ausentes na análise de casos.15/01: Atualizamos
[ Kerr ] para a versão do jornal.1/15: Corrigimos os tamanhos dos grupos de hospitalização em
[ Buonfrate ] .13/01: Adicionamos
[ Abbas , Baguma ] .1/11: Atualizamos
[ Kerr ] para os resultados mais recentes e adicionamos a discussão de
[ Beltran Gonzalez ] .1/7: Atualizamos
[ Buonfrate ] para a versão do jornal e atualizamos
[ Kerr ] para os resultados mais recentes.31/12: Adicionamos
[ Shimizu ] .29/12: Adicionamos
[ Mustafa ] .26/12: Atualizamos
[ Kerr ] para a versão revisada do artigo.16/12: Adicionamos
[ Jamir ] .11/12: Adicionamos
[ Kerr ] .8/12: Adicionamos a análise do número de grupos de pesquisa independentes que relataram resultados positivos estatisticamente significativos.5/12: Adicionamos
[ Ferreira ] .5/12: Adicionamos
[ Rezk ] .12/3: Uma nota sobre Bernigaud: a correção de continuidade usa o recíproco do braço contrastante
[ Sweeting ] , conforme detalhado no apêndice. Anteriormente, limitamos o tamanho do grupo de controle ao mostrar o número total de pacientes, mas isso era confuso para pessoas que não liam os detalhes, conforme discutido abaixo. O tamanho total do grupo sempre foi usado ao calcular o RR.1/12: Atualizações da discussão sobre
Strongyloides .30/11: Corrigimos
[ Ghauri ] para usar a contagem de eventos.24/11: Adicionamos
[ Ozer ] .24/11: Atualizações da discussão do
SSC .21/11: Atualizações da discussão sobre
Strongyloides .20/11: Atualizações da discussão sobre
Strongyloides .19/11: Adicionamos a análise por
prevalência de Strongyloides e a atualizamos para corresponder à classificação revisada usada na análise comparável.19/11: Adicionamos análises de exclusão adicionais nos
dados suplementares .18/11: Incluímos incorretamente
[ López-Medina ] como um estudo que não relata o uso de esteróides, porém eles relatam 6% de uso no grupo controle.18/11: Adicionamos
[ Samajdar ] .17/11:
Resposta SSC.16/11: Atualizações da discussão.11/12: Agora mostramos o número de estudos que relatam resultados estatisticamente significativos para qualquer desfecho, desfechos primários e o desfecho mais grave.9/11: Atualizações da discussão.5/11: Adicionamos a discussão de
Strongyloides , comparação com a recente
aprovação do molnupiravir e notas sobre
o recrutamento para ensaios remotos de tratamento tardio em ambulatório .3/11: Adicionamos
[ Lim ] .11/3: Atualizações da discussão.29/10: Atualizações de discussão, incluindo
análise GMK de vitamina D.28/10: Atualizações da discussão.26/10: Atualizamos a
resposta da GMK.24/10: Adicionamos análises de exclusão adicionais para resultados individuais.21/10: Adicionamos
[ Borody ] .19/10: Atualizações da discussão.18/10:
[ Ghauri ] foi atualizado para a versão do jornal.16/10: Adicionamos um gráfico de resumo para todos os resultados.13/10: Adicionamos análise de resultado primário e análises de exclusão adicionais. Niae et ai. foi relatado como pendente de retratação e foi removido. Atualização de 27/10: a revista relatou que isso está incorreto – nenhuma retratação está pendente.10/11: Atualizações da discussão. Niae et ai. exclusão. Atualizações das
notas do estudo, incluindo discussão de
Vallejos et al. e questões adicionais no
Together Trial . Discussão do
viés inerente em ECRs para intervenções amplamente disponíveis .8/10: Atualizações da discussão.7/10: Samaha et al. foi relatado como pendente de retratação e foi removido. Não houve alteração significativa nos resultados.4/10: Atualizações da discussão da Merck.29/09: Corrigimos um erro de exibição que fazia com que alguns pontos estivessem faltando na
Figura 4 .27/09: Adicionamos
[ Mayer ] .24/09: Adicionamos um gráfico de variantes ao longo do tempo para a discussão do
Together Trial e corrigimos a discussão do resultado para Popp et al.22/09: Atualizações da discussão.20/09: Atualizações da discussão.18/09: Adicionamos
[ Buonfrate ] , e atualizamos a discussão do Julgamento Juntos.17/09: Adicionamos notas de estudo.15/09: Atualizações da discussão.14/09: Atualizações da discussão da FDA.9/9: Adicionamos análise de sensibilidade para calcular o número mínimo de estudos que precisam ser excluídos para evitar mostrar eficácia. Atualizações de discussão.07/09: Atualizações de discussão.06/09: Corrigimos
[ Espia-Hernandez ] para usar o tempo de recuperação relatado e adicionamos resultados ausentes de recuperação e eliminação viral.9/3: Atualizamos a discussão e excluímos Carvallo et al. na análise de exclusão.27/8: Atualizamos
[ Morgenstern (B) ] com a versão do artigo para o periódico.26/08: Atualizamos
[ Mohan ] com a versão do artigo no periódico.16/08: Atualizamos
[ Reis ] com a contagem de eventos.15/8: Atualizamos a discussão e tornamos o resumo mais conciso.8/12: Adicionamos
[ Elavarasi , Reis ] .8/8: Atualizamos a discussão nas respostas.8/6: Atualizamos
[ Behera (B) ] com a versão do artigo do periódico.05/08: Adicionamos
[ Mondal ] .8/4: Adicionamos a discussão da recomendação do FDA.8/3: Adicionamos discussão na seção de
respostas .02/08: Adicionamos análise restrita a resultados sérios e análise restrita a recuperação, e adicionamos discussão na seção de
respostas .31/07: Adicionamos discussão na seção de
respostas relacionadas a evidências
in vitro e concentrações terapêuticas.29/07: Adicionamos discussão na seção de
respostas .20/07: Atualizamos
[ Hashim ] com a versão do artigo no periódico.16/07: Atualizamos
[ Ravikirti (B) ] com a versão de revista do artigo.15/07: Elgazzar et al. foi retirado pelo servidor de pré-impressão e foi removido.09/07: Adicionamos
[ Hazan ] .08/07: Atualizamos o
[ Cadegiani ] para a versão da revista.7/6: Anteriormente, limitamos o tamanho do grupo de controle para
[ Bernigaud ] ao calcular o número total de pacientes, no entanto, isso foi confuso para muitas pessoas que não leram os detalhes. Agora mostramos as contagens originais e observamos o tamanho maior do grupo de controle no texto.03/07: Adicionamos
[ Vallejos ] .7/2: Atualizamos Niaee et al. para a versão do jornal.21/06: Adicionamos mais informações ao resumo.19/06: Atualizamos
[ Bryant ] para a versão do jornal.19/06:
[ Beltran Gonzalez ] foi incluído incorretamente na análise revisada por pares.18/06: Adicionamos
[ Krolewiecki ] .15/06: Adicionamos
[ Aref ] .07/06: Adicionamos
[ Hariyanto ] .05/06: Adicionamos
[ Ahsan ] .02/06: Adicionamos
[ Abd-Elsalam ] .31/05:
[ Biber ] foi atualizado para a pré-impressão.26/05: Samaha et al. foi atualizado para a versão do jornal.18/05: Adicionamos análise da
recomendação da Merck .17/05: Adicionamos
[ Szente Fonseca ] .15/05: Atualizamos a discussão da análise da OMS.13/05: Atualizamos o
[ Mahmud ] para a versão do jornal.5/10: Adicionamos
[ Faisal ] .5/10: Adicionamos informações adicionais no resumo.08/05: Adicionamos
[ Merino ] .07/05 : Atualizamos
[ Shahbaznejad ] para a versão do jornal, que inclui resultados adicionais não relatados anteriormente.5/6: Atualizamos
[ Chahla ] para a pré-impressão do Research Square.5/6: Adicionamos uma comparação das recomendações do CDC.5/6: Adicionamos ventilação mecânica e análise de admissão na UTI.5/6: Atualizamos a discussão com base na revisão por pares, incluindo discussão sobre heterogeneidade, análise de sensibilidade baseada em exclusão e critérios de pesquisa.5/5: Atualizamos
[ Okumuş ] para o jornal.5/5: Anteriormente, limitamos o tamanho do grupo de controle em
[ Bernigaud ] para ser igual ao grupo de tratamento para o cálculo do número total de pacientes. Isso agora também é refletido e observado nas parcelas florestais.5/4: Adicionamos
[ Loue ] .30/04: Adicionamos a análise da meta-análise da OMS e atualizamos
[ Kory ] para a versão do periódico.28/04: Adicionamos os resultados da meta-análise da OMS para comparação.27/04: Adicionamos uma análise restrita aos resultados de internação e uma comparação com a base de evidências usada na aprovação de outros tratamentos para COVID-19.26/4: Adicionamos notas sobre heterogeneidade.25/04: Atualizamos
[ Biber ] para os últimos resultados relatados na Conferência Internacional de Ivermectina para Covid.18/04: Atualizamos
[ Morgenstern ] para a pré-impressão.16/04: Adicionamos
[ Morgenstern ] .14/04: Adicionamos
[ Ver ] .10/04 : Adicionamos
[ Kishória ] .09/04: Corrigimos uma entrada duplicada para
[ Bukhari ] .4/7: Identificamos estudos onde o mínimo de detalhes está atualmente disponível nas parcelas florestais.4/5: Adicionamos
[ Mourya ] .4/4: Adicionamos contagens de eventos às parcelas florestais.31/03: Atualizamos
[ Chahla (B) ] para a pré-impressão.30/03: Adicionamos
[ Chahla ] .28/03: Destacamos e adicionamos discussão para estudos que usam tratamentos combinados.26/03: Adicionamos
[ Tanioka ] .25/03: Adicionamos
[ Huvemek ] .17/03: Adicionamos
[ Nardelli ] .12/03: Adicionamos
[ Bryant , Roy ] .10/03: Adicionamos
[ Pott-Junior ] .3/6: Adicionamos
[ Chowdhury ] e identificamos estudos que comparam com outro tratamento.3/5: Adicionamos a discussão dos efeitos agrupados (mostramos os efeitos agrupados e os resultados individuais).3/4: Adicionamos
[ López-Medina ] e adicionamos mais informações no resumo.3/3: Atualizamos os gráficos para indicar o período de tempo da coluna de dosagem, agora mostrando a dosagem superior a um mês para profilaxia e superior a quatro dias para outros estudos.3/2: Atualizamos
[ IVERCOR PREP ] com os últimos resultados
[ Vallejos (B) ] .27/02: Adicionamos análises restritas a estudos revisados por pares.24/02: Adicionamos uma comparação da base de evidências e do status de aprovação da OMS para o uso de ivermectina com sarna e COVID-19. Atualizamos
[ Okumuş ] com a pré-impressão do Research Square.23/02: Adicionamos
[ Beltran Gonzalez ] .18/02: Atualizamos o
[ Babalola ] para a versão do jornal.17/02: Adicionamos
[ Elalfy ] e adicionamos análises restritas a resultados de eliminação viral e resultados de mortalidade restritos a ECRs.16/02: Atualizamos
[ Behera ] para a versão do jornal do jornal.15/02: Adicionamos
[ Behera (B) ] .14/02: Adicionamos análises restritas aos resultados de casos de COVID-19 e adicionamos resultados adicionais no resumo.12/02: Adicionamos
[ Biber ] .2/11: Adicionamos mais detalhes sobre a análise de estudos prospectivos versus retrospectivos.2/10: Adicionamos
[ Lima-Morales ] .2/5: Atualizamos
[ Bukhari ] para a pré-impressão.2/2: Adicionamos
[ Mohan ] .26/01: Atualizamos
[ Shouman ] com a versão do artigo no periódico.25/1: Atualizamos o
[ IVERCOR PREP ] com os resultados divulgados recentemente.19/01: Adicionamos
[ Shahbaznejad ] e Samaha et al.
[ Chaccour (B) ] foi atualizado para a versão de periódico do artigo.17/01: Adicionamos
[ Bukhari ] .16/01: Mudamos a análise com exclusões para o texto principal e adicionamos comentários adicionais.1/15: Adicionamos o efeito medido para cada estudo nas parcelas florestais.12/01: Adicionamos
[ Okumuş ] .1/11: Adicionamos
[ Chahla (B) ] .1/10: Colocamos todos os estudos de profilaxia em um único grupo.1/9: Adicionamos
[ Ravikirti (B) ] . Devido ao tamanho muito maior do grupo de controle em
[ Bernigaud ] , limitamos o tamanho do grupo de controle para ser o mesmo do grupo de tratamento para o cálculo do número total de pacientes.1/7: Adicionamos links diretos para os detalhes do estudo nas parcelas cronológicas.1/6: Adicionamos
[ Babalola ] .1/5: Adicionamos links diretos para os detalhes do estudo nas parcelas florestais.02/01/2021: Adicionamos informações de dosagem e adicionamos o número de pacientes às parcelas florestais.31/12: Adicionamos detalhes adicionais sobre os estudos no apêndice.29/12: Adicionamos meta-análise excluindo o tratamento tardio.27/12: Adicionamos o número total de autores e pacientes.26/12: Adicionamos
[ Carvallo (B) , IVERCOR PREP ] .17/12: Adicionamos
[ Alam ] .16/12: Adicionamos
[ Ghauri ] .11/12: Adicionamos
[ Soto-Becerra ] .12/7: Adicionamos
[ Chaccour (B) ] .2/12: Adicionamos
[ Ahmed ] .26/11/2020: Revisão inicial.
Apêndice 1. Métodos e DadosRealizamos pesquisas contínuas no PubMed, medRxiv, ClinicalTrials.gov, The Cochrane Library, Google Scholar, Collabovid, Research Square, ScienceDirect, Oxford University Press, as listas de referência de outros estudos e meta-análises e submissões ao site
c19ivermectin.com, que recebe regularmente submissões de estudos após a publicação. Os termos de pesquisa foram ivermectina e COVID-19 ou SARS-CoV-2, ou simplesmente ivermectina. As buscas automatizadas são realizadas a cada hora com notificação de novas correspondências. Os amplos termos de pesquisa resultam em um grande volume de novos estudos diariamente que são revisados para inclusão. Todos os estudos sobre o uso de ivermectina para COVID-19 que relatam uma comparação com um grupo controle estão incluídos na análise principal. A análise de sensibilidade é realizada, excluindo estudos com questões importantes, estudos epidemiológicos e estudos com informações mínimas disponíveis. Esta é uma análise viva e é atualizada regularmente.Extraímos tamanhos de efeito e dados associados de todos os estudos. Se os estudos relatam vários tipos de efeitos, o resultado mais sério é usado na análise agrupada, enquanto outros resultados são incluídos nas análises específicas do resultado. Por exemplo, se os efeitos para mortalidade e casos são relatados, o efeito para mortalidade é usado, isso pode ser diferente do efeito que um estudo focou. Se os resultados sintomáticos forem relatados várias vezes, usamos a última hora, por exemplo, se os resultados de mortalidade forem fornecidos em 14 dias e 28 dias, os resultados em 28 dias serão usados. A mortalidade por si só é preferível aos resultados combinados. Resultados com zero eventos em ambos os braços não foram usados (o próximo resultado mais grave é usado – nenhum estudo foi excluído). Por exemplo, em populações de baixo risco sem mortalidade, a redução da mortalidade com o tratamento não é possível, porém a redução da hospitalização, por exemplo, ainda é valiosa. O resultado clínico é considerado mais importante do que o status do teste de PCR. Quando basicamente todos os pacientes se recuperam em ambos os grupos de tratamento e controle, a preferência pela eliminação viral e recuperação é dada aos resultados na metade da recuperação, quando disponíveis (depois que a maioria ou todos os pacientes se recuperaram, não há espaço para um tratamento eficaz fazer melhor). Se apenas dados de sintomas individuais estiverem disponíveis, o sintoma mais grave tem prioridade, por exemplo, dificuldade para respirar ou SpO baixa a preferência pela eliminação e recuperação viral é dada aos resultados no meio da recuperação, quando disponíveis (depois que a maioria ou todos os pacientes se recuperaram, não há espaço para um tratamento eficaz fazer melhor). Se apenas dados de sintomas individuais estiverem disponíveis, o sintoma mais grave tem prioridade, por exemplo, dificuldade para respirar ou SpO baixa a preferência pela eliminação e recuperação viral é dada aos resultados no meio da recuperação, quando disponíveis (depois que a maioria ou todos os pacientes se recuperaram, não há espaço para um tratamento eficaz fazer melhor). Se apenas dados de sintomas individuais estiverem disponíveis, o sintoma mais grave tem prioridade, por exemplo, dificuldade para respirar ou SpO baixa
2 é mais importante que a tosse. Quando os resultados fornecem uma razão de chances, calculamos o risco relativo quando possível, ou convertemos para um risco relativo de acordo com
[ Zhang ] . Intervalos de confiança relatados e valores de
p foram usados quando disponíveis, usando valores ajustados quando fornecidos. Se vários tipos de ajustes forem relatados, incluindo correspondência de pontuação de propensão (PSM), os resultados do PSM serão usados. Os resultados do resultado primário ajustado têm preferência sobre os resultados não ajustados para um resultado mais sério quando os ajustes alteram significativamente os resultados. Quando necessário, seguiu-se a conversão entre os valores de
p relatados e os intervalos de confiança
[ Altman , Altman (B) ], e o teste exato de Fisher foi usado para calcular os valores de
p para dados de eventos. Se for necessária a correção de continuidade para valores zero, usamos o recíproco do braço oposto com a soma dos fatores de correção igual a 1
[ Sweeting ] . Os resultados são expressos com RR < 1,0 favorecendo o tratamento e usando o risco de desfecho negativo quando aplicável (por exemplo, o risco de morte em vez do risco de sobrevivência). Se os estudos relatarem apenas valores contínuos relativos, como tempos relativos, é usada a razão do tempo para o grupo de tratamento versus o tempo para o grupo de controle. Os cálculos são feitos em Python (3.9.13) com scipy (1.8.0), pythonmeta (1.26), numpy (1.22.2), statsmodels (0.14.0) e plotly (5.6.0).Os gráficos de floresta são calculados usando PythonMeta
[ Deng ] com o modelo de efeitos aleatórios DerSimonian e Laird (a suposição de efeito fixo não é plausível neste caso) e ponderação de variância inversa. Os resultados de meta-regressão de efeitos mistos são calculados com R (4.1.2) usando os pacotes metafor (3.0-2) e rms (6.2-0) e usando o resultado mais sério com potência suficiente. Os gráficos florestais mostram dosagens simplificadas para comparação, são a dose total nos primeiros quatro dias para tratamento e a dose mensal para profilaxia, para uma pessoa de 70kg. Para detalhes completos de dosagem, veja abaixo.Não recebemos nenhum financiamento, esta pesquisa é feita em nosso tempo livre. Não temos afiliações com empresas farmacêuticas ou partidos políticos.Classificamos os estudos como tratamento precoce se a maioria dos pacientes ainda não estiver em estágio grave no momento do tratamento (por exemplo, com base no status de oxigênio ou envolvimento pulmonar) e o tratamento for iniciado em até 5 dias após o início dos sintomas. Se os estudos contiverem uma combinação de pacientes com tratamento precoce e tratamento tardio, consideramos o tempo de tratamento dos pacientes que mais contribuíram para os eventos (por exemplo, considere um estudo em que a maioria dos pacientes é tratada precocemente, mas os pacientes com tratamento tardio são incluídos e todos os eventos de mortalidade foram observado com pacientes de tratamento tardio). Ressaltamos que um tempo menor pode ser preferível. Os antivirais geralmente são considerados eficazes apenas quando usados em um período de tempo mais curto, por exemplo, 0-36 ou 0-48 horas para oseltamivir, com atrasos mais longos não sendo eficazes
[ McLean ,Treano ] .Observe que o tamanho do grupo de controle em
[ Bernigaud ] é significativamente maior do que o grupo de tratamento. Anteriormente, limitamos o tamanho para ser o mesmo do grupo de tratamento para cálculo do número de pacientes, mas isso foi confuso para muitas pessoas que não leram os detalhes.Um resumo dos resultados do estudo está abaixo. Envie atualizações e correções na parte inferior desta página.
Tratamento precoce.A extração de efeitos segue regras pré-especificadas conforme detalhado acima e dá prioridade a resultados mais sérios. Apenas o primeiro resultado (mais grave) é usado na análise agrupada, que pode diferir do efeito no qual um artigo se concentra. Outros resultados são usados em análises específicas de resultados.
| [ Abbas ] , 31/12/2021, Ensaio controlado randomizado duplo cego, controlado por placebo, China, Ásia, revisado por pares, 3 autores, dosagem 300μg/kg dias 1-5, excluído em análises de exclusão: informações mínimas do paciente, três resultados diferentes para o resultado de recuperação, omissão seletiva do valor p de recuperação estatisticamente significativo e outras inconsistências.Envie correções ou atualizações . | risco de morte, 4,0% maior , RR 1,04, p = 1,00 , tratamento 1 de 99 (1,0%), controle 1 de 103 (1,0%). |
| deterioração de 2 ou mais pontos, 40,5% menor , RR 0,59, p = 0,54, tratamento 4 de 99 (4,0%), controle 7 de 103 (6,8%), NNT 36. | |
| escalada de cuidados, 14,9% menor , RR 0,85, p = 0,82, tratamento 9 de 99 (9,1%), controle 11 de 103 (10,7%), NNT 63. | |
| febre durante o estudo, 17,9% menor , RR 0,82, p = 0,58, tratamento 15 de 99 (15,2%), controle 19 de 103 (18,4%), NNT 30. | |
| risco de não recuperação, 35,6% menor , RR 0,64, p = 0,04, tratamento 26 de 99 (26,3%), controle 42 de 103 (40,8%), NNT 6,9, desfecho primário. | |
| tempo de recuperação, 30,8% menor , tempo relativo 0,69, p = 0,08, tratamento 99, controle 103, desfecho primário. | |
| [ Ahmed ] , 2/12/2020, Ensaio controlado randomizado duplo cego, Bangladesh, Sul da Ásia, revisado por pares, idade média 42,0, 15 autores, atraso médio no tratamento 3,83 dias, dosagem 12mg dias 1-5, o grupo ivermectina + doxiciclina tomou apenas uma dose única de ivermectina.Envie correções ou atualizações . | risco de sintomas não resolvidos, 85,0% menor , RR 0,15, p = 0,09 , tratamento 0 de 17 (0,0%), controle 3 de 19 (15,8%), NNT 6,3, risco relativo não é 0 devido à correção de continuidade devido a zero eventos (com recíproca do braço contrastante), dia 7, febre, ivermectina (5 dias), desfecho primário. |
| risco de sintomas não resolvidos, 62,7% menor , RR 0,37, p = 0,35, tratamento 1 de 17 (5,9%), controle 3 de 19 (15,8%), NNT 10, dia 7, febre, ivermectina (1 dia) + doxiciclina. | |
| risco de ausência de depuração viral, 75,6% menor , HR 0,24, p = 0,03, tratamento 11 de 22 (50,0%), controle 20 de 23 (87,0%), NNT 2,7, ajustado por estudo, dia 7, ivermectina (5 dias) . | |
| risco de ausência de depuração viral, 56,5% menor , HR 0,43, p = 0,22, tratamento 16 de 23 (69,6%), controle 20 de 23 (87,0%), NNT 5,8, ajustado por estudo, dia 7, ivermectina (1 dia) + doxiciclina. | |
| risco de ausência de depuração viral, 63,0% menor , HR 0,37, p = 0,02, tratamento 5 de 22 (22,7%), controle 14 de 23 (60,9%), NNT 2,6, ajustado por estudo, dia 14, ivermectina (5 dias) . | |
| risco de ausência de depuração viral, 41,2% menor , HR 0,59, p = 0,19, tratamento 9 de 23 (39,1%), controle 14 de 23 (60,9%), NNT 4,6, ajustado por estudo, dia 14, ivermectina (1 dia) + doxiciclina. | |
| tempo para viral-, 23,6% menor , tempo relativo 0,76, p = 0,02, tratamento 22, controle 23, ivermectina (5 dias). | |
| tempo para viral-, 9,4% menor , tempo relativo 0,91, p = 0,27, tratamento 23, controle 23, ivermectina (1 dia) + doxiciclina. | |
| [ Aref ] , 15/06/2021, Ensaio Controlado Randomizado, Egito, África, revisado por pares, 7 autores, dosagem não especificada, ensaio NCT04716569 .Envie correções ou atualizações . | duração relativa da febre, 63,2% menor , tempo relativo 0,37, p < 0,001 , tratamento 57, controle 57, desfecho primário. |
| duração relativa da dispneia, 56,4% menor , tempo relativo 0,44, p < 0,001, tratamento 57, controle 57. | |
| duração relativa da anosmia, 68,8% menor , tempo relativo 0,31, p < 0,001, tratamento 57, controle 57. | |
| duração relativa da tosse, 64,3% menor , tempo relativo 0,36, p < 0,001, tratamento 57, controle 57. | |
| risco de ausência de depuração viral, 78,6% menor , RR 0,21, p = 0,004, tratamento 3 de 57 (5,3%), controle 14 de 57 (24,6%), NNT 5,2. | |
| tempo para viral-, 35,7% menor , tempo relativo 0,64, p < 0,001, tratamento 57, controle 57. | |
| [ Babalola ] , 06/01/2021, Ensaio controlado randomizado duplo cego, Nigéria, África, revisado por pares, oxigênio basal necessário 8,3%, 10 autores, dosagem de 12mg ou 6mg a cada 84h por duas semanas, este estudo compara com outro tratamento – resultados pode ser melhor quando comparado ao placebo.Envie correções ou atualizações . | risco ajustado de viral+ no dia 5, 63,9% menor , RR 0,36, p = 0,11 , tratamento 40, controle 20, ajustado por estudo. |
| ∆SpO 2 relativo (não ajustado), 41,5% melhor , RR 0,59, p = 0,07, tratamento 38, controle 18, figura 3. | |
| risco de ausência de depuração viral, 58,0% menor , HR 0,42, p = 0,01, tratamento 20, controle 20, 12mg – modelo de risco proporcional de Cox. | |
| risco de ausência de depuração viral, 40,5% menor , HR 0,60, p = 0,12, tratamento 20, controle 20, 6mg – modelo de risco proporcional de Cox. | |
| tempo para viral-, 49,2% menor , tempo relativo 0,51, p = 0,02, tratamento 20, controle 20, 12mg, desfecho primário. | |
| tempo para viral-, 34,4% menor , tempo relativo 0,66, p = 0,08, tratamento 20, controle 20, 6mg. | |
| [ Biber ] , 12/02/2021, Ensaio controlado randomizado duplo cego, Israel, Oriente Médio, pré-impressão, 10 autores, atraso médio no tratamento 4,0 dias, dosagem 12mg dias 1-3, 15mg para pacientes >= 70kg, ensaio NCT04429711 .Envie correções ou atualizações . | risco de internação, 70,2% menor , RR 0,30, p = 0,34 , tratamento 1 de 47 (2,1%), controle 3 de 42 (7,1%), NNT 20. |
| risco de ausência de depuração viral, 44,8% menor , RR 0,55, p = 0,04, tratamento 13 de 47 (27,7%), controle 21 de 42 (50,0%), NNT 4,5, ajustado por estudo, odds ratio convertido em risco relativo, multivariável regressão logística, dia 6, Ct>30, desfecho primário. | |
| risco de ausência de depuração viral, 70,2% menor , RR 0,30, p = 0,14, tratamento 2 de 47 (4,3%), controle 6 de 42 (14,3%), NNT 10,0, dia 10, amostras não infecciosas (Ct>30 ou cultura inviável). | |
| risco de ausência de depuração viral, 82,1% menor , RR 0,18, p = 0,01, tratamento 2 de 47 (4,3%), controle 10 de 42 (23,8%), NNT 5,1, dia 8, amostras não infecciosas (Ct>30 ou cultura inviável). | |
| risco de ausência de depuração viral, 75,6% menor , RR 0,24, p = 0,02, tratamento 3 de 47 (6,4%), controle 11 de 42 (26,2%), NNT 5,0, dia 6, amostras não infecciosas (Ct>30 ou cultura inviável). | |
| risco de ausência de depuração viral, 65,1% menor , RR 0,35, p = 0,05, tratamento 4 de 28 (14,3%), controle 9 de 22 (40,9%), NNT 3,8, dia 4, amostras não infecciosas (Ct>30 ou cultura inviável). | |
| risco de ausência de depuração viral, 51,9% menor , RR 0,48, p = 0,08, tratamento 7 de 47 (14,9%), controle 13 de 42 (31,0%), NNT 6,2, dia 10, Ct>30. | |
| risco de ausência de depuração viral, 57,9% menor , RR 0,42, p = 0,02, tratamento 8 de 47 (17,0%), controle 17 de 42 (40,5%), NNT 4,3, dia 8, Ct>30. | |
| risco de ausência de depuração viral, 44,7% menor , RR 0,55, p = 0,049, tratamento 13 de 47 (27,7%), controle 21 de 42 (50,0%), NNT 4,5, dia 6, Ct>30. | |
| risco de ausência de depuração viral, 31,9% menor , RR 0,68, p = 0,16, tratamento 13 de 28 (46,4%), controle 15 de 22 (68,2%), NNT 4,6, dia 4, Ct>30. | |
| [ Borody ] , 19/10/2021, retrospectivo, Austrália, Oceania, pré-impressão, 2 autores, período de estudo 1 de junho de 2021 – 30 de setembro de 2021, dosagem 24mg dias 1-10, este estudo usa vários tratamentos no braço de tratamento ( combinado com zinco e doxiciclina) – os resultados dos tratamentos individuais podem variar, excluídos nas análises de exclusão: relatório preliminar com detalhes mínimos.Envie correções ou atualizações . | risco de morte, 92,3% menor , RR 0,08, p = 0,03 , tratamento 0 de 600 (0,0%), controle 6 de 600 (1,0%), NNT 100, risco relativo não é 0 por causa da correção de continuidade devido a zero eventos ( com o recíproco do braço contrastante). |
| risco de hospitalização, 92,9% menor , RR 0,07, p < 0,001, tratamento 5 de 600 (0,8%), controle 70 de 600 (11,7%), NNT 9,2, desfecho primário. | |
| [ Bukhari ] , 16/01/2021, Ensaio Controlado Randomizado, Paquistão, Sul da Ásia, pré-impressão, 10 autores, dose única de 12mg, ensaio NCT04392713 .Envie correções ou atualizações . | risco de ausência de depuração viral, 82,4% menor , RR 0,18, p < 0,001 , tratamento 4 de 41 (9,8%), controle 25 de 45 (55,6%), NNT 2,2, dia 7, desfecho primário. |
| risco de ausência de depuração viral, 38,7% menor , RR 0,61, p < 0,001, tratamento 24 de 41 (58,5%), controle 43 de 45 (95,6%), NNT 2,7, dia 3. | |
| [ Buonfrate ] , 06/09/2021, Ensaio controlado randomizado duplo cego, Itália, Europa, revisado por pares, 18 autores, atraso médio no tratamento 4,0 dias, dosagem 1200μg/kg dias 1-5, braço B 600µg/kg, braço C 1200µg/kg, ensaio NCT04438850 , excluído nas análises de exclusão: diferenças significativas não ajustadas entre os grupos, com 3 vezes mais pacientes nos braços de ivermectina tendo a consulta inicial em um ambiente hospitalar, e o braço C com grandes diferenças na linha de base de gênero, peso, tosse, pirexia e anosmia, dose excessiva para o braço C.Envie correções ou atualizações . | risco de internação, 210,7% maior , RR 3,11, p = 0,47 , tratamento 1 de 28 (3,6%), controle 0 de 31 (0,0%), correção de continuidade por evento zero (com recíproca do braço contrastante), braço B . |
| risco de internação, 610,0% maior , RR 7,10, p = 0,11, tratamento 3 de 30 (10,0%), controle 0 de 31 (0,0%), correção de continuidade por evento zero (com recíproca do braço contrastante), braço C , dose muito alta, mal tolerada com baixa adesão. | |
| mudança relativa na carga viral, RR 0,80, p = 0,59, média de tratamento 2,5 (±2,2) n=28, média de controle 2,0 (±4,4) n=29, dia 7, braço B, resultado primário. | |
| mudança relativa na carga viral, RR 0,69, p = 0,07, média de tratamento 2,9 (±1,6) n=30, média de controle 2,0 (±2,1) n=29, dia 7, braço C, resultado primário. | |
| [ Cadegiani ] , 4/11/2020, prospectivo, Brasil, América do Sul, revisado por pares, 4 autores, atraso médio no tratamento 2,9 dias, dosagem 200μg/kg dias 1-3, este estudo usa vários tratamentos no braço de tratamento (combinação com AZ, nitazoxanida (82), HCQ (22), espironolactona (66), dutasterida (4)) – os resultados dos tratamentos individuais podem variar, excluídos nas análises de exclusão: grupo controle obtido retrospectivamente de pacientes não tratados na mesma população.Envie correções ou atualizações . | risco de morte, 78,3% menor , RR 0,22, p = 0,50 , tratamento 0 de 110 (0,0%), controle 2 de 137 (1,5%), NNT 68, risco relativo não é 0 por causa da correção de continuidade devido a zero eventos ( com recíproca do braço contrastante), grupo controle 1. |
| risco de ventilação mecânica, 94,2% menor , RR 0,06, p = 0,005, tratamento 0 de 110 (0,0%), controle 9 de 137 (6,6%), NNT 15, risco relativo não é 0 devido à correção de continuidade devido a zero eventos (com recíproca do braço contrastante), grupo controle 1. | |
| risco de hospitalização, 98,0% menor , RR 0,02, p < 0,001, tratamento 0 de 110 (0,0%), controle 27 de 137 (19,7%), NNT 5,1, risco relativo não é 0 devido à correção de continuidade devido a zero eventos ( com recíproca do braço contrastante), grupo controle 1. | |
| [ Carvallo (C) ] , 15/09/2020, prospectivo, Argentina, América do Sul, revisado por pares, idade média 55,7, 3 autores, dosagem 36mg dias 1, 8, dose variada dependendo da condição do paciente – leve 24mg, moderado 36mg , grave 48mg, este estudo usa vários tratamentos no braço de tratamento (combinado com dexametasona, enoxaparina e aspirina) – os resultados dos tratamentos individuais podem variar, excluídos nas análises de exclusão: detalhes mínimos dos grupos fornecidos.Envie correções ou atualizações . | risco de morte, 85,4% menor , RR 0,15, p = 0,08 , tratamento 1 de 32 (3,1%), controle 3 de 14 (21,4%), NNT 5,5, pacientes moderados/graves, o único tratamento morte foi um paciente já em a UTI antes do tratamento, desfecho primário. |
| [ Chaccour (B) ] , 7/12/2020, Ensaio controlado randomizado duplo-cego, Espanha, Europa, revisado por pares, 23 autores, atraso médio no tratamento de 1,0 dias, dosagem 400μg/kg dose única, ensaio NCT04390022 .Envie correções ou atualizações . | risco de sintomas, 96,0% menor , OR 0,04, p < 0,05 , tratamento 12, controle 12, regressão logística, chance de apresentar algum sintoma, RR aproximado de OR. |
| carga viral, 94,6% menor , carga relativa 0,05, p < 0,01, tratamento 12, controle 12, dia 7 de recuperação média, média do gene E e do gene N, dados em anexo suplementar. | |
| risco de ausência de depuração viral, 8,0% menor , RR 0,92, p = 1,00, tratamento 12, controle 12, desfecho primário. | |
| [ Chahla ] , 30/03/2021, Ensaio controlado randomizado em cluster, Argentina, América do Sul, pré-impressão, 9 autores, dosagem 24mg dias 1, 8, 15, 22, ensaio NCT04784481 .Envie correções ou atualizações . | risco de não alta, 86,9% menor , RR 0,13, p = 0,004 , tratamento 2 de 110 (1,8%), controle 20 de 144 (13,9%), NNT 8,3, ajustado por estudo, odds ratio convertido em risco relativo, regressão logística , resultado primário. |
| [ Chowdhury ] , 14/07/2020, Ensaio Controlado Randomizado, Bangladesh, Sul da Ásia, revisado por pares, 6 autores, dosagem 200μg/kg dose única, este ensaio compara com outro tratamento – os resultados podem ser melhores quando comparados ao placebo, este ensaio usa vários tratamentos no braço de tratamento (combinado com doxiciclina) – os resultados de tratamentos individuais podem variar, ensaio NCT04434144 .Envie correções ou atualizações . | risco de hospitalização, 80,6% menor , RR 0,19, p = 0,23 , tratamento 0 de 60 (0,0%), controle 2 de 56 (3,6%), NNT 28, risco relativo não é 0 por causa da correção de continuidade devido a zero eventos ( com o recíproco do braço contrastante). |
| risco de não recuperação, 46,4% menor , RR 0,54, p < 0,001, tratamento 27 de 60 (45,0%), controle 47 de 56 (83,9%), NNT 2,6, meio de recuperação dia 5. | |
| tempo de recuperação, 15,2% menor , tempo relativo 0,85, p = 0,07, tratamento 60, controle 56. | |
| risco de ausência de depuração viral, 80,6% menor , RR 0,19, p = 0,23, tratamento 0 de 60 (0,0%), controle 2 de 56 (3,6%), NNT 28, risco relativo não é 0 devido à correção de continuidade devido a zero eventos (com recíproca do braço contrastante), desfecho primário. | |
| tempo para viral, 4,3% menor , tempo relativo 0,96, p = 0,23, tratamento 60, controle 56. | |
| [ de Jesús Ascencio-Montiel ] , 24/01/2022, retrospectivo, México, América do Norte, revisado por pares, 10 autores, dosagem 6mg dias 1-2, este estudo usa vários tratamentos no braço de tratamento (combinado com AZ, acetaminofeno , aspirina) – os resultados dos tratamentos individuais podem variar.Envie correções ou atualizações . | risco de morte/hospitalização, 59,0% menor , RR 0,41, p < 0,001 , tratamento 7.898, controle 20.150, ajustado por estudo, multivariável, desfecho primário. |
| risco de morte/hospitalização, 71,0% menor , RR 0,29, p < 0,001, tratamento 5.557, controle 12.526, ajustado por estudo, com acompanhamento por telefone, multivariável. | |
| risco de morte, 15,0% menor , RR 0,85, p = 0,16, tratamento 101 de 7.898 (1,3%), controle 303 de 20.150 (1,5%), NNT 445, não ajustado, excluído em análises de exclusão: resultados não ajustados com resultados ajustados de desfecho alternativo mostrando mudanças significativas com ajustes. | |
| risco de ventilação mecânica, 9,1% menor , RR 0,91, p = 0,51, tratamento 77 de 7.898 (1,0%), controle 216 de 20.150 (1,1%), NNT 1031, não ajustado, excluído em análises de exclusão: resultados não ajustados com resultado alternativo ajustado resultados mostrando mudanças significativas com ajustes. | |
| risco de hospitalização, 47,6% menor , RR 0,52, p < 0,001, tratamento 485 de 7.898 (6,1%), controle 2.360 de 20.150 (11,7%), NNT 18, não ajustado, excluído nas análises de exclusão: resultados não ajustados com resultados ajustados de resultado alternativo mostrando mudanças significativas com ajustes. | |
| risco de progressão, 41,8% menor , RR 0,58, p < 0,001, tratamento 435 de 7.898 (5,5%), controle 1.906 de 20.150 (9,5%), NNT 25, não ajustado, ER, excluído nas análises de exclusão: resultados não ajustados com resultado alternativo resultados ajustados mostrando mudanças significativas com os ajustes. | |
| [ Elalfy ] , 16/02/2021, retrospectivo, Egito, África, revisado por pares, 15 autores, dosagem 18mg dias 1, 4, 7, 10, 13, <90kg 18mg, 90-120kg 24mg, >120kg 30mg, este ensaio usa vários tratamentos no braço de tratamento (combinado com nitazoxanida, ribavirina e zinco) – os resultados dos tratamentos individuais podem variar.Envie correções ou atualizações . | risco de ausência de depuração viral, 86,9% menor , RR 0,13, p < 0,001 , tratamento 7 de 62 (11,3%), controle 44 de 51 (86,3%), NNT 1,3, dia 15, desfecho primário. |
| risco de ausência de depuração viral, 58,1% menor , RR 0,42, p < 0,001, tratamento 26 de 62 (41,9%), controle 51 de 51 (100,0%), NNT 1,7, dia 7. | |
| [ Espitia-Hernandez ] , 15/08/2020, retrospectivo, México, América do Norte, revisado por pares, idade média 45,1, 5 autores, dosagem 6mg dias 1-2, 8-9, este estudo usa vários tratamentos no braço de tratamento (combinado com azitromicina e colecalciferol) – os resultados dos tratamentos individuais podem variar.Envie correções ou atualizações . | tempo de recuperação, 70,0% menor , tempo relativo 0,30, p < 0,001 , tratamento 28, controle 7. |
| risco de viral+ no dia 10, 97,2% menor , RR 0,03, p < 0,001, tratamento 0 de 28 (0,0%), controle 7 de 7 (100,0%), NNT 1,0, risco relativo não é 0 devido à correção de continuidade devido a zero eventos (com recíproca do braço contrastante), desfecho primário. | |
| [ Faisal ] , 10/05/2021, Ensaio Controlado Randomizado, Paquistão, Sul da Ásia, revisado por pares, 3 autores, dosagem 12mg dias 1-5.Envie correções ou atualizações . | risco de não recuperação, 68,4% menor , RR 0,32, p = 0,005 , tratamento 6 de 50 (12,0%), controle 19 de 50 (38,0%), NNT 3,8, 6-8 dias, recuperação intermediária, desfecho primário. |
| risco de não recuperação, 27,3% menor , RR 0,73, p = 0,11, tratamento 24 de 50 (48,0%), controle 33 de 50 (66,0%), NNT 5,6, 3-5 dias. | |
| risco de não recuperação, 75,0% menor , RR 0,25, p = 0,09, tratamento 2 de 50 (4,0%), controle 8 de 50 (16,0%), NNT 8,3, 9-10 dias. | |
| [ Ghauri ] , 15/12/2020, retrospectivo, Paquistão, Sul da Ásia, revisado por pares, 6 autores, dosagem 12mg dias 1-6.Envie correções ou atualizações . | risco de febre, 92,2% menor , RR 0,08, p = 0,04 , tratamento 0 de 37 (0,0%), controle 7 de 53 (13,2%), NNT 7,6, risco relativo não é 0 devido à correção de continuidade devido a zero eventos ( com recíproca do braço contrastante), dia 14. |
| risco de febre, 86,4% menor , RR 0,14, p < 0,001, tratamento 2 de 37 (5,4%), controle 21 de 53 (39,6%), NNT 2,9, dia 10. | |
| risco de febre, 55,7% menor , RR 0,44, p < 0,001, tratamento 13 de 37 (35,1%), controle 42 de 53 (79,2%), NNT 2,3, dia 7. | |
| risco de febre, 42,2% menor , RR 0,58, p < 0,001, tratamento 21 de 37 (56,8%), controle 52 de 53 (98,1%), NNT 2,4, dia 5. | |
| [ Krolewiecki ] , 18/06/2021, Ensaio Controlado Randomizado, Argentina, América do Sul, revisado por pares, 23 autores, atraso médio no tratamento de 3,5 dias, dosagem 600μg/kg dias 1-5, ensaio NCT004381884 .Envie correções ou atualizações . | risco de ventilação mecânica, 151,9% maior , RR 2,52, p = 1,00 , tratamento 1 de 27 (3,7%), controle 0 de 14 (0,0%), correção de continuidade por evento zero (com recíproca do braço contrastante). |
| risco de progressão, 3,7% maior , RR 1,04, p = 1,00, tratamento 2 de 27 (7,4%), controle 1 de 14 (7,1%). | |
| taxa de decaimento viral, 65,6% menor , RR 0,34, p = 0,09, tratamento 20, controle 14, taxa média relativa de decaimento viral (tabela 2 de correção), desfecho primário. | |
| [ Loue ] , 17/04/2021, retrospectivo quase randomizado (escolha do paciente), França, Europa, revisado por pares, 2 autores, dosagem 200μg/kg dose única.Envie correções ou atualizações . | risco de morte, 70,0% menor , RR 0,30, p = 0,34 , tratamento 1 de 10 (10,0%), controle 5 de 15 (33,3%), NNT 4,3. |
| risco de caso grave, 55,0% menor , RR 0,45, p = 0,11, tratamento 3 de 10 (30,0%), controle 10 de 15 (66,7%), NNT 2,7. | |
| [ López-Medina ] , 4/3/2021, Ensaio controlado randomizado duplo cego, Colômbia, América do Sul, revisado por pares, idade mediana 37,0, 19 autores, atraso médio no tratamento 5,0 dias, dosagem 300μg/kg dias 1-5, excluídos nas análises de exclusão: forte evidência de pacientes do grupo controle se automedicando, ivermectina amplamente utilizada na população na época, e a identidade do medicamento do estudo foi ocultada pelo nome D11AX22.Envie correções ou atualizações . | risco de morte, 66,8% menor , RR 0,33, p = 0,50 , tratamento 0 de 200 (0,0%), controle 1 de 198 (0,5%), NNT 198, risco relativo não é 0 devido à correção de continuidade devido a zero eventos ( com o recíproco do braço contrastante). |
| risco de escalada de cuidados, 60,8% menor , RR 0,39, p = 0,11, tratamento 4 de 200 (2,0%), controle 10 de 198 (5,1%), NNT 33, odds ratio convertido em risco relativo. | |
| risco de escalonamento de cuidados com exclusão post-hoc <12h, 34,3% menor , RR 0,66, p = 0,52, tratamento 4 de 200 (2,0%), controle 6 de 198 (3,0%), NNT 97, odds ratio convertido para relativo risco. | |
| risco de deterioração >= 2 pontos em uma escala de 8 pontos, 43,1% menor , RR 0,57, p = 0,37, tratamento 4 de 200 (2,0%), controle 7 de 198 (3,5%), NNT 65, odds ratio convertido ao risco relativo, desfecho primário. | |
| risco de febre após a randomização, 24,8% menor , RR 0,75, p = 0,38, tratamento 16 de 200 (8,0%), controle 21 de 198 (10,6%), NNT 38, odds ratio convertido em risco relativo. | |
| risco de sintomas não resolvidos no dia 21, 15,3% menor , RR 0,85, p = 0,53, tratamento 36 de 200 (18,0%), controle 42 de 198 (21,2%), NNT 31, odds ratio convertido em risco relativo, Cox proporcional- modelo de perigo. | |
| ausência de resolução dos sintomas, 6,5% menor , HR 0,93, p = 0,53, tratamento 200, controle 198, resultado primário post-hoc. | |
| [ Mahmud ] , 9/10/2020, Ensaio controlado randomizado duplo cego, Bangladesh, Sul da Ásia, revisado por pares, 15 autores, atraso médio no tratamento de 4,0 dias, dosagem de 12mg em dose única, este estudo usa vários tratamentos no braço de tratamento (combinação com doxiciclina) – os resultados dos tratamentos individuais podem variar, ensaio NCT04523831 .Envie correções ou atualizações . | risco de morte, 85,7% menor , HR 0,14, p = 0,25 , tratamento 0 de 183 (0,0%), controle 3 de 183 (1,6%), NNT 61, risco relativo não é 0 devido à correção de continuidade devido a zero eventos ( com o recíproco do braço contrastante). |
| risco de progressão, 57,0% menor , HR 0,43, p < 0,001, tratamento 16 de 183 (8,7%), controle 32 de 180 (17,8%), NNT 11, ajustado por estudo, regressão de Cox. | |
| risco de não recuperação, 94,0% menor , HR 0,06, p < 0,001, tratamento 72 de 183 (39,3%), controle 100 de 180 (55,6%), NNT 6,2, ajustado por estudo, dia 7, regressão de Cox. | |
| risco de não recuperação, 38,5% menor , RR 0,61, p = 0,005, tratamento 40 de 183 (21,9%), controle 64 de 180 (35,6%), NNT 7,3, dia 11. | |
| risco de não recuperação, 96,0% menor , HR 0,04, p < 0,001, tratamento 42 de 183 (23,0%), controle 67 de 180 (37,2%), NNT 7,0, ajustado por estudo, dia 12, regressão de Cox. | |
| tempo de recuperação, 27,0% menor , HR 0,73, p = 0,003, tratamento 183, controle 180, regressão de Cox, desfecho primário. | |
| risco de ausência de depuração viral, 39,0% menor , HR 0,61, p = 0,002, tratamento 14 de 183 (7,7%), controle 36 de 180 (20,0%), NNT 8,1, ajustado por estudo, regressão de Cox. | |
| [ Manomaipiboon ] , 2/2/2022, Ensaio controlado randomizado duplo-cego, controlado por placebo, Tailândia, Sul da Ásia, pré-impressão, 8 autores, dosagem 12mg dias 1-5.Envie correções ou atualizações . | risco de não recuperação, 43,5% menor , RR 0,57, p = 0,26 , tratamento 3 de 36 (8,3%), controle 6 de 36 (16,7%), NNT 12, ajustado por estudo, odds ratio convertido em risco relativo, resolução de sintomas, dia 28. |
| tempo de recuperação, 15,3% menor , RR 0,85, p = 0,57, tratamento 36, controle 36, tempo de resolução dos sintomas. | |
| risco de ausência de depuração viral, 5,0% menor , RR 0,95, p = 1,00, tratamento 19 de 36 (52,8%), controle 20 de 36 (55,6%), NNT 36, dia 14, desfecho primário. | |
| risco de ausência de depuração viral, 3,3% menor , RR 0,97, p = 1,00, tratamento 29 de 36 (80,6%), controle 30 de 36 (83,3%), NNT 36, dia 7. | |
| [ Mayer ] , 23/09/2021, retrospectivo, Argentina, América do Sul, revisado por pares, 14 autores, dosagem 540μg/kg dias 1-5, dose média prescrita.Envie correções ou atualizações . | risco de morte, 55,1% menor , RR 0,45, p < 0,001 , tratamento 3.266, controle 17.966, ajustado por estudo, odds ratio convertido em risco relativo, Figura 3, multivariável. |
| risco de internação na UTI, 65,9% menor , RR 0,34, p < 0,001, tratamento 3.266, controle 17.966, ajustado por estudo, odds ratio convertido em risco relativo, Figura 3, multivariável. | |
| risco de morte, 27,6% menor , RR 0,72, p = 0,03, tratamento 3.266, controle 17.966, odds ratio convertido em risco relativo, não ajustado. | |
| risco de internação na UTI, 26,0% menor , RR 0,74, p = 0,13, tratamento 3.266, controle 17.966, odds ratio convertido em risco relativo, não ajustado. | |
| [ Merino ] , 03/05/2021, quase randomizado retrospectivo (pacientes recebendo kit), coorte de base populacional, México, América do Norte, pré-impressão, 7 autores, dosagem 6mg bid dias 1-2.Envie correções ou atualizações . | risco de internação, 74,4% menor , RR 0,26, p < 0,001 , modelo 7, mesmo período, pacientes que receberam kit. |
| risco de internação, 68,4% menor , RR 0,32, p < 0,001, modelo 1, diferentes períodos de tempo, portaria. | |
| [ Mohan ] , 2/2/2021, Ensaio controlado randomizado duplo cego, Índia, Sul da Ásia, revisado por pares, 27 autores, atraso médio no tratamento de 5,0 dias, dosagem de 400μg/kg em dose única, 200μg/kg também testado.Envie correções ou atualizações . | risco de não alta no dia 14, 62,5% menor , RR 0,38, p = 0,27 , tratamento 2 de 40 (5,0%), controle 6 de 45 (13,3%), NNT 12, ivermectina 24mg. |
| risco de piora clínica, 32,5% menor , RR 0,68, p = 0,72, tratamento 3 de 40 (7,5%), controle 5 de 45 (11,1%), NNT 28, ivermectina 24mg. | |
| risco de ausência de depuração viral, 23,8% menor , RR 0,76, p = 0,18, tratamento 21 de 40 (52,5%), controle 31 de 45 (68,9%), NNT 6,1, ivermectina 24mg, dia 5, desfecho primário. | |
| risco de ausência de depuração viral, 10,3% menor , RR 0,90, p = 0,65, tratamento 20 de 36 (55,6%), controle 26 de 42 (61,9%), NNT 16, ivermectina 24mg, dia 7. | |
| [ Mourya ] , 01/04/2021, retrospectivo, Índia, Sul da Ásia, revisado por pares, 5 autores, dosagem 12mg dias 1-7.Envie correções ou atualizações . | risco de ausência de depuração viral, 89,4% menor , RR 0,11, p < 0,001 , tratamento 5 de 50 (10,0%), controle 47 de 50 (94,0%), NNT 1,2, desfecho primário. |
| [ Ravikirti (B) ] , 09/01/2021, Ensaio controlado randomizado duplo-cego, Índia, Sul da Ásia, revisado por pares, 11 autores, atraso médio no tratamento 6,1 dias, dosagem 12mg dias 1, 2.Envie correções ou atualizações . | risco de morte, 88,7% menor , RR 0,11, p = 0,12 , tratamento 0 de 55 (0,0%), controle 4 de 57 (7,0%), NNT 14, risco relativo não é 0 devido à correção de continuidade devido a zero eventos ( com o recíproco do braço contrastante). |
| risco de ventilação mecânica, 79,3% menor , RR 0,21, p = 0,10, tratamento 1 de 55 (1,8%), controle 5 de 57 (8,8%), NNT 14. | |
| risco de internação na UTI, 13,6% menor , RR 0,86, p = 0,80, tratamento 5 de 55 (9,1%), controle 6 de 57 (10,5%), NNT 70. | |
| risco de não alta hospitalar, 88,7% menor , RR 0,11, p = 0,12, tratamento 0 de 55 (0,0%), controle 4 de 57 (7,0%), NNT 14, risco relativo não é 0 por causa da correção de continuidade devido a zero eventos (com recíproca do braço contrastante). | |
| risco de ausência de depuração viral, 11,6% maior , RR 1,12, p = 0,35, tratamento 42 de 55 (76,4%), controle 39 de 57 (68,4%). | |
| [ Reis ] , 06/08/2021, Ensaio controlado randomizado duplo cego, Brasil, América do Sul, revisado por pares, 27 autores, período de estudo 23 de março de 2021 – 6 de agosto de 2021, dosagem 400μg/kg dias 1-3, ensaio NCT04727424 (JUNTOS), excluídos nas análises de exclusão: anomalias múltiplas conforme análise detalhada.Envie correções ou atualizações . | risco de morte, 12,0% menor , RR 0,88, p = 0,68 , tratamento 21 de 679 (3,1%), controle 24 de 679 (3,5%), NNT 226. |
| risco de ventilação mecânica, 23,0% menor , RR 0,77, p = 0,38, tratamento 19 de 679 (2,8%), controle 25 de 679 (3,7%), NNT 113. | |
| risco de internação, 17,0% menor , RR 0,83, p = 0,19, tratamento 79 de 679 (11,6%), controle 95 de 679 (14,0%), NNT 42. | |
| observação de emergência estendida ou hospitalização, 10,0% menor , RR 0,90, p = 0,42, tratamento 100 de 679 (14,7%), controle 111 de 679 (16,3%), NNT 62, desfecho primário. | |
| risco de ausência de depuração viral, sem alteração , RR 1,00, p = 1,00, tratamento 106 de 142 (74,6%), controle 123 de 165 (74,5%), dia 7. | |
| [ Rocha ] , 23/05/2022, Ensaio controlado randomizado duplo cego, controlado por placebo, México, América do Norte, pré-impressão, 21 autores, dosagem 12mg dias 1-3, ensaio NCT04407507 .Envie correções ou atualizações . | risco de progressão para eventos adversos graves, 186,7% maior , RR 2,87, p = 1,00 , tratamento 1 de 30 (3,3%), controle 0 de 26 (0,0%), correção de continuidade devido a evento zero (com recíproca do braço contrastante ). |
| carga viral, 2,4% menor , carga relativa 0,98, p = 0,64, média de tratamento 33,74 (±4,77) n=30, média de controle 32,94 (±7,74) n=26, dia 14. | |
| carga viral, 7,8% menor , carga relativa 0,92, p = 0,04, média de tratamento 30,64 (±3,74) n=30, média de controle 28,25 (±4,21) n=26, dia 5. | |
| [ Roy ] , 12/03/2021, retrospectiva, análise de banco de dados, Índia, Sul da Ásia, pré-impressão, 5 autores, dosagem não especificada, este estudo usa vários tratamentos no braço de tratamento (combinado com doxiciclina) – os resultados dos tratamentos individuais podem variar , excluídos nas análises de exclusão: nenhum desfecho grave relatado e recuperação rápida nos grupos de tratamento e controle, há pouco espaço para um tratamento melhorar os resultados.Envie correções ou atualizações . | tempo relativo para resposta clínica de bem-estar, 5,6% menor , tempo relativo 0,94, p = 0,87 , tratamento 14, controle 15, desfecho primário. |
| [ Szente Fonseca ] , 31/10/2020, retrospectivo, Brasil, América do Sul, revisado por pares, idade média 50,6, 10 autores, atraso médio no tratamento 4,6 dias, dosagem 12mg dias 1-2, excluídos nas análises de exclusão: o resultado é provável afetada pela colinearidade entre os tratamentos no modelo.Envie correções ou atualizações . | risco de hospitalização, 13,9% maior , RR 1,14, p = 0,53 , tratamento 340, controle 377, ajustado por estudo, odds ratio convertido em risco relativo, prevalência de controle aproximada com prevalência geral, desfecho primário. |
| [ Vallejos ] , 2/7/2021, Ensaio controlado randomizado duplo cego, Argentina, América do Sul, revisado por pares, 29 autores, atraso médio no tratamento 4,0 dias, dosagem 12mg dias 1-2, <80kg 12mg, 80-110kg 18mg, >110kg 24mg.Envie correções ou atualizações . | risco de morte, 33,5% maior , RR 1,33, p = 0,70 , tratamento 4 de 250 (1,6%), controle 3 de 251 (1,2%), razão de chances convertida em risco relativo. |
| risco de ventilação mecânica, 33,5% maior , RR 1,33, p = 0,70, tratamento 4 de 250 (1,6%), controle 3 de 251 (1,2%), odds ratio convertido em risco relativo. | |
| risco de hospitalização, 33,0% menor , RR 0,67, p = 0,23, tratamento 14 de 250 (5,6%), controle 21 de 251 (8,4%), NNT 36, odds ratio convertido em risco relativo, desfecho primário. | |
| risco de ausência de depuração viral, 5,0% maior , RR 1,05, p = 0,55, tratamento 137 de 250 (54,8%), controle 131 de 251 (52,2%), razão de chances convertida em risco relativo, dia 3. | |
| risco de ausência de depuração viral, 26,8% maior , RR 1,27, p = 0,29, tratamento 38 de 250 (15,2%), controle 30 de 251 (12,0%), razão de chances convertida em risco relativo, dia 12. |
Tratamento tardio.A extração de efeitos segue regras pré-especificadas conforme detalhado acima e dá prioridade a resultados mais sérios. Apenas o primeiro resultado (mais grave) é usado na análise agrupada, que pode diferir do efeito no qual um artigo se concentra. Outros resultados são usados em análises específicas de resultados.
| [ Abd-Elsalam ] , 02/06/2021, Ensaio Controlado Randomizado, Egito, África, revisado por pares, 16 autores, dosagem 12mg dias 1-3.Envie correções ou atualizações . | risco de morte, 25,0% menor , RR 0,75, p = 0,70 , tratamento 3 de 82 (3,7%), controle 4 de 82 (4,9%), NNT 82, odds ratio convertido em risco relativo, regressão logística, desfecho primário. |
| risco de ventilação mecânica, sem alteração , RR 1,00, p = 1,00, tratamento 3 de 82 (3,7%), controle 3 de 82 (3,7%). | |
| tempo de internação, 19,6% menor , tempo relativo 0,80, p = 0,09, tratamento 82, controle 82. | |
| [ Ahsan ] , 29/04/2021, retrospectivo, Paquistão, Sul da Ásia, revisado por pares, 10 autores, dosagem 150μg/kg dias 1-2, 150-200µg/kg, este estudo usa vários tratamentos no braço de tratamento (combinação com doxiciclina) – os resultados dos tratamentos individuais podem variar, excluídos nas análises de exclusão: resultados não ajustados sem detalhes do grupo.Envie correções ou atualizações . | risco de morte, 50,0% menor , RR 0,50, p = 0,03 , tratamento 17 de 110 (15,5%), controle 17 de 55 (30,9%), NNT 6,5. |
| [ Baguma ] , 28/12/2021, retrospectivo, Uganda, África, pré-impressão, 16 autores, período de estudo março 2020 – outubro 2021, dosagem não especificada.Envie correções ou atualizações . | risco de morte, 96,8% menor , RR 0,03, p = 0,31 , tratamento 7, controle 474, ajustado por estudo, odds ratio convertido em risco relativo, multivariável, prevalência de controle aproximada com prevalência global. |
| [ Beltran Gonzalez ] , 23/02/2021, Ensaio controlado randomizado duplo cego, México, América do Norte, revisado por pares, idade média 53,8, 13 autores, atraso médio no tratamento 7,0 dias, dosagem de 12mg em dose única, 18mg para pacientes >80kg, excluídos nas análises de exclusão: principais inconsistências relatadas e os dados não estão mais disponíveis, embora os autores afirmem que estão disponíveis e os compartilharam com um grupo antitratamento.Envie correções ou atualizações . | risco de morte, 14,4% menor , RR 0,86, p = 1,00 , tratamento 5 de 36 (13,9%), controle 6 de 37 (16,2%), NNT 43. |
| risco de deterioração respiratória ou morte, 8,6% menor , RR 0,91, p = 1,00, tratamento 8 de 36 (22,2%), controle 9 de 37 (24,3%), NNT 48. | |
| risco de não alta hospitalar, 37,0% maior , RR 1,37, p = 0,71, tratamento 4 de 36 (11,1%), controle 3 de 37 (8,1%). | |
| tempo de internação, 20,0% maior , tempo relativo 1,20, p = 0,43, tratamento 36, controle 37, desfecho primário. | |
| [ Budhiraja ] , 18/11/2020, retrospectiva, Índia, Sul da Ásia, pré-impressão, 12 autores, dosagem não especificada.Envie correções ou atualizações . | risco de morte, 99,1% menor , RR 0,009, p = 0,04 , tratamento 0 de 34 (0,0%), controle 103 de 942 (10,9%), NNT 9,1, risco relativo não é 0 devido à correção de continuidade devido a zero eventos ( com recíproca do braço contrastante), resultado primário não ajustado. |
| [ Camprubí ] , 11/11/2020, retrospectivo, Espanha, Europa, revisado por pares, 9 autores, atraso médio de tratamento 12,0 dias, dosagem 200μg/kg dose única.Envie correções ou atualizações . | risco de ventilação mecânica, 40,0% menor , RR 0,60, p = 0,67 , tratamento 3 de 13 (23,1%), controle 5 de 13 (38,5%), NNT 6,5. |
| risco de internação na UTI, 33,3% menor , RR 0,67, p = 1,00, tratamento 2 de 13 (15,4%), controle 3 de 13 (23,1%), NNT 13, UTI no dia 8. | |
| risco de nenhuma melhora no dia 8, 33,3% maior , RR 1,33, p = 1,00, tratamento 4 de 13 (30,8%), controle 3 de 13 (23,1%). | |
| risco de ausência de depuração viral, 25,0% maior , RR 1,25, p = 1,00, tratamento 5 de 13 (38,5%), controle 4 de 13 (30,8%), exames realizados entre os dias 3-5, desfecho primário. | |
| [ Chachar ] , 30/09/2020, Ensaio Controlado Randomizado, Índia, Sul da Ásia, revisado por pares, 6 autores, dosagem 36mg, 12mg stat, 12mg após 12 horas, 12mg após 24 horas.Envie correções ou atualizações . | risco de não recuperação no dia 7, 10,0% menor , RR 0,90, p = 0,50 , tratamento 9 de 25 (36,0%), controle 10 de 25 (40,0%), NNT 25, desfecho primário. |
| [ Efimenko ] , 28/02/2022, retrospectivo, correspondência de pontuação de propensão, EUA, América do Norte, revisado por pares, 6 autores, período de estudo 1 de janeiro de 2020 – 11 de julho de 2021, dosagem não especificada, este estudo compara com outro tratamento – os resultados podem ser melhores quando comparados ao placebo.Envie correções ou atualizações . | risco de morte, 69,2% menor , OR 0,31, p < 0,001 , tratamento 1.072, controle 40.536, correspondência de escore de propensão, RR aproximado com OR. |
| [ Elavarasi ] , 8/12/2021, retrospectivo, Índia, Sul da Ásia, pré-impressão, 26 autores, dosagem não especificada, excluídos em análises de exclusão: resultados não ajustados sem detalhes de grupo.Envie correções ou atualizações . | risco de morte, 19,6% menor , RR 0,80, p = 0,12 , tratamento 48 de 283 (17,0%), controle 311 de 1.475 (21,1%), NNT 24, não ajustado. |
| [ Ferreira ] , 26/11/2021, retrospectivo, Brasil, América do Sul, revisado por pares, 5 autores, período de estudo 12 de março de 2020 – 8 de julho de 2020, atraso médio no tratamento de 7,0 dias, dosagem não especificada, excluída nas análises de exclusão : resultados não ajustados sem detalhes de grupo, confusão substancial não ajustada por indicação provável.Envie correções ou atualizações . | risco de morte, 5,0% maior , RR 1,05, p = 1,00 , tratamento 3 de 21 (14,3%), controle 11 de 81 (13,6%). |
| risco de morte/intubação, 54,3% maior , RR 1,54, p = 0,37, tratamento 6 de 21 (28,6%), controle 15 de 81 (18,5%). | |
| risco de morte/intubação/UTI, 62,4% maior , RR 1,62, p = 0,27, tratamento 8 de 21 (38,1%), controle 19 de 81 (23,5%). | |
| [ George ] , 27/05/2022, Ensaio Controlado Randomizado, Índia, Sul da Ásia, revisado por pares, 15 autores, período de estudo junho de 2020 a fevereiro de 2021, dosagem de 24 mg em dose única, ensaio CTRI/2020/05/025068.Envie correções ou atualizações . | risco de morte, 30,4% menor , RR 0,70, p = 0,55 , tratamento 5 de 35 (14,3%), controle 8 de 39 (20,5%), NNT 16, 24mg. |
| risco de morte, 2,6% maior , RR 1,03, p = 1,00, tratamento 8 de 38 (21,1%), controle 8 de 39 (20,5%), 12mg. | |
| tempo de recuperação, 18,7% menor , tempo relativo 0,81, p = 0,37, média de tratamento 4,82 (±4,35) n=35, média de controle 5,93 (±5,93) n=39, 24mg. | |
| tempo de recuperação, 6,2% menor , tempo relativo 0,94, p = 0,78, média de tratamento 5,56 (±5,42) n=38, média de controle 5,93 (±5,93) n=39, 12mg. | |
| risco de progressão, 33,1% menor , RR 0,67, p = 0,41, tratamento 6 de 35 (17,1%), controle 10 de 39 (25,6%), NNT 12, 24mg. | |
| risco de progressão, 17,9% menor , RR 0,82, p = 0,79, tratamento 8 de 38 (21,1%), controle 10 de 39 (25,6%), NNT 22, 12mg. | |
| [ Gorial ] , 08/07/2020, retrospectiva, Iraque, Oriente Médio, pré-impressão, 9 autores, dosagem 200μg/kg dose única.Envie correções ou atualizações . | risco de morte, 71,0% menor , RR 0,29, p = 1,00 , tratamento 0 de 16 (0,0%), controle 2 de 71 (2,8%), NNT 36, risco relativo não é 0 por causa da correção de continuidade devido a zero eventos ( com o recíproco do braço contrastante). |
| tempo de internação, 42,0% menor , tempo relativo 0,58, p < 0,001, tratamento 16, controle 71. | |
| risco de não recuperação, 71,0% menor , RR 0,29, p = 1,00, tratamento 0 de 16 (0,0%), controle 2 de 71 (2,8%), NNT 36, risco relativo não é 0 devido à correção de continuidade devido a zero eventos (com recíproca do braço contrastante), desfecho primário. | |
| [ Hashim ] , 26/10/2020, Ensaio Controlado Aleatório Randomizado Único, Iraque, Oriente Médio, revisado por pares, 7 autores, dosagem 200μg/kg dias 1-2, alguns pacientes receberam uma terceira dose no dia 8, este estudo usa vários tratamentos no braço de tratamento (combinado com doxiciclina) – os resultados de tratamentos individuais podem variar, ensaio NCT04591600 .Envie correções ou atualizações . | risco de morte, 91,7% menor , RR 0,08, p = 0,03 , tratamento 0 de 59 (0,0%), controle 6 de 70 (8,6%), NNT 12, risco relativo não é 0 por causa da correção de continuidade devido a zero eventos ( com recíproca do braço contrastante), excluindo pacientes críticos não randomizados, desfecho primário. |
| risco de morte, 67,1% menor , RR 0,33, p = 0,16, tratamento 2 de 70 (2,9%), controle 6 de 70 (8,6%), NNT 18, odds ratio convertido em risco relativo, incluindo pacientes críticos que sempre foram alocados ao tratamento. | |
| risco de progressão, 83,1% menor , RR 0,17, p = 0,07, tratamento 1 de 59 (1,7%), controle 7 de 70 (10,0%), NNT 12, excluindo pacientes críticos não randomizados. | |
| risco de progressão, 57,4% menor , RR 0,43, p = 0,20, tratamento 3 de 70 (4,3%), controle 7 de 70 (10,0%), NNT 18, odds ratio convertido em risco relativo, incluindo pacientes críticos que sempre foram alocados ao tratamento. | |
| tempo de recuperação, 40,7% menor , tempo relativo 0,59, p < 0,001, tratamento 70, controle 70. | |
| [ Hazan ] , 7/7/2021, retrospectivo, EUA, América do Norte, pré-impressão, 7 autores, atraso médio no tratamento 9,2 dias, dosagem 12mg dias 1, 4, 8, este estudo usa vários tratamentos no braço de tratamento (combinado com doxiciclina , zinco, vitamina D, vitamina C) – os resultados dos tratamentos individuais podem variar, excluídos nas análises de exclusão: o estudo usa um braço de controle sintético.Envie correções ou atualizações . | risco de morte, 86,2% menor , RR 0,14, p = 0,04 , NNT 6,9, risco relativo não é 0 devido à correção de continuidade devido a zero eventos (com recíproca do braço contrastante). |
| risco de hospitalização, 93,5% menor , RR 0,07, p = 0,001, NNT 3,3, risco relativo não é 0 devido à correção de continuidade devido a zero eventos (com recíproca do braço contrastante), desfecho primário. | |
| [ Huvemek ] , 25/03/2021, Ensaio controlado randomizado duplo-cego, Bulgária, Europa, pré-impressão, 1 autor, atraso médio no tratamento 7,0 dias, dosagem 400μg/kg dias 1-3.Envie correções ou atualizações . | risco de nenhuma melhora, 31,6% menor , RR 0,68, p = 0,28 , tratamento 13 de 50 (26,0%), controle 19 de 50 (38,0%), NNT 8,3, dia 7, pacientes com melhora na escala da OMS. |
| risco de nenhuma melhora, 34,5% menor , RR 0,66, p = 0,07, tratamento 19 de 50 (38,0%), controle 29 de 50 (58,0%), NNT 5,0, dia 4, pacientes com melhora na escala da OMS. | |
| [ Jamir ] , 13/12/2021, retrospectivo, Índia, Sul da Ásia, revisado por pares, 6 autores, período de estudo junho de 2020 a outubro de 2010, dosagem não especificada.Envie correções ou atualizações . | risco de morte, 53,0% maior , RR 1,53, p = 0,13 , tratamento 32 de 76 (42,1%), controle 69 de 190 (36,3%), ajustado por estudo, regressão de Cox multivariável. |
| [ Khan ] , 24/09/2020, retrospectiva, Bangladesh, Sul da Ásia, pré-impressão, idade mediana 35,0, 8 autores, dosagem de 12mg em dose única.Envie correções ou atualizações . | risco de morte, 87,1% menor , RR 0,13, p = 0,02 , tratamento 1 de 115 (0,9%), controle 9 de 133 (6,8%), NNT 17. |
| risco de internação na UTI, 89,5% menor , RR 0,11, p = 0,007, tratamento 1 de 115 (0,9%), controle 11 de 133 (8,3%), NNT 14. | |
| risco de progressão, 83,5% menor , RR 0,17, p < 0,001, tratamento 3 de 115 (2,6%), controle 21 de 133 (15,8%), NNT 7,6. | |
| risco de não recuperação, 87,1% menor , RR 0,13, p = 0,02, tratamento 1 de 115 (0,9%), controle 9 de 133 (6,8%), NNT 17. | |
| tempo de internação, 40,0% menor , tempo relativo 0,60, p < 0,001, tratamento 115, controle 133. | |
| tempo para viral, 73,3% menor , tempo relativo 0,27, p < 0,001, tratamento 115, controle 133. | |
| [ Kishória ] , 31/08/2020, Ensaio Controlado Randomizado, Índia, Sul da Ásia, revisado por pares, 7 autores, dosagem de 12mg em dose única, excluído nas análises de exclusão: diferenças excessivas não ajustadas entre os grupos.Envie correções ou atualizações . | risco de não alta hospitalar, 7,5% maior , RR 1,08, p = 1,00 , tratamento 11 de 19 (57,9%), controle 7 de 13 (53,8%). |
| risco de ausência de depuração viral, 7,5% maior , RR 1,08, p = 1,00, tratamento 11 de 19 (57,9%), controle 7 de 13 (53,8%), dia 3, desfecho primário. | |
| risco de ausência de depuração viral, 220,0% maior , RR 3,20, p = 0,45, tratamento 1 de 5 (20,0%), controle 0 de 6 (0,0%), correção de continuidade devido a evento zero (com recíproca do braço contrastante), dia 5. | |
| [ Lim ] , 3/11/2021, Ensaio Controlado Randomizado, Malásia, Europa, revisado por pares, 26 autores, período de estudo 31 de maio de 2021 – 9 de outubro de 2021, atraso médio no tratamento 5,1 dias, dosagem 400μg/kg dias 1- 5, julgamento NCT04920942 (I-TECH).Envie correções ou atualizações . | risco de morte, 69,0% menor , RR 0,31, p = 0,09 , tratamento 3 de 241 (1,2%), controle 10 de 249 (4,0%), NNT 36. |
| risco de morte, 75,2% menor , RR 0,25, p = 0,02, tratamento 3 de 52 (5,8%), controle 10 de 43 (23,3%), NNT 5,7, entre pacientes que evoluíram para casos graves (principalmente antes do término do tratamento). | |
| risco de ventilação mecânica, 59,0% menor , RR 0,41, p = 0,17, tratamento 4 de 241 (1,7%), controle 10 de 249 (4,0%), NNT 42. | |
| risco de internação na UTI, 22,0% menor , RR 0,78, p = 0,79, tratamento 6 de 241 (2,5%), controle 8 de 249 (3,2%), NNT 138. | |
| risco de progressão, 31,1% menor , RR 0,69, p = 0,29, tratamento 14 de 241 (5,8%), controle 21 de 249 (8,4%), NNT 38, óbito/IMV/NIV/alto fluxo (casos graves da OMS). | |
| risco de progressão, 25,0% maior , RR 1,25, p = 0,25, tratamento 52 de 241 (21,6%), controle 43 de 249 (17,3%), desfecho primário. | |
| tempo de internação, 5,5% maior , tempo relativo 1,05, p = 0,38, tratamento 241, controle 249. | |
| risco de não recuperação, 2,5% maior , RR 1,02, p = 0,86, tratamento 116 de 241 (48,1%), controle 116 de 247 (47,0%), dia 5. | |
| [ Lima-Morales ] , 10/02/2021, prospectivo, México, América do Norte, revisado por pares, 9 autores, atraso médio no tratamento de 7,2 dias, dosagem de 12mg em dose única, este estudo usa vários tratamentos no braço de tratamento (combinado com azitromicina , montelucaste e aspirina) – os resultados dos tratamentos individuais podem variar.Envie correções ou atualizações . | risco de morte, 77,7% menor , RR 0,22, p < 0,001 , tratamento 15 de 481 (3,1%), controle 52 de 287 (18,1%), NNT 6,7, ajustado por estudo, odds ratio convertido em risco relativo, multivariado. |
| risco de ventilação mecânica, 51,9% menor , RR 0,48, p = 0,15, tratamento 8 de 434 (1,8%), controle 11 de 287 (3,8%), NNT 50. | |
| risco de internação, 67,4% menor , RR 0,33, p < 0,001, tratamento 44 de 481 (9,1%), controle 89 de 287 (31,0%), NNT 4,6, ajustado por estudo, odds ratio convertido em risco relativo, multivariado. | |
| risco de não recuperação, 58,6% menor , RR 0,41, p < 0,001, tratamento 75 de 481 (15,6%), controle 118 de 287 (41,1%), NNT 3,9, ajustado por estudo, odds ratio convertido em risco relativo, recuperação em dia 14 após os sintomas, multivariada. | |
| [ Mustafa ] , 29/12/2021, retrospectivo, Paquistão, Sul da Ásia, revisado por pares, 7 autores, dosagem varia, excluído em análises de exclusão: resultados não ajustados sem detalhes do grupo.Envie correções ou atualizações . | risco de morte, 63,7% menor , RR 0,36, p = 0,09 , tratamento 3 de 73 (4,1%), controle 42 de 371 (11,3%), NNT 14. |
| [ Naggie ] , 12/06/2022, Ensaio controlado randomizado duplo cego, controlado por placebo, EUA, América do Norte, pré-impressão, idade média 48,0, 1 autor, período de estudo 15 de dezembro de 2021 – 1 de fevereiro de 2022, atraso médio no tratamento 6,0 dias, dosagem 400μg/kg dias 1-3, ensaio NCT04885530 .Envie correções ou atualizações . | risco de morte, 194,7% maior , RR 2,95, p = 1,00 , tratamento 1 de 817 (0,1%), controle 0 de 774 (0,0%), correção de continuidade devido a evento zero (com recíproca do braço contrastante), dia 28 . |
| risco de hospitalização, 5,3% maior , RR 1,05, p = 1,00, tratamento 10 de 817 (1,2%), controle 9 de 774 (1,2%), dia 28. | |
| risco de progressão, 68,4% menor , RR 0,32, p = 0,36, tratamento 1 de 817 (0,1%), controle 3 de 774 (0,4%), NNT 377, pneumonia C19 agravada. | |
| risco de progressão, 5,3% menor , RR 0,95, p = 1,00, tratamento 4 de 817 (0,5%), controle 4 de 774 (0,5%), NNT 3676, pneumonia C19. | |
| risco de progressão, 20,0% maior , RR 1,20, p = 0,32, tratamento 32 de 817 (3,9%), controle 28 de 774 (3,6%), ajustado por estudo, atendimentos de urgência ou emergência, hospitalizações ou óbito. | |
| risco de não recuperação, 6,5% menor , HR 0,93, p = 0,18, tratamento 817, controle 774, desfecho primário. | |
| risco de não recuperação, 44,1% menor , HR 0,56, p = 0,03, tratamento 39, controle 51, grave. | |
| risco de não recuperação, 2,9% menor , HR 0,97, p = 0,80, tratamento 247, controle 221, moderado. | |
| risco de não recuperação, 10,7% menor , HR 0,89, p = 0,12, tratamento 434, controle 490, leve. | |
| risco de não recuperação, 10,7% menor , HR 0,89, p = 0,12, tratamento 54, controle 55, sem sintomas. | |
| risco de não recuperação, 5,7% menor , HR 0,94, p = 0,62, início 3 dias. | |
| risco de não recuperação, 13,8% menor , HR 0,86, p = 0,03, início 5 dias. | |
| risco de não recuperação, 12,3% menor , HR 0,88, p = 0,08, início 7 dias. | |
| risco de não recuperação, sem alteração , HR 1,00, p = 1,00, início 9 dias. | |
| risco de não recuperação, 16,3% maior , HR 1,16, p = 0,40, início 11 dias. | |
| risco de não recuperação, 35,1% maior , HR 1,35, p = 0,28, início 13 dias. | |
| [ Okumuş ] , 1/12/2021, Ensaio controlado randomizado duplo-cego, Turquia, Europa, revisado por pares, 15 autores, dosagem 200μg/kg dias 1-5, 36-50kg – 9mg, 51-65kg – 12mg, 66- 79kg – 15mg, >80kg 200μg/kg, ensaio NCT04646109 .Envie correções ou atualizações . | risco de morte, 33,3% menor , RR 0,67, p = 0,55 , tratamento 6 de 30 (20,0%), controle 9 de 30 (30,0%), NNT 10. |
| risco de nenhuma melhora no dia 10, 42,9% menor , RR 0,57, p = 0,18, tratamento 8 de 30 (26,7%), controle 14 de 30 (46,7%), NNT 5,0. | |
| risco de nenhuma melhora no dia 5, 15,8% menor , RR 0,84, p = 0,60, tratamento 16 de 30 (53,3%), controle 19 de 30 (63,3%), NNT 10, desfecho primário. | |
| risco de ausência de depuração viral, 80,0% menor , RR 0,20, p = 0,02, tratamento 2 de 16 (12,5%), controle 5 de 8 (62,5%), NNT 2,0, dia 10. | |
| [ Ozer ] , 23/11/2021, prospectivo, EUA, América do Norte, revisado por pares, 12 autores, dosagem 200μg/kg dias 1, 3.Envie correções ou atualizações . | risco de morte, 75,0% menor , RR 0,25, p = 0,09 , tratamento 2 de 60 (3,3%), controle 8 de 60 (13,3%), NNT 10,0, PSM. |
| risco de ventilação mecânica, 12,6% menor , RR 0,87, p = 0,20, tratamento 3 de 60 (5,0%), controle 2 de 60 (3,3%), odds ratio convertido em risco relativo, PSM, multivariável. | |
| tempo de ventilação, 83,3% menor , tempo relativo 0,17, p = 0,002, tratamento 60, controle 60. | |
| risco de internação na UTI, 48,7% menor , RR 0,51, p = 0,42, tratamento 6 de 60 (10,0%), controle 3 de 60 (5,0%), odds ratio convertido em risco relativo, PSM, multivariável. | |
| Tempo de UTI, 70,6% menor , tempo relativo 0,29, p < 0,001, tratamento 60, controle 60. | |
| tempo de internação, 9,0% maior , tempo relativo 1,09, p = 0,09, tratamento 60, controle 60, PSM, multivariável. | |
| [ Podder ] , 03/09/2020, Ensaio Controlado Randomizado, Bangladesh, Sul da Ásia, revisado por pares, 4 autores, atraso médio no tratamento de 7,0 dias, dosagem de 200μg/kg em dose única.Envie correções ou atualizações . | tempo de recuperação da inscrição, 16,1% menor , tempo relativo 0,84, p = 0,34 , tratamento 32, controle 30. |
| [ Pott-Junior ] , 09/03/2021, Ensaio Controlado Randomizado, Brasil, América do Sul, revisado por pares, 10 autores, atraso médio no tratamento 8,0 dias, dosagem 200μg/kg dose única, dose varia em três braços 100, 200, 400μg/kg, ensaio NCT04431466 .Envie correções ou atualizações . | risco de ventilação mecânica, 85,2% menor , RR 0,15, p = 0,25 , tratamento 1 de 27 (3,7%), controle 1 de 4 (25,0%), NNT 4,7. |
| risco de internação na UTI, 85,2% menor , RR 0,15, p = 0,25, tratamento 1 de 27 (3,7%), controle 1 de 4 (25,0%), NNT 4,7. | |
| melhora relativa no valor de Ct, 0,8% melhor , RR 0,99, p = 1,00, tratamento 27, controle 3. | |
| risco de ausência de depuração viral, 11,1% maior , RR 1,11, p = 1,00, tratamento 10 de 27 (37,0%), controle 1 de 3 (33,3%), desfecho primário. | |
| [ Rajter ] , 13/10/2020, retrospectivo, correspondência de escore de propensão, EUA, América do Norte, revisado por pares, 6 autores, dosagem 200μg/kg dose única.Envie correções ou atualizações . | risco de morte, 46,0% menor , RR 0,54, p = 0,045 , tratamento 13 de 98 (13,3%), controle 24 de 98 (24,5%), NNT 8,9, ajustado por estudo, odds ratio convertido em risco relativo, PSM. |
| risco de morte, 66,9% menor , RR 0,33, p = 0,03, tratamento 26 de 173 (15,0%), controle 27 de 107 (25,2%), NNT 9,8, ajustado por estudo, odds ratio convertido em risco relativo, multivariado, primário resultado. | |
| risco de ventilação mecânica, 63,6% menor , RR 0,36, p = 0,10, tratamento 4 de 98 (4,1%), controle 11 de 98 (11,2%), NNT 14, coorte pareada excluindo intubados no início do estudo. | |
| [ Ravikirti ] , 4/6/2022, retrospectivo, Índia, Sul da Ásia, pré-impressão, 7 autores, período de estudo 1 de abril de 2021 – 15 de maio de 2021, dosagem varia, excluída em análises de exclusão: exclusão de pacientes em condição menos grave, preocupações de dados/análises.Envie correções ou atualizações . | risco de morte, 2,8% menor , RR 0,97, p = 0,82 , tratamento 53 de 171 (31,0%), controle 254 de 794 (32,0%), NNT 100, odds ratio convertido em risco relativo. |
| [ Rezk ] , 30/10/2021, prospectivo, Egito, África, revisado por pares, 4 autores, dosagem 36mg dias 1, 3, 6.Envie correções ou atualizações . | risco de morte, 80,0% menor , RR 0,20, p = 0,50 , tratamento 0 de 160 (0,0%), controle 2 de 160 (1,2%), NNT 80, risco relativo não é 0 devido à correção de continuidade devido a zero eventos ( com o recíproco do braço contrastante). |
| risco de progressão, 55,6% menor , RR 0,44, p = 0,06, tratamento 8 de 160 (5,0%), controle 18 de 160 (11,2%), NNT 16, 2 semanas, incluindo óbitos. | |
| risco de não recuperação, 33,4% menor , RR 0,67, p = 0,27, tratamento 14 de 145 (9,7%), controle 20 de 138 (14,5%), NNT 21, 4 semanas, mais pacientes foram perdidos para acompanhamento no grupo controle . | |
| tempo para viral, 27,3% menor , tempo relativo 0,73, p = 0,01, tratamento 160, controle 160. | |
| [ Shahbaznejad ] , 19/01/2021, Ensaio controlado randomizado duplo cego, Irã, Oriente Médio, revisado por pares, 8 autores, atraso médio no tratamento de 6,29 dias, dosagem de 200μg/kg em dose única.Envie correções ou atualizações . | risco de morte, 197,1% maior , RR 2,97, p = 1,00 , tratamento 1 de 35 (2,9%), controle 0 de 34 (0,0%), correção de continuidade devido a evento zero (com recíproca do braço contrastante), paciente faleceu dentro de 24 horas da admissão. |
| risco de ventilação mecânica, 94,3% maior , RR 1,94, p = 1,00, tratamento 2 de 35 (5,7%), controle 1 de 34 (2,9%). | |
| tempo de recuperação, 31,6% menor , tempo relativo 0,68, p = 0,048, tratamento 35, controle 34, duração da dispneia. | |
| tempo de recuperação, 19,2% menor , tempo relativo 0,81, p = 0,02, tratamento 35, controle 34, duração de todos os sintomas, desfecho primário. | |
| tempo de internação, 15,5% menor , tempo relativo 0,85, p = 0,02, tratamento 35, controle 34. | |
| [ Shimizu ] , 31/12/2021, retrospectivo, Japão, Ásia, revisado por pares, 11 autores, período de estudo dezembro de 2020 – maio de 2021, dosagem 200μg/kg dias 1, 14.Envie correções ou atualizações . | risco de morte, 99,9% menor , HR 0,001, p < 0,001 , tratamento 0 de 39 (0,0%), controle 8 de 49 (16,3%), NNT 6,1, ajustado por estudo, regressão de risco proporcional de Cox. |
| dias livres de ventilador, 47,9% menor , OR 0,52, p = 0,03, tratamento 39, controle 49, ajustado por estudo, regressão logística de probabilidades proporcionais, desfecho primário, RR aproximado com OR. | |
| tempo de ventilação, 38,5% menor , tempo relativo 0,62, p < 0,001, tratamento 39, controle 49. | |
| Dias livres de UTI, 42,8% menor , OR 0,57, p = 0,06, tratamento 39, controle 49, ajustado por estudo, regressão logística de odds proporcionais, RR aproximado com OR. | |
| Tempo de UTI, 37,5% menor , tempo relativo 0,62, p < 0,001, tratamento 39, controle 49. | |
| Complicações gastrointestinais durante a ventilação, 77,9% menor , RR 0,22, p = 0,03, tratamento 39, controle 49, ajustado por estudo, regressão de risco proporcional de Cox. | |
| [ Soto ] , 02/03/2022, retrospectivo, Peru, América do Sul, revisado por pares, idade mediana 58,0, 10 autores, período de estudo abril de 2020 – agosto de 2020, dosagem não especificada, excluída em análises de exclusão: confusão substancial não ajustada por indicação provável, confusão substancial pelo tempo possível devido a mudanças significativas no SOC e na propensão ao tratamento perto do início da pandemia.Envie correções ou atualizações . | risco de morte, 41,0% maior , HR 1,41, p = 0,001 , tratamento 280 de 484 (57,9%), controle 374 de 934 (40,0%), ajustado por estudo, multivariável. |
| [ Soto-Becerra ] , 8/10/2020, retrospectivo, análise de banco de dados, Peru, América do Sul, pré-impressão, idade mediana 59,4, 4 autores, período de estudo 1 de abril de 2020 – 19 de julho de 2020, dosagem 200μg/kg dose única, excluído em análises de exclusão: confusão não ajustada substancial por indicação provável, inclui pacientes PCR+ que podem ser assintomáticos para COVID-19, mas hospitalizados por outros motivos.Envie correções ou atualizações . | risco de morte, 17,1% menor , HR 0,83, p = 0,01 , tratamento 92 de 203 (45,3%), controle 1.438 de 2.630 (54,7%), NNT 11, IVM vs. controle dia 43 (último dia disponível) KM ponderado de Figura 3, de acordo com as regras pré-especificadas, os resultados de mortalidade do último dia disponíveis têm prioridade. |
| risco de morte, 39,0% maior , HR 1,39, p = 0,16, tratamento 47 de 203 (23,2%), controle 401 de 2.630 (15,2%), ajustado por estudo, dia 30, Tabela 2, IVM wHR, desfecho primário. | |
| [ Spoorthi ] , 14/11/2020, prospectivo, Índia, Sul da Ásia, revisado por pares, 2 autores, dosagem não especificada, este estudo usa vários tratamentos no braço de tratamento (combinado com doxiciclina) – os resultados dos tratamentos individuais podem variar.Envie correções ou atualizações . | tempo de recuperação, 21,1% menor , tempo relativo 0,79, p = 0,03 , tratamento 50, controle 50. |
| tempo de internação, 15,5% menor , tempo relativo 0,84, p = 0,01, tratamento 50, controle 50. | |
| [ Thairu ] , 25/02/2022, retrospectivo, Nigéria, África, pré-impressão, 5 autores, período de estudo abril de 2021 – novembro de 2021, dosagem 200μg/kg dias 1-5, excluídos em análises de exclusão: confusão significativa por tempo possível devido a separação de grupos em diferentes períodos de tempo.Envie correções ou atualizações . | risco de morte, 87,9% menor , RR 0,12, p = 0,12 , tratamento 0 de 21 (0,0%), controle 4 de 26 (15,4%), NNT 6,5, risco relativo não é 0 devido à correção de continuidade devido a zero eventos ( com o recíproco do braço contrastante), emparelhamento de escore de propensão. |
| risco de morte, 93,0% menor , RR 0,07, p = 0,007, tratamento 0 de 61 (0,0%), controle 4 de 26 (15,4%), NNT 6,5, risco relativo não é 0 por causa da correção de continuidade devido a zero eventos ( com recíproca do braço contrastante), todos os pacientes. | |
| tempo para alta, 54,6% menor , tempo relativo 0,45, p < 0,001, tratamento 61, controle 26, correspondência de escore de propensão. | |
| risco de ausência de depuração viral, 94,8% menor , RR 0,05, p = 0,001, tratamento 0 de 21 (0,0%), controle 10 de 26 (38,5%), NNT 2,6, risco relativo não é 0 devido à correção de continuidade devido a zero eventos (com recíproca do braço contrastante), correspondência de pontuação de propensão, dia 21. | |
| risco de ausência de depuração viral, 95,2% menor , RR 0,05, p < 0,001, tratamento 1 de 21 (4,8%), controle 26 de 26 (100,0%), NNT 1,1, correspondência de pontuação de propensão, dia 14. | |
| risco de ausência de depuração viral, 28,6% menor , RR 0,71, p = 0,005, tratamento 15 de 21 (71,4%), controle 26 de 26 (100,0%), NNT 3,5, correspondência de pontuação de propensão, dia 5. | |
| [ Zubair ] , 18/01/2022, retrospectivo, Paquistão, Sul da Ásia, revisado por pares, 8 autores, período de estudo outubro de 2020 – fevereiro de 2021, dosagem de 12 mg em dose única, excluído em análises de exclusão: confusão substancial não ajustada por indicação provável, não ajustada resultados sem detalhes do grupo.Envie correções ou atualizações . | risco de morte, 9,0% maior , RR 1,09, p = 1,00 , tratamento 5 de 90 (5,6%), controle 5 de 98 (5,1%), não ajustado. |
| tempo de internação, 8,0% maior , tempo relativo 1,08, p = 0,40, tratamento 90, controle 98, não ajustado, Tabela 3, média de dias. |
Profilaxia.A extração de efeitos segue regras pré-especificadas conforme detalhado acima e dá prioridade a resultados mais sérios. Apenas o primeiro resultado (mais grave) é usado na análise agrupada, que pode diferir do efeito no qual um artigo se concentra. Outros resultados são usados em análises específicas de resultados.
| [ Alam ] , 15/12/2020, prospectivo, Bangladesh, Sul da Ásia, revisado por pares, 13 autores, dosagem 12mg mensal.Envie correções ou atualizações . | risco de caso, 90,6% menor , RR 0,09, p < 0,001 , tratamento 4 de 58 (6,9%), controle 44 de 60 (73,3%), NNT 1,5. |
| [ Behera (B) ] , 15/02/2021, prospectivo, Índia, Sul da Ásia, revisado por pares, 14 autores, dosagem 300μg/kg dias 1, 4.Envie correções ou atualizações . | risco de caso, 83,0% menor , RR 0,17, p < 0,001 , tratamento 45 de 2.199 (2,0%), controle 133 de 1.147 (11,6%), NNT 10, duas doses, desfecho primário. |
| [ Behera ] , 3/11/2020, retrospectivo, Índia, Sul da Ásia, revisado por pares, 13 autores, dosagem 300μg/kg dias 1, 4.Envie correções ou atualizações . | risco de caso, 53,8% menor , RR 0,46, p < 0,001 , tratamento 41 de 117 (35,0%), controle 145 de 255 (56,9%), NNT 4,6, ajustado por estudo, odds ratio convertido em risco relativo, modelo 2 2 + doses de regressão logística condicional. |
| [ Bernigaud ] , 28/11/2020, retrospectivo, França, Europa, revisado por pares, 12 autores, dosagem 200μg/kg dias 1, 8, 15, 400μg/kg dias 1, 8, 15, duas dosagens diferentes.Envie correções ou atualizações . | risco de morte, 99,4% menor , RR 0,006, p = 0,08 , tratamento 0 de 69 (0,0%), controle 150 de 3.062 (4,9%), NNT 20, risco relativo não é 0 devido à correção de continuidade devido a zero eventos ( com o recíproco do braço contrastante). |
| risco de caso, 55,1% menor , RR 0,45, p = 0,01, tratamento 7 de 69 (10,1%), controle 692 de 3.062 (22,6%), NNT 8,0. | |
| [ Carvallo ] , 17/11/2020, prospectivo, Argentina, América do Sul, revisado por pares, 4 autores, dosagem 12mg semanalmente, este estudo usa vários tratamentos no braço de tratamento (combinado com iota-carragenina) – os resultados de tratamentos individuais podem variam, excluídos em análises de exclusão: preocupação com possíveis problemas de dados.Envie correções ou atualizações . | risco de caso, 99,9% menor , RR 0,001, p < 0,001 , tratamento 0 de 788 (0,0%), controle 237 de 407 (58,2%), NNT 1,7, risco relativo não é 0 devido à correção de continuidade devido a zero eventos ( com o recíproco do braço contrastante). |
| [ Carvallo (B) ] , 19/10/2020, prospectivo, Argentina, América do Sul, pré-impressão, 1 autor, dosagem 1mg dias 1-14, este estudo usa vários tratamentos no braço de tratamento (combinado com iota-carragenina) – resultados dos tratamentos individuais podem variar, excluídos nas análises de exclusão: preocupação com possíveis problemas de dados.Envie correções ou atualizações . | risco de caso, 96,3% menor , RR 0,04, p < 0,001 , tratamento 0 de 131 (0,0%), controle 11 de 98 (11,2%), NNT 8,9, risco relativo não é 0 devido à correção de continuidade devido a zero eventos ( com o recíproco do braço contrastante). |
| [ Chahla (B) ] , 1/11/2021, Ensaio Controlado Randomizado, Argentina, América do Sul, revisado por pares, 11 autores, dosagem de 12mg semanalmente, este ensaio usa vários tratamentos no braço de tratamento (combinado com iota-carragenina) – os resultados dos tratamentos individuais podem variar, ensaio NCT04701710 .Envie correções ou atualizações . | risco de caso moderado/grave, 95,2% menor , RR 0,05, p = 0,002 , tratamento 0 de 117 (0,0%), controle 10 de 117 (8,5%), NNT 12, risco relativo não é 0 devido à correção de continuidade devido a zero eventos (com recíproca do braço contrastante), COVID-19 moderado/severo. |
| risco de caso, 84,0% menor , RR 0,16, p = 0,004, tratamento 4 de 117 (3,4%), controle 25 de 117 (21,4%), NNT 5,6, ajustado por estudo, odds ratio convertido em risco relativo, todos os casos, resultado primário. | |
| [ Hellwig ] , 28/11/2020, retrospectivo, estudo ecológico, vários países, várias regiões, revisado por pares, 2 autores, dosagem 200μg/kg, dose variada, tipicamente 150-200μg/kg, excluído em análises de exclusão: não um ensaio típico, análise de países africanos que usaram ou não a profilaxia com ivermectina para infecções parasitárias.Envie correções ou atualizações . | risco de caso, 78,0% menor , RR 0,22, p < 0,02 , países africanos, PCTI vs. sem PCT, casos relativos per capita. |
| [ IVERCOR PREP ] , 20/12/2020, retrospectivo, Argentina, América do Sul, preprint, 1 autor, dosagem 12mg semanal, excluído em análises de exclusão: detalhes mínimos fornecidos.Envie correções ou atualizações . | risco de caso, 73,4% menor , RR 0,27, p < 0,001 , tratamento 13 de 389 (3,3%), controle 61 de 486 (12,6%), NNT 11. |
| [ Kerr ] , 11/12/2021, retrospectivo, correspondência de pontuação de propensão, Brasil, América do Sul, revisado por pares, 9 autores, período de estudo julho de 2020 – dezembro de 2020, dosagem 200μg/kg dias 1, 2, 16, 17, 0,2 mg/kg/dia por 2 dias a cada 15 dias.Envie correções ou atualizações . | risco de morte, 70,0% menor , RR 0,30, p < 0,001 , tratamento 25 de 3.034 (0,8%), controle 79 de 3.034 (2,6%), NNT 56, ajustado por estudo, regressão linear multivariada, correspondência de escore de propensão. |
| risco de internação, 67,0% menor , RR 0,33, p < 0,001, tratamento 44 de 3.034 (1,5%), controle 99 de 3.034 (3,3%), ajustado por estudo, regressão linear multivariada, pareamento por escore de propensão. | |
| risco de caso, 44,5% menor , RR 0,56, p < 0,001, tratamento 4.197 de 113.845 (3,7%), controle 3.034 de 45.716 (6,6%), NNT 34. | |
| [ Mondal ] , 31/05/2021, retrospectivo, Índia, Sul da Ásia, revisado por pares, 11 autores, dosagem não especificada.Envie correções ou atualizações . | risco de caso sintomático, 87,9% menor , RR 0,12, p = 0,006 , tratamento 128, controle 1.342, ajustado por estudo, odds ratio convertido em risco relativo, prevalência de controle aproximada com prevalência global, multivariável, desfecho primário. |
| [ Morgenstern ] , 16/04/2021, retrospectivo, propensity score matching, República Dominicana, Caribe, revisado por pares, 16 autores, dosagem 200μg/kg semanalmente, ensaio NCT04832945 .Envie correções ou atualizações . | risco de hospitalização, 80,0% menor , RR 0,20, p = 0,50 , tratamento 0 de 271 (0,0%), controle 2 de 271 (0,7%), NNT 136, risco relativo não é 0 por causa da correção de continuidade devido a zero eventos ( com recíproca do braço contrastante), PSM. |
| risco de caso, 74,0% menor , RR 0,26, p = 0,008, tratamento 5 de 271 (1,8%), controle 18 de 271 (6,6%), NNT 21, ajustado por estudo, PSM, regressão multivariada de Cox, desfecho primário. | |
| [ Samajdar ] , 17/11/2021, retrospectivo, Índia, Sul da Ásia, revisado por pares, 9 autores, período de estudo 1 de setembro de 2020 – 31 de dezembro de 2020, dosagem não especificada, excluída em análises de exclusão: detalhes mínimos fornecidos, não ajustados resultados sem detalhes do grupo, os resultados podem ser significativamente afetados pelo viés da pesquisa.Envie correções ou atualizações . | risco de caso, 79,8% menor , RR 0,20, p < 0,001 , tratamento 12 de 164 (7,3%), controle 29 de 81 (35,8%), NNT 3,5, odds ratio convertido em risco relativo, pesquisa médica. |
| risco de caso, 48,6% menor , RR 0,51, p = 0,03, tratamento 11 de 109 (10,1%), controle 39 de 200 (19,5%), NNT 11, odds ratio convertido em risco relativo, ivermectina combinada ou HCQ na comunidade. | |
| [ Ver ] , 14/04/2021 , Ensaio Controlado Randomizado em Cluster, Cingapura, Ásia, revisado por pares, 15 autores, dosagem 12mg em dose única, 200µg/kg, máximo 12mg, este ensaio compara com outro tratamento – os resultados podem ser melhores quando comparado com placebo, ensaio NCT04446104 .Envie correções ou atualizações . | risco de caso sintomático, 49,8% menor , RR 0,50, p < 0,001 , tratamento 32 de 617 (5,2%), controle 64 de 619 (10,3%), NNT 19. |
| risco de caso, 5,8% menor , RR 0,94, p = 0,61, tratamento 398 de 617 (64,5%), controle 433 de 619 (70,0%), NNT 18, ajustado por estudo, odds ratio convertido em risco relativo, modelo 6, resultado primário. | |
| [ Shouman ] , 28/08/2020, Ensaio Controlado Randomizado, Egito, África, revisado por pares, 8 autores, dosagem 18mg dias 1, 3, a dose varia dependendo do peso – 40-60kg: 15mg, 60-80kg: 18mg, >80kg: 24mg, ensaio NCT04422561 .Envie correções ou atualizações . | risco de caso sintomático, 91,3% menor , RR 0,09, p < 0,001 , tratamento 15 de 203 (7,4%), controle 59 de 101 (58,4%), NNT 2,0, ajustado por estudo, multivariado, desfecho primário. |
| risco de caso grave, 92,9% menor , RR 0,07, p = 0,002, tratamento 1 de 203 (0,5%), controle 7 de 101 (6,9%), NNT 16, não ajustado. | |
| [ Tanioka ] , 26/03/2021, estudo retrospectivo, ecológico, vários países, várias regiões, pré-impressão, 3 autores, dosagem 200μg/kg, dose variada, tipicamente 150-200μg/kg, excluído em análises de exclusão: não é um estudo típico , análise de países africanos que utilizaram ou não a profilaxia com ivermectina para infecções parasitárias.Envie correções ou atualizações . | risco de morte, 88,2% menor , RR 0,12, p = 0,002 , mortalidade média relativa por milhão. |
Dados suplementaresReferências
Abbas et al., Indian Journal of Pharmaceutical Sciences ,
doi:10.36468/pharmaceutical-sciences.spl.416 ,
The Effect of Ivermectin on Reducing Viral Sintomas in Patients with Mild COVID-19 ,
https://www.ijpsonline.com/abstrac ..tients-with-mild-covid19-4455.html .
Abd-Elsalam et al., Journal of Medical Virology ,
https://onlinelibrary.wiley.com/doi/ 10.1002/jmv.27122 .
https://www.acpjournals.org/doi/10.7326/M21-3221 .
https://actgnetwork.org/2021/07/29..-experience-excessive-weight-gain/ .
https://www.fiercebiotech.com/biot..rug-us-government-asked -comprar .
Ahmed et al., International Journal of Infectious Diseases ,
doi:10.1016/j.ijid.2020.11.191 ,
Um curso de cinco dias de ivermectina para o tratamento de COVID-19 pode reduzir a duração da doença ,
https://www.sciencedirect .com/science/article/pii/S1201971220325066 .
https://www.cureus. com/articles/56..-care-hospital-in-karachi-pakistan .
https://www.ajtmh.org/view/journals/tpmd/104/1/article-p35.xml .
Alam et al., European Journal of Medical and Health Sciences ,
doi:10.24018/ejmed.2020.2.6.599 ,
https:/ /ejmed.org/index.php/ejmed/article/view/599 .
Albariqi et al., International Journal of Pharmaceutics ,
doi:10.1016/j.ijpharm.2022.121688 ,
Pharmacokinetics and Safety of Inhaled Ivermectin in Mice as a Potential COVID-19 Treatment ,
https://www.sciencedirect.com/science/article/ pii/S0378517322002435 .
Albariqi (B) et al., Journal of Aerosol Medicine and Pulmonary Drug Delivery ,
https://www.liebertpub.com/ doi/epub/10.1089/jamp.2021.0059 .
Como obter o valor P de um intervalo de confiança ,
https://www.bmj.com/content/343/bmj.d2304 .
Como obter o intervalo de confiança de um valor P ,
https://www.bmj.com/content/343/bmj.d2090 .
Alvarado et al., Computational Biology and Chemistry ,
doi:10.1016/j.compbiolchem.2022.107692 ,
https://www.sciencedirect.com/science/article/pii/S147692712200072X .
Aminpour et al., Computation ,
doi:10.3390/computation10040051 ,
In Silico Analysis of the Multi-Targeted Mode of Action of Ivermectin and Related Compounds ,
https://www.mdpi.com/2079-3197/10/4/51 .
Amrhein et al., Nature, 567:305-307 ,
Scientists levantar-se contra significância estatística ,
https://www.nature.com/articles/d41586-019-00857-9 .
Anglemyer et al., Cochrane Database of Systematic Reviews 2014, Issue 4 ,
doi:10.1002/14651858.MR000034.pub2 ,
https://www.cochranelibrary.com/ cd..0.1002/14651858.MR000034.pub2/full .
Aref et al., International Journal of Nanomedicine ,
https://www.dovepress.com /clinical..peer-reviewed-fulltext-article-IJN .
Arévalo et al., Scientific Reports ,
doi:10.1038/s41598-021-86679-0 (pré-impressão 2/11/20),
a ivermectina reduz a infecção por coronavírus in vivo em um modelo experimental de camundongo ,
https://www.nature.com/ artigos/s41598-021-86679-0 .
Arise et ai., Afr. J. Biochem. Res., 2009:3 ,
Efeitos da ivermectina e albendazol em alguns índices de função hepática e renal em ratos ,
https://academicjournals.org/journ..article-full-text-pdf/E62326811023 .
https://ars.els-cdn.com/content/im../1-s2.0-S2667193X21001381-mmc3.pdf .
Babalola et al., QJM: An International Journal of Medicine ,
doi:10.1093/qjmed/hcab035 (pré-impressão 1/6),
https://academic.oup.com/qjmed/adv../doi/10.1093/qjmed/hcab035/6143037 .
Baguma et al., Research Square ,
doi:10.21203/rs.3.rs-1193578/v1 ,
https://www .researchsquare.com/article/rs-1193578/v1 .
Baqui et al., The Lancet Global Health ,
doi:10.1016/S2214-109X(20)30285-0 ,
https://www .sciencedirect.com/science/article/pii/S2214109X20302850 .
doi:10.1371/journal.pone.0247163 (pré-impressão 11/3),
https://journals.plos.org/plosone/..le?id=10.1371/journal.pone.0247163 .
Behera (B) et al., Cureus 13:8 ,
doi:10.7759/cureus.16897 (pré-impressão 15/2/21), Prophylactic
https://www .cureus.com/articles/64..infection-entre-healthcare-workers .
Bello et al., Journal of Biomolecular Structure and Dynamics ,
doi:10.1080/07391102.2021.1911857 ,
https://www.tandfonline.com /doi/full/10.1080/07391102.2021.1911857 .
Beltran Gonzalez et al., Infectious Disease Reports ,
doi:10.3390/idr14020020 (pré-impressão 23/02/2021),
https://www. mdpi.com/2036-7449/14/2/20 .
Bernigaud et al., Annals of Dermatology and Venereology ,
doi:10.1016/j.annder.2020.09.231 ,
Benefício da ivermectina: da sarna ao COVID-19, um exemplo de serendipidade ,
https://www.sciencedirect.com/science/ artigo/pii/S015196382030627X .
Bhattacharya et ai., Int. J. Scientific Research ,
https://www.worldwidejournals.com/.. outubro_2020_1614017661_0932284.pdf .
doi:10.1101/2021.05.31.21258081 (resultados 2/12/21),
https://www.medrxiv.org/content/10.1101/2021.05.31.21258081v1 .
O artigo recente da BBC “False Science” se desintegra sob escrutínio ,
https://bird-group.org/the-bbcs-re..-is-disintegrating-under-scrutiny/ .
https://bird-group.org/rebuttal-to-roman-et-al/ .
Bitterman et al., JAMA Network Open ,
doi:10.1001/jamanetworkopen.2022.3079 ,
https://jamanetwork.com/journals/jamanetworkopen/fullarticle/ 2790173 .
https://blogs.bmj.com/bmj/2018/11/..ochrane-no-longer-a-collaboration/ .
bmj.com ,
https://www.bmj.com/content/364/bmj.k5302 .
Borody et al., TrialSite News ,
Combination Therapy For COVID-19 Based on Ivermectin in an Australian Population ,
https://covidmedicalnetwork.com/me..lSite-media-release-19.10.2021.pdf .
Bramante et al., Open Forum Infectious Diseases ,
https://academic.oup.com/ofid/ adva..e/doi/10.1093/ofid/ofac066/6532584 .
doi:10.1016/j.antiviral.2020.104805 ,
https://www.ncbi.nlm .nih.gov/pmc/articles/PMC7172803/ .
Bryant et al., American Journal of Therapeutics ,
doi:10.1097/MJT.0000000000001402 (pré-impressão 11/03/21),
https://journals.lww.com/americant..Prevention_and_Treatment_of.7.aspx .
doi:10.1101/2020.11.16.20232223 ,
https://www.medrxiv.org/ conteúdo/10.1101/2020.11.16.20232223v1 .
doi:10.1101/2021.02.02.21250840 (resultados 1/16),
Efficacy of Ivermectin in COVID-19 Patients with Leve to Moderate Disease ,
https://www.medrxiv.org/content/10.1101/2021.02 .02.21250840v1 .
Buonfrate et al., International Journal of Antimicrobial Agents ,
doi:10.1016/j.ijantimicag.2021.106516 (pré-impressão 06/09/2021),
https://www.sciencedirect.com/science/article/pii/S0924857921013571 .
Buonfrate (B) et al., Pathogens ,
doi:10.3390/pathogens9060468 ,
The Global Prevalence of Strongyloides Stercoralis Infection ,
https://www.mdpi.com/2076-0817/9/6/468 .
Butler et al., The Lancet Respiratory Medicine ,
doi:10.1016/S2213-2600(21)00310-6 ,
https://www.sciencedirect.com/science/article/pii/S2213260021003106 .
https://c19ivermectin.com/lawrieletter.html .
https://c19ivermectin.com/harperhill.html .
https://c19ivermectin.com/files/To..herTrialRandomizationAnalysis.xlsx .
Cadegiani et al., New Microbes and New Infections ,
doi:10.1016/j.nmni.2021.100915 (pré-impressão 04/11/2020),
https://www.sciencedirect.com/science/article/pii/S2052297521000792 .
Caly et al., Antiviral Research ,
doi:10.1016/j.antiviral.2020.104787 ,
The FDA-approved drug ivermectin inibe a replicação do SARS-CoV-2 in vitro ,
https://www.sciencedirect.com/science/article/ pii/S0166354220302011 .
BBC desmascara a ivermectina ,
https://www.youtube.com/watch?v=zy7c_FHiEac .
Camprubí et al., PLoS ONE, 15:11 ,
doi:10.1371/journal.pone.0242184 ,
Falta de eficácia de doses padrão de ivermectina em pacientes graves com COVID-19 ,
https://journals.plos.org/plosone/. .le?id=10.1371/journal.pone.0242184 .
doi:10.1208/s12248-007-9000-9 ,
The Pharmacokinetics and Interactions of Ivermectin in Humans—A Mini-review ,
https://www.ncbi.nlm.nih.gov/pmc /articles/PMC2751445/ .
Carvallo et al., Journal of Biomedical Research and Clinical Investigation ,
https://medicalpressopenaccess .com/upload/1605709669_1007.pdf .
Carvallo (B) et al., NCT04425850 ,
Usefulness of Topic Ivermectin and Carragenan to Prevent Contagion of Covid 19 (IVERCAR) ,
https://clinicaltrials.gov/ct2/show/results/NCT04425850 .
Carvallo (C) et al., Journal of Clinical Trials, 11:459 (pré-impressão 15/09/20) ,
https: //www.longdom.org/open-acces..vid19-the-idea-protocol-70290.html .
https://www.certara.com/pressrelea..ientific-data-access-and-analysis/ .
Chaccour et al., Scientific Reports ,
doi:10.1038/s41598-020-74084-y ,
https://www.nature .com/articles/s41598-020-74084-y .
Chaccour (B) et al., EClinicalMedicine ,
doi:10.1016/j.eclinm.2020.100720 (pré-impressão 12/7),
https://www.thelancet.com/journals../PIIS2589-5370(20)30464-8/fulltext .
Chaccour (C) et ai., Malar. J. ,
doi:10.1186/s12936-017-1801-4 ,
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5402169 / .
Chachar et al., International Journal of Sciences, 9:31-35 ,
Effectiveness of Ivermectin in SARS-CoV-2/COVID-19 Patients ,
https://www.ijsciences.com/pub /artigo/2378 .
Chahla et al., Research Square ,
doi:10.21203/rs.3.rs-495945/v1 (pré-impressão original 3/30),
https://www.researchsquare.com/article/rs-495945/v1 .
Chahla (B) et al., American Journal of Therapeutics ,
doi:10.1097/MJT.0000000000001433 ,
https:/ /www.ncbi.nlm.nih.gov/pmc/articles/PMC8415509/ .
Mais sobre Ivermectina. Este estudo é uma fraude? ,
https://juanchamie.substack.com/p/more-about-ivermectin-is-this-study .
Chamie-Quintero et al., OSF Preprints ,
The Latest Results of Ivermectin’s Success in Treating Outbreaks of COVID-19 ,
https://covid19criticalcare.com/iv..nalyses-on-covid19-and-ivermectin/ .
Charilaou et al., American Journal of Gastroenterology ,
doi:10.14309/00000434-201610001-01012 ,
Acetaminophen Toxicity: Trends in Hospitalization and Their Outcomes in United States from 2002-2011 ,
https://journals.lww.com/ajg/Fullt ..rends_in_Hospitalization.1012.aspx .
Chiu et ai., J. Agric. Química Alimentar. ,
https://pubs.acs.org/doi/abs/10.1021/jf00101a015 .
Choudhury et al., Future Medicine ,
https://www.futuremedicine.com /doi/10.2217/fvl-2020-0342 .
Chowdhury et al., Eurasian Journal of Medicine and Oncology ,
doi:10.14744/ejmo.2021.16263 ,
https://ejmo.org/10.14744/ejmo. 2021.16263/ .
https://clinicaltrials.gov/ct2/show/NCT04092452 .
https://clinicaltrials.gov/ct2/show/NCT04727424 .
https://clinicaltrials.gov/ct2/his..=1&B=2&C=Side-by-Side#StudyPageTop .
https://clinicaltrials.gov/ct2/his../NCT04727424?V_1=View#StudyPageTop .
https://clinicaltrials.gov/ct2/his..7424?A=2&B=3&C=merged#StudyPageTop .
Concato et al., NEJM, 342:1887-1892 ,
doi:10.1056/NEJM200006223422507 ,
https://www.nejm.org/doi/full/10.1056/nejm200006223422507 .
Análise de López-Medina et al. ,
https://c19ivermectin.com/lopezmedina.html .
atualização semanal COVID-NMA, 14 de maio de 2021 ,
https://web.archive.org/web/202105..58/https://www.covid-nma.com/news/ .
https://covid19criticalcare.com/wp..her-Trial-WSJ-Article-Mar-18-1.pdf .
covid19treatmentguidelines.nih.gov ,
https://www.covid19treatmentguidel..elines/panel-financial-disclosure/ .
https://www.cytel.com/blog/an-interview-with-pfizers-chris-conklin .
https://www.cytel.com/news/nordic-..d-advanced-analytics-company-cytel .
https://www.cytel.com/blog/the-tog..tform-trial-for-covid-19-therapies .
https://dcricollab.dcri.duke.edu/sites/NIHKR/KR/GR-Slides-08-06-21.pdf .
de Jesús Ascencio-Montiel et al., Archives of Medical Research ,
doi:10.1016/j.arcmed.2022.01.002 ,
https://www .sciencedirect.com/science/article/pii/S0188440922000029 .
de Melo et ai., EMBO Mol. Med. ,
doi:10.15252/emmm.202114122 (pré-impressão 22/11/20),
Atenuação de resultados clínicos e imunológicos durante a infecção por SARS-CoV-2 por ivermectina ,
https://www.embopress.org/doi/abs/10.15252/emmm .202114122 .
Deaton et al., Social Science & Medicine, 210 ,
doi:10.1016/j.socscimed.2017.12.005 ,
Understanding and mal-entendido randomizado controlado ensaios ,
https://www.sciencedirect.com/science/article/pii/S0277953617307359 .
Delandre et al., Pharmaceuticals ,
https://www.mdpi.com/1424-8247/15 /4/445 .
PyMeta, módulo Python para meta-análise ,
Descotes , J., ImmunoSafe Consultance ,
Medical Safety of Ivermectin ,
https://www.medincell.com/wp-conte.._MDCL_safety_ivermectine-50321.pdf .
DiNicolantonio et al., Open Heart ,
doi:10.1136/openhrt-2020-001350 ,
Ivermectina pode ser um agente anti-inflamatório clinicamente útil para COVID-19 em estágio avançado ,
https://openheart.bmj.com/content/7/ 2/e001350 .
DiNicolantonio (B) et al., Open Heart ,
doi:10.1136/openhrt-2021-001655 ,
https://openheart.bmj. com/content/8/1/e001655 .
doyourownresearch.substack.com ,
https://doyourownresearch.substack..the-together-trial/comment/6043250 .
doyourownresearch.substack.com (B) ,
https://doyourownresearch.substack..-solving-the-3-day/comment/6143361 .
doyourownresearch.substack.com (C) ,
https://doyourownresearch.substack../together-trial-impossible-numbers .
doyourownresearch.substack.com (D) ,
https://doyourownresearch.substack..the-together-trial/comment/6409395 .
doyourownresearch.substack.com (E) ,
https://doyourownresearch.substack..p-its?utm_source=twitter&sd=fs&s=r .
doyourownresearch.substack.com (F) ,
https://doyourownresearch.substack..p/together-trial-solving-the-3-day .
doyourownresearch.substack.com (G) ,
https://doyourownresearch.substack../what-went-wrong-with-the-together .
https://drive.google.com/file/d/1qh9U0FvrF-lNnNyuZ9_ljPS8PCXpAdzR/view .
https://drive.google.com/file/d/18OfEy2byeYQBxY_xRuQjgmwtRS8m23zu/view .
https://drive.google.com/file/d/1RewIbMErzo0ALy3au9NbTy6DHBeRd7D2/view .
https://ebm.bmj.com/content/23/5/165 .
Efimenko et al., International Journal of Infectious Diseases ,
doi:10.1016/j.ijid.2021.12.096 ,
https://www. sciencedirect.com/science/article/pii/S1201971221009887 .
doi:10.1136/bmj.315.7109.629 ,
Viés na meta-análise detectado por um teste gráfico simples ,
https://syndication.highwire.org/content/doi/10.1136/bmj.315.7109. 629 .
Elalfy et ai., J. Med. Virol. ,
https://onlinelibrary.wiley.com/doi/10.1002 /jmv.26880 .
doi:10.1101/2021.08.10.21261855 ,
https://www.medrxiv. org/content/10.1101/2021.08.10.21261855v1 .
Como a ivermectina se tornou um alvo para os ‘detetives de fraude’. ,
https://trialsitenews.com/how-iver..a-target-for-the-fraud-detectives/ .
https://empendium.com/mcmtextbook/..at-or-not-to-treat-platform-trials .
https://en.wikipedia.org/wiki/Ivermectin .
https://en.x-mol.com/paper/article/947631 .
Errecalde et al., Journal of Pharmaceutical Sciences ,
doi:10.1016/j.xphs.2021.01.017 ,
Safety and Pharmacokinetic Assessments of a Novel Ivermectin Nasal Spray Formulation in a Pig Model ,
https://www.sciencedirect.com/science/ artigo/pii/S0022354921000320 .
Espitia-Hernandez et al., Biomedical Research, 31:5 ,
https://www.biomedres.info/biomedi..- prova de conceito-estudo-14435.html .
Evans , R., Política de Saúde, 5:4 ,
Duro com o Crime? Pfizer e CIHR ,
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2875889/ .
Eweas et al., Frontiers in Microbiology ,
doi:10.3389/fmicb.2020.592908 ,
Molecular Docking Reveals Ivermectin and Remdesivir as Potential Repurposed Drugs Against SARS-CoV-2 ,
https://www.frontiersin.org/articles/10.3389/fmicb. 2020.592908/completo .
Faisal et al., The Professional Medical Journal ,
doi:10.29309/TPMJ/2021.28.05.5867 ,
http://theprofesional.com/index. php/tpmj/article/view/5867 .
Genomics and epidemiology of the P.1 SARS-CoV-2 lineage in Manaus, Brazil ,
https://www.science.org/lookup/doi/10.1126/ science.abh2644 .
O curioso valor-p perfeito: um estudo de caso em difamação e ignorância ,
https://www.normanfenton.com/post/..-study-in-defamation-and-ignorance .
Ferreira et al., Revista da Associação Médica Brasileira ,
doi:10.1590/1806-9282.20210661 ,
https://www.scielo.br/j /ramb/a/kzbmDvJqjJdQR9GfqK65CZs/ .
Figueroa et al., International Journal of General Medicine ,
doi:10.2147/IJGM.S328486 (pré-impressão 15/04/2021),
https://www.dovepress.com/efficacy..eer-reviewed-fulltext-article-IJGM .
files.covid19treatmentguidelines.nih.gov ,
https://files.covid19treatmentguid..treatmentguidelines-08-27-2020.pdf .
Fordham et al., OSF Preprints ,
The uses and abuses of sistemáticas revisões ,
Forrest et al., The American Journal of Tropical Medicine and Hygiene ,
https:/ /www.ajtmh.org/view/journals/tpmd/106/2/article-p389.xml .
Fox , C., RealClearInvestigations ,
https://www.realclearinvestigation..enting_doctors_say_yes_808045.html .
Francés-Monerris et al., Physical Chemistry Chemical Physics ,
https://pubs.rsc.org/en/Content /ArticleLanding/2021/CP/D1CP02967C .
Francés-Monerris (B) et al., ChemRxiv ,
doi:10.26434/chemrxiv.12782258.v1 ,
https://chemrxiv.org/articles/prep..itarget_Antiviral_Agent/12782258/1 .
https://www.francesoir.fr/societe-..-participants-letude-est-confirmee .
Galan et al., Pathogens and Global Health ,
doi:10.1080/20477724.2021.1890887 ,
https://www.tandfonline. com/doi/full/10.1080/20477724.2021.1890887 .
https://gatesopenresearch.org/articles/5-117 .
https://gatesopenresearch.org/articles/5-117/v2 .
Notícias de engenharia genética e biotecnologia ,
Merck buscará FDA EUA para pílula COVID-19 após dados positivos de fase III ,
https://www.genengnews.com/news/me..ill-after-positive-phase-iii-data/ .
George et al., Indian Journal of Hematology and Blood Transfusion ,
doi:10.1007/s12288-022-01546-w ,
https://link.springer.com/10.1007/s12288-022-01546-w .
Ghauri et al., International Journal of Clinical Studies & Medical Case Reports ,
doi:10.46998/IJCMCR.2021.13.000320 (pré-impressão 15/12/2020),
Uso de Ivermectina Associado à Duração Reduzida da Doença Febril Covid-19 em um Ambiente Comunitário ,
https://ijclinmedcasereports.com/pdf/IJCMCR-RA-00320.pdf .
gob.mx ,
https://www.gob.mx/salud/documentos/datos-abiertos-152127 .
González-Paz et al., Biophysical Chemistry ,
doi:10.1016/j.bpc.2021.106677 ,
https://www .sciencedirect.com/scie../article/abs/pii/S0301462221001599 .
González-Paz (B) et al., Journal of Molecular Liquids ,
doi:10.1016/j.molliq.2021.117284 ,
https://www.sciencedirect.com/science/article/pii/S0167732221020080 .
Os principais estudos de ivermectina são projetados para o fracasso? ,
https://trialsitenews.com/are-majo..ctin-studies-designed-for-failure/ .
doi:10.1101/2020.07.07.20145979 ,
Effectiveness of Ivermectin as add-on Therapy in COVID-19 Management (Pilot Trial) ,
https://www.medrxiv.org/content/10.1101/2020.07.07.20145979 v1 .
doi:10.1101/2021.03.04.21252084 ,
https://www.medrxiv.org /content/10.1101/2021.03.04.21252084v1 .
Guzzo et al., J. Clinical Pharmacology ,
https://accp1.onlinelibrary.wiley…7/009127002237994?sid =nlm%3Apubmed .
https://www.halifaxexaminer.ca/fea..he-deal-with-ivermectin-and-covid/ .
Harbord et al., Statistics in Medicine ,
https://api.wiley.com/onlinelibrary/tdm/ v1/articles/10.1002%2Fsim.2380 .
Hariyanto et al., Reviews In Medical Virology ,
https://onlinelibrary.wiley.com/ doi/abs/10.1002/rmv.2265 .
https://philharper.substack.com/p/professor-tied-to-altered-andrew?s=r .
Hashim et al., Iraqi Journal of Medical Science, 19:1 ,
http://www.iraqijms.net/upload/pdf/iraqijms60db8b76d3b1e .pdf .
doi:10.1101/2021.07.06.21259924 ,
Effectiveness of Ivermectin-Based Multidrug Therapy in Severe Hypoxic Ambulatory COVID-19 Patients ,
https://www.medrxiv.org/content/10.1101/2021.07.06.21259924v1 .
Heidary et al., The Journal of Antibiotics, 73, 593-602 ,
doi:10.1038/s41429-020-0336-z ,
Ivermectina: uma revisão sistemática de efeitos antivirais ao regime complementar de COVID-19 ,
https://www.nature .com/articles/s41429-020-0336-z .
Hellwig et al., International Journal of Antimicrobial Agents ,
doi:10.1016/j.ijantimicag.2020.106248 ,
A COVID-19 Prophylaxis? Menor incidência associada à administração profilática de Ivermectina ,
https://www.sciencedirect.com/science/article/pii/S0924857920304684 .
Henderson , J., MedPage Today ,
Ivermectin Arm of PRINCIPLE Trial Put on Hold — O site de teste cita problemas de fornecimento ,
https://www.medpagetoday.com/special-reports/exclusives/96194 .
Comunicado de imprensa Huvemek ,
Kovid-19 – Ensaio clínico Huvemek® Fase 2 ,
https://huvemec.bg/covid-19-huveme..linichno-izpitanie/za-isledvaneto/ .
IVERCOR PREP , Preliminary Results ,
Ivermectina en agentes de salud e IVERCOR COVID19 ,
https://twitter.com/Covid19Crusher/status/1365420061859717124 .
Randomized Controlled Trials: Questions, Answers, and Musings, Second Edition ,
https://onlinelibrary.wiley.com/doi/book/10.1002/9780470691922 .
https://jamanetwork.com/journals/jamanetworkopen/fullarticle/2779044 .
https://jamanetwork.com/journals/jama/fullarticle/2777389 .
https://www.cureus.com/articles/ 73..al-study-from-andhra-pradesh-india .
Jans et al., Cells 2020, 9:9, 2100 ,
Ivermectin as a Broad-Spectrum Host-Directed Antiviral: The Real Deal? ,
https://www.mdpi.com/2073-4409/9/9/2100 .
Jayk Bernal et al., New England Journal of Medicine ,
Molnupiravir for Oral Treatment of Covid-19 in Nonhospitalized Patients ,
http://www.nejm.org/doi/pdf/10.1056/NEJMoa2116044 .
Jeffreys et al., International Journal of Antimicrobial Agents ,
doi:10.1016/j.ijantimicag.2022.106542 (pré-impressão 24/12/2020),
https: //www.sciencedirect.com/science/article/pii/S0924857922000309 .
cientista israelense diz que o COVID-19 pode ser tratado por menos de US$ 1/dia ,
https://www.jpost.com/health-scien..d-be-treated-for-under-1day-675612 .
Jitobaom et al., Research Square ,
doi:10.21203/rs.3.rs-1069947/v1 ,
Synergistic Anti-SARS-CoV-2 Activity of Repurposed Anti-Parasitic Drug Combinations ,
https://www.researchsquare.com/article /rs-1069947/v1 .
Jitobaom (B) et al., Research Square ,
doi:10.21203/rs.3.rs-941811/v1 ,
Favipiravir and Ivermectin Showed in Vitro Synergistic Antiviral Activity against SARS-CoV-2 ,
https://www.researchsquare.com /artigo/rs-941811/v1 .
doi:10.1101/2020.11.30.20236570 ,
https://www.medrxiv.org/content/10.1101/2020.11.30.20236570 v1 .
doi:10.1101/2021.08.27.21262754 ,
https://www.medrxiv.org/content/10.1101/ 2021.08.27.21262754v1 .
Kern et al., Frontiers in Pharmacology ,
doi:10.3389/fphar.2021.625678 ,
Modeling of SARS-CoV-2 Treatment Effects for Informed Drug Repurposing ,
https://www.frontiersin.org/articles/10.3389/fphar.2021.625678/full .
doi:10.7759/cureus.21272 (pré-impressão 12/11/2021),
https:// www.cureus.com/articles/82..ts-using-propensity-score-matching .
Khan et al., Archivos de Bronconeumología ,
doi:10.1016/j.arbres.2020.08.007 ,
O tratamento com ivermectina pode melhorar o prognóstico de pacientes com COVID-19 ,
https://www.archbronconeumol.org/e..ognosis-articulo -S030028962030288X .
https://pharmashots.com/61076/merc..or-molnupiravir-to-treat-covid -19/ .
Kishoria et al., Paripex – Indian Journal of Research ,
doi:10.36106/paripex/4801859 ,
https: //www.worldwidejournals.com/..August_2020_1597492974_4801859.pdf .
Kory et al., American Journal of Therapeutics ,
doi:10.1097/MJT.0000000000001377 ,
https://journals.lww.com/americant. ._Evidence_Demonstrating_the.4.aspx .
Commentary on medical journals ,
https://twitter.com/PierreKory/status/1434741303527579648 .
Dr. Pierre Kory Fala Sobre Direitos Humanos e A Grande Desinformação da Ciência ,
https://www.youtube.com/watch?v=3UTuT9TSRFQ&t=2890s .
https://covid19criticalcare.com/wp..INFORMATION-CAMPAIGN-5.11.2021.pdf .
Krolewiecki et al., EClinicalMedicine ,
doi:10.1016/j.eclinm.2021.100959 ,
Antiviral effect of high-dose ivermectin in adult with COVID-19: A proof-of-concept random trial ,
https://www.sciencedirect.com/ science/article/pii/S258953702100239X .
https://b3d2650e-e929-4448 -a527-4e..b655bd21b1448ba6cf1f4c59f0d73d.pdf .
https://trialsitenews.com/a-letter-to-the-bbc/ .
Lee et al., Arch Intern Med., 2011, 171:1, 18-22 ,
doi:10.1001/archinternmed.2010.482 ,
https://jamanetwork.com /journals/j..nternalmedicine/fullarticle/226373 .
Lehrer et al., In Vivo, 34:5, 3023-3026 ,
Ivermectin Docks to the SARS-CoV-2 Spike Receptor-binding Domain Attached to ACE2 ,
http://iv.iiarjournals. org/content/34/5/3023 .
Li et al., J. Cellular Physiology ,
https://onlinelibrary.wiley.com/doi/10.1002 /jcp.30055 .
doi:10.1001/jamainternmed.2022.0189 (dados 3/11/21),
https://jamanetwork.com/journals/j..ternalmedicine/fullarticle/2789362 .
https://www.sciencedirect.com/science/article/pii /S1201971221001004 .
doi:10.1101/2022.01.20.477147 ,
https://www.biorxiv.org/ conteúdo/10.1101/2022.01.20.477147 .
https://longhaulwiki.com/resources..0with%20the%20TOGETHER%20trial.pdf .
https://jamanetwork.com/journals/jama /fullarticle/2777389 .
Loue et al., J. Infectious Diseases and Epidemiology ,
doi:10.23937/2474-3658/1510202 ,
Ivermectin and COVID-19 in Care Home: Case Report ,
https://www.clinmedjournals.org/ar..idemiology-jide -7-202.php?jid=jide .
Macaskill et al., Statistics in Medicine ,
Uma comparação de métodos para detectar viés de publicação em meta-análise ,
https://api.wiley.com/onlinelibrary/tdm/v1/articles/10.1002% 2Fsim.698 .
doi:10.1016/j.heliyon.2020.e05820 ,
https://www.sciencedirect.com/science/article/pii /S2405844020326633 .
Mahmud et al., Journal of International Medical Research ,
doi:10.5061/dryad.qjq2bvqf6 (pré-impressão 09/10/20),
https://journals.sagepub .com/doi/10.1177/03000605211013550 .
Manomaipiboon et al., Research Square ,
doi:10.21203/rs.3.rs-1290999/v1 ,
https://www.researchsquare.com/article/rs-1290999/v1 .
Mansour et al., International Immunopharmacology ,
doi:10.1016/j.intimp.2021.108004 ,
https://www.sciencedirect.com/science /article/pii/S1567576921006408 .
TOGETHER Trial: Solving the 3-Day Placebo Subgroup Riddle ,
https://doyourownresearch.substack..he-problem-with-the-together-trial .
The Problem With The TOGETHER Trial ,
https://doyourownresearch.substack..he-problem-with-the-together-trial .
Mayer et al., Frontiers in Public Health ,
doi:10.3389/fpubh.2022.813378 (preprint 23/09/2021),
Safety and Efficacy of a MEURI Program for the Use of High Dose Ivermectin in COVID-19 Patients ,
https:// www.frontiersin.org/articles/10.3389/fpubh.2022.813378/full .
McLean et ai., Open Forum Infect. Des. Setembro de 2015, 2:3 ,
https://www.ncbi.nlm.nih.gov/pmc/ artigos/PMC4525010/ .
medicospelavidacovid19.com.br ,
https://medicospelavidacovid19.com..icos-que-fazem-tratamento-precoce/ .
https://www.medscape.org/viewarticle/523643 .
Merck ,
Declaração da Merck sobre o uso de ivermectina durante a pandemia de COVID-19 ,
https://www.merck.com/news/merck-s..-use-during-the-covid-19-pandemic/ .
Mais de 30 anos: The Mectizan® Donation Program ,
https://www.merck.com/stories/mectizan/ .
https://www.merck.com/product/usa/..ars/s/stromectol/stromectol_pi.pdf .
http://web.archive.org/web/2021121.. 9?action=download&direct&version=1 .
https://www.health.com/nutrition/v..pplements/dr-fauci- vitamina-c-e-d .
https://www.mmsholdings.com/pfizer..-language-summary-writing-support/ .
Mody et al., Communications Biology ,
doi:10.1038/s42003-020-01577-x ,
https://www.nature. com/articles/s42003-020-01577-x .
Mohan et al., Journal of Infection and Chemotherapy ,
doi:10.1016/j.jiac.2021.08.021 (pré-impressão 2/2/2021),
https://www.sciencedirect.com/science/article/pii/S1341321X21002397 .
Mondal et al., Journal of the Indian Medical Association, 119:5 ,
https://onlinejima.com/read_journals .php?article=683 .
Moreno et al., BMC Medical Research Methodology ,
http://link.springer.com/article /10.1186/1471-2288-9-2/fulltext.html .
doi:10.7759/cureus.17455 (pré-impressão 16/04/2021),
https ://www.cureus.com/articles/63..matched-retrospective-cohort-study .
Morgenstern (B) et al., J. Clinical Trials (pré-impressão 11/3) ,
https://www.longdom.org/open-acces..talized-patients-with-clinical.pdf .
MD de Mountain Valley,
https://www.globenewswire.com/en/n..ariants-Tested-With-Ivectosol. html .
Mourya et ai., Int. J. Saúde e Pesquisa Clínica ,
https://ijhcr.com/index.php/ijhcr/article /view/1263 .
Muñoz et ai., PLoS Negl. Tropa Des. ,
doi:10.1371/journal.pntd.0006020 ,
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5773004/ .
doi:10.1001/jama.2020.26848 (pré-impressão 11/17),
https://jamanetwork.com/journals/jama/fullarticle/2776738 .
Mustafa et al., Pesquisa Exploratória em Farmácia Clínica e Social ,
doi:10.1016/j.rcsop.2021.100101 ,
https:// www.sciencedirect.com/science/article/pii/S2667276621001013 .
Muthusamy et al., Journal of Virology & Antiviral Research ,
https://www.scitechnol.com/abstrac..-sarscov2- spike-protein-16398.html .
doi:10.1101/2022.06.10.22276252 ,
://www .medrxiv.org/content/10.1101/2022.06.10.22276252 .
Nardelli et al., Signa Vitae ,
https://www.signavitae.com/articles/10.22514/sv.2021.043 .
nejm.org ,
https://www.nejm.org/doi/suppl/10…file/nejmcp2009249_disclosures.pdf .
https://www.nejm.org/doi/full/10.1056/NEJMc2102446 .
Nichol et al., Injury, 2010, doi: 10.1016/j.injury.2010.03.033 ,
Challenging issues in randomizado controlados ,
https://www.injuryjournal.com/article/S0020-1383(10)00233-0/ texto completo .
NIH ,
COVID-19 Treatment Guidelines: Ivermectin ,
https://www.covid19treatmentguidel..pies/antiviral-therapy/ivermectin/ .
Nonaka et al., International Journal of Infectious Diseases ,
doi:10.1016/j.ijid.2021.08.003 ,
https://www.sciencedirect.com/science/article/pii/S1201971221006354 .
Nunes et al., Brazilian Journal of Nephrology ,
doi:10.1590/2175-8239-JBN-2020-0105 ,
http://dx. doi.org/10.1590/2175-8239-jbn-2020-0105 .
A Lifeline from Buenos Aires ,
https://rescue.substack.com/p/a-li..ost&utm_medium=web&utm_source=copy .
https://odysee.com/@FrontlineCovid..weekly_webinar_6April2022:c?t=2507 .
https://odysee.com/@FrontlineCovid../weekly_webinar_6April2022:c?t=612 .
https://odysee.com/@FrontlineCovid..ents-defeating-the-delta-variant:a .
Okumuş et al., BMC Infectious Diseases ,
doi:10.1186/s12879-021-06104-9 (pré-impressão 1/12),
https://bmcinfectdis .biomedcentral..rticles/10.1186/s12879-021-06104-9 .
Ontai et al., Epidemiology International Journal ,
Early multidrug treatment of SARS-CoV-2 (COVID-19) and menores taxas de letalidade em Honduras ,
https://medwinpublishers.com/EIJ/e ..ase-fatality-rates-in-honduras.pdf .
Carta aberta de mais de 170 médicos dos EUA ,
JAMA Ivermectin Study Is Fatally Flawed ,
https://openpaymentsdata.cms.gov/physician/8802542 .
openpaymentsdata.cms.gov (B) ,
https://openpaymentsdata.cms.gov/physician/748947 .
openpaymentsdata.cms.gov (C) ,
https://openpaymentsdata.cms.gov/physician/249538 .
openpaymentsdata.cms.gov (D) ,
https://openpaymentsdata.cms.gov/physician/1273478 .
openpaymentsdata.cms.gov (E) ,
https://openpaymentsdata.cms.gov/physician/37453 .
openpaymentsdata.cms.gov (F) ,
https://openpaymentsdata.cms.gov/physician/200209 .
osf.io ,
https://www.otempo.com.br/interess..eocupa-por-risco-a-saude-1.2466432 .
https://ourworldindata.org/grapher/covid-variants-area?country=~BRA .
Ozer et al., Journal of Medical Virology ,
https://onlinelibrary.wiley.com/doi /10.1002/jmv.27469 .
Parvez et al., arXiv:2201.08176 [q-bio.OT] ,
https://arxiv.org/abs /2201.08176 .
doi:10.1101/2021.12.31.474653 ,
https://www.biorxiv .org/content/10.1101/2021.12.31.474653 .
Comparação de dois métodos para detectar viés de publicação em meta-análise ,
http://jamanetwork.com/journals/jama/fullarticle/202337 .
Análise da recomendação do FDA sobre ivermectina ,
https://twitter.com/marybethpf/status/1370182744718856193 .
https://pierrekory.substack.com/p/the-false-sinister-and-duplicitous .
https://pierrekory.substack.com/p/..itous?utm_source=twitter&sd=fs&s=r .
Podder et ai., IMC J. Med. Science, 14:2, julho de 2020 ,
http://imcjms.com/registration/journal_abstract/353 .
Popp et al., Cochrane Database of Systematic Reviews ,
doi:10.1002/14651858.CD015017.pub2 ,
Ivermectin for prevent and treatment COVID-19 ,
https://www.cochranelibrary.com/cd..0.1002/14651858.CD015017.pub2 /cheio .
Pott-Junior et al., Toxicology Reports ,
doi:10.1016/j.toxrep.2021.03.003 ,
Use of ivermectin in the treatment of Covid-19: a pilot trial ,
https://www.sciencedirect.com/science/article /pii/S2214750021000445 .
https://pubmed.ncbi.nlm.nih.gov/35528725/ .
https://pubpeer.com/publications/955418F3D4D39742CFFA8C1B023AA3 .
Qureshi et al., Journal of Biomolecular Structure and Dynamics ,
doi:10.1080/07391102.2021.1906750 ,
Mechanistic insights into the inibitory activity of FDA aprovou ivermectin against SARS-CoV-2: old drug with new requirements ,
https://www.tandfonline .com/doi/ab..02.2021.1906750?journalCode=tbsd20 .
doi:10.1016/j.chest.2020.10.009 ,
https://www.sciencedirect.com/science /article/pii/S0012369220348984 .
Rana et al., Research Square ,
doi:10.21203/rs.3.rs-755838/v1 ,
A Computational Study of Ivermectin and Doxycycline Combination Drug Against SARS-CoV-2 Infection ,
https://www.researchsquare.com/article /rs-755838/v1 .
Ravikirti et al., Research Square ,
doi:10.21203/rs.3.rs-1522422/v1 ,
https://www.researchsquare. com/article/rs-1522422/v1 .
Ravikirti (B) et al., Journal of Pharmacy & Pharmaceutical Sciences ,
https://journals.library .ualberta…/index.php/JPPS/article/view/32105 .
https://www.reddit.com/r/ivermecti..trial_was_not_randomized_possible/ .
Reis et al., New England Journal of Medicine ,
doi:10.1056/NEJMoa2115869 (resultados divulgados em 06/08/2021),
Effect of Early Treatment with Ivermectin between Patients with Covid-19 ,
https://www.nejm.org/doi /full/10.1056/NEJMoa2115869 .
Reis (B) et al., The Lancet Global Health ,
doi:10.1016/S2214-109X(21)00448-4 (pré-impressão 23/08/2021),
https://www.thelancet.com/journals../PIIS2214-109X(21)00448-4/fulltext .
Reuters ,
OMS se junta à Europa, Merck na recomendação contra a ivermectina para COVID-19 ,
https://news.trust.org/item/20210331135538-tajza/ .
Rezk et al., Zagazig University Medical Journal ,
doi:10.21608/zumj.2021.92746.2329 ,
miRNA-223-3p, miRNA-2909 and Cytokines Expression in COVID-19 Patients Treated with Ivermectin ,
https://journals.ekb.eg /article_202150_0.html .
https://rmed.acponline.org/authors..20.1631444170-955471710.1626461961 .
Rocha et al., Research Square ,
doi:10.21203/rs.3.rs-1640339/v1 ,
https:// www.researchsquare.com/article/rs-1640339/v1 .
Remdesivir para covid-19 grave: uma diretriz de prática clínica ,
https://www.bmj.com/content/370/bmj.m2924 .
Roman et al., Clinical Infectious Diseases ,
doi:10.1093/cid/ciab591 (preprint 25/05/21),
https:// academic.oup.com/cid/advan..le/doi/10.1093/cid/ciab591/6310839 .
Publication Bias in Meta-Analysis: Prevention, Assessment and Adjustments ,
https://www.wiley.com/en-ae/Public..nt+and+Adjustments-p-9780470870143 .
roundingtheearth.substack.com ,
https://roundingtheearth.substack…ta-analytical-fixers-an-ivermectin .
doi:10.1101/2021.03.08.21252883 ,
https://www.medrxiv.org/content /10.1101/2021.03.08.21252883v1 .
Rücker et al., Statistics in Medicine ,
Arcsine test for publishing bias in meta-analyses with binary results ,
https://api.wiley.com/onlinelibrary/tdm/v1/articles/10.1002% 2Fsim.2971 .
doi:10.1016/S0140-6736(21)00183-5 ,
Resurgence of COVID-19 in Manaus, Brazil, apesar da alta soroprevalência ,
https://www.thelancet.com/article/S0140-6736 (21)00183-5/texto completo .
Saha et al., Structural Chemistry ,
doi:10.1007/s11224-021-01776-0 (pré-impressão 3/1),
The Binding engine of ivermectin and levosalbutamol with spike protein of SARS-CoV-2 ,
https://www.researchsquare .com/article/rs-160254/v1 .
Samajdar et al., Journal of the Association of Physicians India, 69:11 ,
https:// japi.org/x2a464b4/ivermect..ice-of-physicians-vis-vis-outcomes .
Scheim , D., TrialsSite News ,
https://trialsitenews.com/mercks-d..ed- prêmio nobel-honrado-ivermectina/ .
Schöning et al., Research Square ,
doi:10.21203/rs.3.rs-379291/v1 ,
https://www. researchsquare.com/article/rs-379291/v1 .
https://www.scidev.net/america-lat..ta-saber-si-sirve-contra-covid-19/ .
https://www.sciencedirect.com/science/article/pii/S0166354220302199 .
Seet et al., International Journal of Infectious Diseases ,
doi:10.1016/j.ijid.2021.04.035 ,
https:/ /www.ijidonline.com/article/S1201-9712(21)00345-3/fulltext .
https://www. .mdpi.com/1999-4915/13/10/2084 .
Shahbaznejad et al., Clinical Therapeutics ,
doi:10.1016/j.clinthera.2021.04.007 (resultados parciais disponíveis 1/19),
Effect of ivermectin on COVID-19: A multicenter double-blind randomizado controlado ,
https:// www.sciencedirect.com/scie../article/abs/pii/S0149291821002010 .
Shimizu et al., Journal of Infection and Chemotherapy ,
doi:10.1016/j.jiac.2021.12.024 ,
https://www.jiac-j.com/article/S1341-321X(21)00360-3/fulltext .
Shouman et al., Journal of Clinical and Diagnostic Research ,
doi:10.7860/JCDR/2020/46795.0000 ,
Use of Ivermectin as a Potential Chemoprophylaxis for COVID-19 in Egypt: A Randomized Clinical Trial ,
https://www.jcdr.net /articles/PDF/..Sh)_PF1(SY_OM)_PFA_(OM)_PN(KM).pdf .
doi:10.1371/journal.pone.0264789 ,
https://journals.plos.org/plosone/. .le?id=10.1371/journal.pone.0264789 .
Soto-Becerra et al., medRxiv ,
doi:10.1101/2020.10.06.20208066 ,
https://www.medrxiv.org/content/10.1101/2020.10.06.20208066v1 .
Spoorthi et al., IAIM, 2020, 7:10, 177-182 ,
Utility of Ivermectin and Doxycycline Combination for the treatment of SARSCoV-2 ,
http://iaimjournal.com/wp-content/..oads/2020/10 /iaim_2020_0710_23.pdf .
Stanley et al., Research Synthesis Methods ,
Meta-regression aproximações para reduzir o viés de seleção de publicações ,
https://api.wiley.com/onlinelibrar..dm/v1/articles/10.1002%2Fjrsm. 1095 .
https://static1.squarespace.com/st..052/Together_MP_V2.0_25Mar2021.pdf .
https://static1.squarespace.com/st..65/Together_MP_V3.0_22June2021.pdf .
https://stevekirsch.substack.com/p/did-the-together-study-show-that .
Surnar et ai., ACS Pharmacol. Trad. Sci. ,
doi:10.1021/acsptsci.0c00179 ,
https://pubs.acs.org/doi/abs/10.1021/acsptsci.0c00179 .
Swargiary , A., Research Square ,
doi:10.21203/rs.3.rs-73308/v1 ,
https:/ /www.researchsquare.com/article/rs-73308/v1 .
Sweeting et al., Statistics in Medicine ,
https://onlinelibrary.wiley.com/doi/10.1002/sim.1761 .
Szente Fonseca et al., Travel Medicine and Infectious Disease ,
doi:10.1016/j.tmaid.2020.101906 ,
https://www.sciencedirect.com /scie../article/abs/pii/S1477893920304026 .
t.me ,
https://t.me/birdgroupuk/1942 .
https://www.tandfonline.com/doi/full/10.1080/25787489.2020.1844521 .
doi:10.1101/2021.03.26.21254377 ,
Por que o COVID-19 não é tão disseminado na África: como a ivermectina o afeta? ,
https://www.medrxiv.org/content/10.1101/2021.03.26.21254377v1 .
Thairu et al., Research Square ,
doi:10.21203/rs.3.rs-1373673/v1 ,
https://www.researchsquare.com/article/rs-1373673/v1 .
Thorlund et al., The American Journal of Tropical Medicine and Hygiene ,
Making Statistical Sense of the Molnupiravir MOVe-OUT Clinical Trial ,
https://www.ajtmh.org/view/journal. ./article-10.4269-ajtmh.21-1339.xml .
https://www.togethertrial.com/s/EN..19_AMB_02_Brazil_v10_17Dec2020.pdf .
https://www.togethertrial.com/s/Figure-2-with-ITT .
https://www.togethertrial.com/who-we-are .
https://www.togethertrial.com/protocols .
Treanor et al., JAMA, 2000, 283:8, 1016-1024 ,
https:// jamanetwork.com/journals/jama/fullarticle/192425 .
https://trialsitenews.com/nih-covi..ll-from-ivermectin-recommendation/ .
https://trialsitenews.com/grotesqu..nih-ivermectin-non-recommendation/ .
https://trialsitenews.com/nejm-rep..t-benefit-lets-take-a-closer-look/ .
https://trialsitenews.com/jama-ive..ceived-participants-on-study-drug/ .
https://trialsitenews.com/jama-una..tudy-consent-form-used-ivermectin/ .
https://trialsitenews.com/jama-ive..articipants-is-publicly-confirmed/ .
https://trialsitenews.com/is-there..g-the-trial-site-during-the-study/ .
https://trialsitenews.com/ivercovi..erdoses-ivermectin-comes-up-short/ .
https://trialsitenews.com/statemen..iseases-acceptance-of-roman-et-al/ .
https://twitter.com/rogjack6112/status/1455722142843215875 .
https://twitter.com/boulware_dr/status/1457905701573984261 .
https://twitter.com/alexandrosM/status/1530912240638959616 .
https://twitter.com/PPmerino/status/1489734477442019330 .
https://twitter.com/alexandrosM/status/1522469401198440449 .
https://twitter.com/sudokuvariante/status/1509451010972033024 .
https://twitter.com/alexandrosM/status/1511612742351798276 .
https://twitter.com/GabinJean3/status/1511289767379439618 .
https://twitter.com/mmpaquette/status/1509579476413210665 .
https://twitter.com/alexandrosM/status/1513903147755864067 .
https://twitter.com/millenamos/status/1516666147264815106 .
https://twitter.com/alexandrosM/status/1509400149608448000 .
https://twitter.com/fatlas8/status/1509444690638254084 .
https://twitter.com/alexandrosM/status/1509431705777565698 .
https://twitter.com/alexandrosM/status/1512180753769005061 .
https://twitter.com/alexandrosM/status/1513912773343809537 .
https://twitter.com/alexandrosM/status/1511111408150228997 .
https://twitter.com/alexandrosM/status/1518960937151074305 .
https://twitter.com/alexandrosM/status/1510765353462239232 .
https://twitter.com/alexandrosM/status/1510075920106762243 .
https://twitter.com/Amabiel1/status/1509292304951123970 .
https://twitter.com/alexandrosM/status/1513752737191583744 .
https://twitter.com/AOlavarria/status/1509603082195415043 .
https://twitter.com/alexandrosM/status/1510937829483839489 .
https://twitter.com/alexandrosM/status/1510931119725682693 .
https://twitter.com/alexandrosM/status/1510902227686223876 .
https://twitter.com/sudokuvariante/status/1512801565446447109 .
https://twitter.com/alexandrosM/status/1531711888454606849 .
https://twitter.com/alexandrosM/status/1531711890463723520/photo/3 .
https://twitter.com/alexandrosM/status/1531711899099729920 .
https://twitter.com/GabinJean3/status/1511289764044947460 .
https://twitter.com/alexandrosM/status/1512973870067724290 .
https://twitter.com/alexandrosM/status/1531711890463723520/photo/1 .
https://twitter.com/alexandrosM/status/1465867144705372161 .
https://twitter.com/Covid19Crusher/status/1426612910579757059 .
https://twitter.com/Covid19Crusher/status/1427255119800848386 .
https://twitter.com/GabinJean3/status/1511289679378669570 .
https://twitter.com/alexandrosM/status/1486080464523718660 .
https://twitter.com/Data_is_Louder/status/1447387394408321026 .
Udofia et al., Network Modeling Analysis in Health Informatics and Bioinformatics ,
doi:10.1007/s13721-021-00299-2 ,
https://link.springer.com/article/10.1007/s13721-021-00299-2 .
ufmg.br ,
https://ufmg.br/comunicacao/notici..rs-cov-2-pelo-estado-e-heterogenea .
Vallejos et al., BMC Infectious Diseases ,
doi:10.1186/s12879-021-06348-5 ,
https: //bmcinfectdis.biomedcentral..rticles/10.1186/s12879-021-06348-5 .
Ivermectina en agentes de salud e ivercor COVID-19: resultados al 18 de feb 2021 ,
https://twitter.com/Covid19Crusher/status/1365420061859717124 .
https://vimeo.com/690426154#t=33m00s .
https://vimeo.com/690426154#t=49m00s .
https://vimeo.com/690426154#t=29m00s .
https://vivo.weill.cornell.edu/display/cwid-rgulick .
Wagstaff et al., Ivermectin Global Sumit ,
In vitro Investigations of ivermectin as an antiviral agent ,
https://vimeo.com/554860553#t=1h32m0s .
http://web.archive.org/web/2014112..ww.medscape.org/viewarticle/523643 .
http://web.archive.org/web/2021091..jchamie/status/1438631284163715074 .
Wehbe et ai., Front. Immunol. ,
doi:10.3389/fimmu.2021.663586 ,
Reutilizando Ivermectina para COVID-19: Aspectos Moleculares e Possibilidades Terapêuticas ,
https://www.frontiersin.org/articles/10.3389/fimmu.2021.663586/full .
OMS ,
Therapeutics and COVID-19: Living Guideline 31 de março de 2021 ,
https://apps.who.int/iris/bitstrea..9-nCoV-therapeutics-2021.1-eng.pdf .
https://en.wikipedia.org/wiki/Molnupiravir .
doi:10.1101/2022.01.03.21268111 ,
https://www.medrxiv.org /content/10.1101/2022.01.03.21268111 .
Yagisawa et al., The Japanese Journal of Antibiotics, 74-1, Mar 2021 ,
Global trends in clinical studies of ivermectin in COVID-19 ,
http://jja-contents.wdc-jp.com/pdf/JJA74/74- 1-open/74-1_44-95.pdf .
https://www.bmj.com/content/363/bmj.k5094 .
Yesilbag et al., Virus Research ,
doi:10.1016/j.virusres.2021.198384 ,
https://www .sciencedirect.com/science/article/pii/S0168170221000915 .
Systemic unreported protocol violações in key ivermectin study ,
https://trialsitenews.com/systemic..iolations-in-key-ivermectin-study/ .
Yim (B) , P., TrialSite News ,
Grotesque conflitos de interesse na não recomendação do NIH ivermectina ,
https://trialsitenews.com/grotesqu..nih-ivermectin-non-recommendation/ .
Zaidi et al., The Journal of Antibiotics ,
doi:10.1038/s41429-021-00491-6 ,
Os mecanismos de ação da ivermectina contra SARS-CoV-2—uma revisão extensa ,
https://www.nature.com/articles /s41429-021-00491-6 .
Reportagem de notícias sobre os resultados In Vitro do instituto de pesquisa do Prof. Zatloukal ,
https://www.servustv.com/videos/aa-27juub3a91w11/ .
Zavascki et al., Research Square ,
doi:10.21203/rs.3.rs-910467/v1 ,
https://www.researchsquare.com/article/rs-910467/v1 .
doi:10.1101/2022.04.04.22273372 ,
https://www.medrxiv.org/content/10.1101/2022.04. 04.22273372 .
Zhang et al., JAMA, 80:19, 1690 ,
doi:10.1001/jama.280.19.1690 ,
https://jamanetwork.com/journals/jama/fullarticle/188182 .
Zheng et al., International Journal of Pharmaceutics ,
doi:10.1016/j.ijpharm.2022.121719 ,
Red blood cell-hitchhiking mediated lung delivery of ivermectin: Effects of nanoparticle properties ,
https://www.sciencedirect.com/science/article/ pii/S0378517322002745 .
Zubair et al., Monaldi Archives for Chest Disease ,
doi:10.4081/monaldi.2022.2062 ,
The effect of ivermectin on non-severe and serious COVID-19 disease and gender-based Difference of its Effective ,
https://monaldi-archives. org/index.php/macd/article/download/2062/1397 .Envie-nos correções, atualizações ou comentários. Vacinas e tratamentos são valiosos e complementares. Todos os meios práticos, eficazes e seguros devem ser usados. Nenhum tratamento, vacina ou intervenção está 100% disponível e eficaz para todas as variantes atuais e futuras. Negar a eficácia de qualquer método aumenta a mortalidade, a morbidade, os danos colaterais e o risco de endemia. Não fornecemos aconselhamento médico. Antes de tomar qualquer medicação, consulte um médico qualificado que possa fornecer aconselhamento personalizado e detalhes de riscos e benefícios com base em seu histórico médico e situação.
FLCCC e
WCH fornecem protocolos de tratamento.
Fonte: https://ivmmeta.com/
#ivermectina #estudosobreivermectina #covid19 #tratamentodocovid19 #ivermetinanotratamentodocovid19 #estudocientificodaivermectina #pmbnoticias


